
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Азеотропные смеси. Второй закон Коновалова
Однако не все смеси можно разделить обычной ректификацией. Есть смеси, которые не разделяются при разгонке, например, не разделяются смеси состава: бензол (60%) – метанол (40%); спирт этиловый (96%) – вода (4%) и т.д.
Температуры кипения некоторых азеотропных смесей приведены в табл. 8.1. Эти смеси имеют постоянную точку кипения, которая может быть выше или ниже температуры кипения высококипящего и низкокипящего компонентов раствора.
Коновалов Д.П. установил, что причиной невозможности разделения азеотропных смесей является совпадение состава жидкой и паровой фаз.
Если взять смесь состава «С», имеющего азеотроп с минимумом температуры кипения (рис. 8.10), и начать нагревать, то в паровую фазу будет в основном переходить азеотроп, а жидкая фаза будет обогащаться компонентом А.
Если взять эту же смесь состава «К», то при нагревании вновь в паровую фазу будет в основном переходить азеотроп, жидкая фаза будет обогащаться компонентом В.
Таблица 8.1
| Компоненты смеси | Состав смеси, % масс. | Температура кипения смеси, °С | Температура кипения компонента, °С |
| Бензол Метанол | 58,3 | ||
| Бензол Этанол | 68,2 | ||
| Толуол Бутанол | 105,5 |
При нагревании раствора, имеющего азеотроп с максимумом температуры кипения жидкая фаза обогащается азеотропной смесью (высококипящая часть), а в паровую фазу в большей степени будет поступать компонент А или В в зависимости от состава исходной смеси. Если смесь имела состав «С», то отгоняться будет компонент А; если смесь имела исходный состав «Д», то отгоняться будет компонент «В».
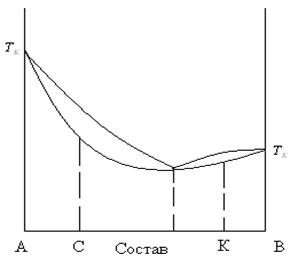
Рис. 8.10 Азеотропная смесь с минимум температуры кипения.
При горении в условиях пожара азеотропные смеси должны вести себя аналогично индивидуальным жидкостям, так как они имеют постоянные температуры кипения. Однако скорости их выгорания могут быть выше или ниже скоростей выгорания наиболее легкокипящего (азеотроп с минимумом температуры кипения) или выше высококипящего компонента (азеотроп с максимумом температуры кипения).
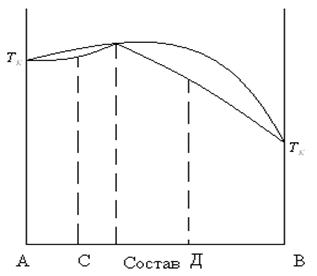
Рис.8.10 Азеотропная смесь с максимумом температуры кипения.
Литература
1. Воробьев В.К., Елисеев С.Ю., Врублевский А.В. Практические и самостоятельные работы по химии. – Мн.: УП «Донарит», 2005. – С. 58-60.
2. Елисеев С.Ю. Бинарные жидкие системы. Учебно-методическое пособие. – Мн.: КИИ МЧС РБ, 2004. – С. 28.
Тема 9. Электродные потенциалы. Электродвижущие силы. Электролиз
Лекция 9/1 Электродные потенциалы. Электродвижущие силы
Рассматриваемые вопросы:
1. Электродные потенциалы и механизм их возникновения.
2. Водородный электрод. Стандартные электродные потенциалы металлов. Ряд стандартных электродных потенциалов.
3. Принцип действия и электродвижущие силы гальванического элемента.
Для определения направления и полноты протекания окислительно-восстановительных реакций между окислительно-восстановительными системами в водных растворах используются значения электродных потенциалов этих систем.
Механизм возникновения электродных потенциалов, их количественное определение, процессы, которые сопровождаются возникновением электрического тока или вызваны электрическим током, изучаются особым разделом химии – электрохимией.
К электрохимическим относятся явления, возникающие на границе двух фаз с участием заряженных частиц (ионов и электронов), например, при погружении металлической пластинки в воду.
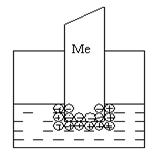
Для всех металлов характерно свойство в большей или меньшей степени растворяться в воде. При этом в воду переходят положительно заряженные ионы металла, в результате чего пластинка (из-за появления в ней избыточных электронов) заряжается отрицательно. Гидратированные катионы металла скапливаются возле поверхности пластинки на границе раздела двух фаз (металл-раствор). Возникает двойной электрический слой, характеризующийся некоторой разностью электростатических потенциалов. Как известно, энергию, которую необходимо затратить (положительный потенциал) или которую можно получить (отрицательный потенциал) при переносе единицы электричества из бесконечности в данную точку, называют электрическим потенциалом. Между пластинкой и раствором устанавливается окислительно-восстановительное равновесие:
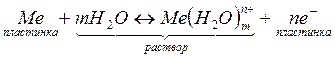 . (9.1)
. (9.1)
При погружении металла в раствор его соли также возникает двойной
электрический слой, но в этом случае возможны два механизма его образования. Если концентрация катионов металла в растворе мала или металл довольно активный, вследствие чего равновесие процесса, указанного выше, сдвинуто вправо, то металлическая пластинка заряжается отрицательно:
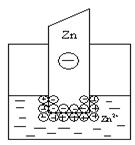
В том случае, когда концентрация катионов металла в растворе велика или металл малоактивный, равновесие указанного процесса сдвигается влево и металлическая пластинка заряжается положительно:

В любом случае на границе раздела двух фаз образуется двойной электрический слой. Разность (скачок) потенциалов, возникающая между металлом и жидкой фазой, называется электродным потенциалом Е. Потенциалу металла приписывается тот знак, который возникает на его поверхности в двойном электрическом слое.
Пластинка металла и раствор его соли (т.е. катионы этого металла) вместе составляют единую окислительно-восстановительную систему, характеризующуюся определенным электродным потенциалом, который зависит от природы металла, концентрации его ионов в растворе, от температуры и рН среды.
При определении скачка потенциала в окислительно-восстановительных системах, не содержащих твердой фазы (например, MnO4-/Mn2+ или Cr2O72-/Cr3+), используют инертные электроды (благородные металлы, графит). В этом случае инертные электроды, адсорбируя из раствора молекулы, атомы или ионы, играют роль твердой фазы, обеспечивающей возникновение скачка потенциалов на межфазной границе.
Экспериментально определить абсолютное значение электродного потенциала невозможно. Поэтому на практике измеряется разность потенциалов между электродным потенциалом исследуемой системы и потенциалом электрода сравнения. В качестве стандартного электрода сравнения обычно используют водородный электрод. Он изготавливается из губчатой платины, погруженной в раствор H2SO4 c активностью ионов водорода, равной единице (что соответствует примерно их концентрации, равной 1 моль/л). Через раствор при 298 К (25 оС) под давлением в 101,325 кПа пропускается газообразный водород, который поглощается губчатой платиновой пласти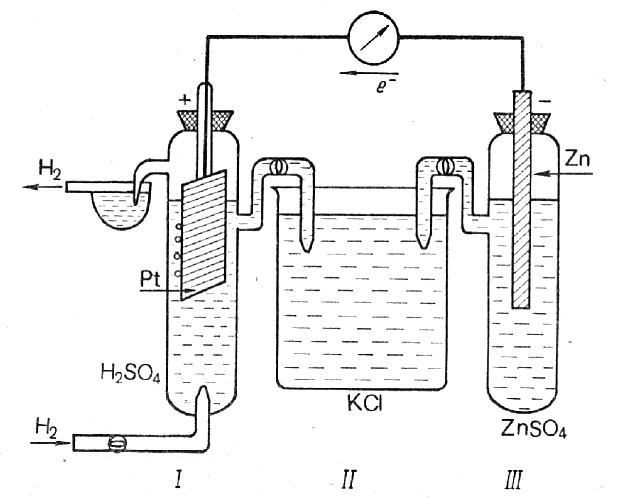 ной.
ной.
Рис.9.1 Гальваническая цепь для измерения электродного потенциала:
I – водородный электрод, II – солевой мостик, III – измеряемый электрод.
Таким образом, поверхность платинового электрода фактически насыщена водородом, в результате чего в системе устанавливается равновесие:
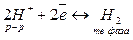 , (9.2)
, (9.2)
которое характеризуется определенным значением скачка потенциала на межфазной границе. Электродный потенциал, отвечающий данным условиям, получил название стандартного водородного потенциала 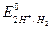 , а его численное значение условно принято равным нулю. Потенциал водородного электрода воспроизводится с очень высокой точностью.
, а его численное значение условно принято равным нулю. Потенциал водородного электрода воспроизводится с очень высокой точностью.
Сочетая электрод, представляющий исследуемую окислительно-восстановительную систему, со стандартным водородным электродом, определяют электродный потенциал Е данной системы. Для того, чтобы можно было сравнивать окислительно-восстановительные свойства различных систем по их электродным потенциалам, необходимо, чтобы последние также были измерены при стандартных условиях. Таковыми обычно являются концентрация ионов, равная 1 моль/л, давление газообразных веществ 101,325 кПа и температура 298,15 К. Потенциалы, измеренные в таких условиях, носят название стандартных электродных потенциалов и обозначаются Ео. Они часто называются также окислительно-восстановительными или редокс-потенциалами, представляя собой разность между редокс-потенциалом системы при стандартных условиях и потенциалом стандартного водородного электрода.
Знак конкретного Ео соответствует заряду электрода по отношению к стандартному водородному электроду.
Стандартный электродный потенциал – это потенциал данного электродного процесса при концентрациях всех участвующих в нем веществ, равных единице.
Стандартные электродные потенциалы окислительно-восстановительных систем приводятся в справочной литературе. Эти системы записаны в форме уравнений полуреакций восстановления, в левой части которых находятся атомы, ионы или молекулы, принимающие электроны (окисленная форма):
Ox + n×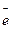 = Red. (9.3)
= Red. (9.3)
Эти системы в таблицах расположены в порядке возрастания величин их потенциалов, что соответствует падению восстановительной и росту окислительной активности. Система с большим электродным потенциалом всегда является окислителем по отношению к системе с меньшим потенциалом.
Выделяя из этого ряда окислительно-восстановительные системы типа Меn+/Me и располагая их в порядке возрастания стандартных электродных потенциалов, получают электрохимический ряд напряжений металлов: Li, Rb, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H2, Bi, Cu, Hg, Ag, Pd, Pt, Au.
Электрохимический ряд напряжений характеризует свойства металлов в водных растворах:
1. чем меньше электродный потенциал металла, тем легче он окисляется и труднее восстанавливается из своих ионов;
2. металлы, имеющие отрицательные электродные потенциалы, т.е. стоящие в ряду напряжений левее водорода, способны вытеснять его из разбавленных растворов кислот;
3. каждый металл способен вытеснять (восстанавливать) из растворов солей те металлы, которые имеют более высокий электродный потенциал.
При условиях, отличающихся от стандартных, численное значение равновесного электродного потенциала для окислительно-восстановительной системы, записанной в форме 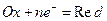 , определяется по уравнению Нернста:
, определяется по уравнению Нернста:
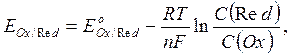 (9.4)
(9.4)
где 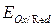 и
и 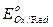 - соответственно электродный и стандартный потенциалы системы; R – универсальная газовая постоянная; Т – абсолютная температура; F – постоянная Фарадея; n – число электронов, участвующих в окислительно-восстановительном процессе.
- соответственно электродный и стандартный потенциалы системы; R – универсальная газовая постоянная; Т – абсолютная температура; F – постоянная Фарадея; n – число электронов, участвующих в окислительно-восстановительном процессе.
С(Red) и C(Ox) – молярные концентрации соответственно восстановленной и окисленной форм соединения.
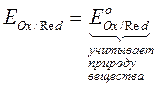 , когда C(Red) = C(Ox) = 1.
, когда C(Red) = C(Ox) = 1.
При подстановке численных значений R = 8,314 Дж/(моль×К), F=96494 Кл и Т (298 К) и замене натуральных логарифмов на десятичные уравнение упрощается:
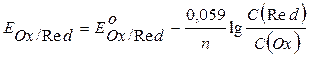 . (9.5)
. (9.5)
Например, для окислительно-восстановительной системы
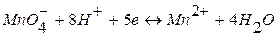
уравнение Нернста имеет вид
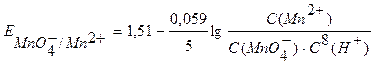 .
.
Ячейка для измерения электродного потенциала, например элемент Якоби-Даниэля, представляет собой пример электрохимического (гальванического) элемента – устройства, в котором химическая энергия окислительно-восстановительной реакции непосредственно преобразуется в электрический ток. Их называют также химическими источниками электрической энергии (ХИЭЭ).
Гальванический элемент состоит из двух полуэлементов (окислительно-восстановительных систем), соединенных между собой металлическим проводником и солевым мостиком. На каждом полуэлементе (часто называемом электродом) происходит полуреакция (электродный процесс). Процесс окисления (отдача электронов) осуществляется на аноде (отрицательный полюс), а восстановления (прием электронов) – на катоде (положительный полюс). Например, в представленном гальваническом элементе анодом является цинковый электрод: 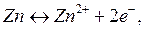
а катодом – водородный или медный электрод:
2Н+ + 2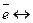 Н2
Н2

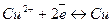 .
.
Электроны от анода по внешней цели протекают к катоду. Соответствующая схема такого гальванического элемента записывается следующим образом:
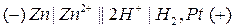 - водородный катод;
- водородный катод;
(-) Zn½Zn2+ êê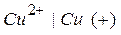 - медный катод.
- медный катод.
На схеме одна вертикальная линия изображает границу раздела фаз (элетрод-раствор), а две вертикальные линии – границу между растворами (на практике она обычно обеспечивается с помощью солевого мостика – U-образной трубки с раствором электролита, необходимого для замыкания цели между двумя электродами).
Причиной возникновения и протекания электрического тока в гальваническом элементе является разность электродных потенциалов (э.д.с) двух окислительно-восстановительных систем, соединенных между собой. Э.д.с (DЕ) любого гальванического элемента определяется общей формулой:
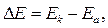
где Ек и Еа – электродный потенциал соответственно на катоде и на аноде.
Так как  может иметь только положительное значение, то Ек > Еа, т.е. катодом является электрод с более высоким электродным потенциалом.
может иметь только положительное значение, то Ек > Еа, т.е. катодом является электрод с более высоким электродным потенциалом.
При таком осуществлении окислительно-восстановительной реакции ее энергия превращается в электрическую энергию, которую можно использовать, включив во внешнюю цель устройство, потребляющее электрическую энергию (например, электронагревательный прибор, электрическую лампу и т.п.).
Действие любого гальванического элемента основано на протекании в нем окислительно-восстановительной реакции. В простейшем случае гальванический элемент состоит из двух пластин или стержней, изготовленных из различных металлов и погруженных в раствор электролита. Такая система делает возможным пространственное разделение окислительно-восстановительной реакции: окисление протекает на одном металле, а восстановление – на другом. Таким образом, электроны передаются от восстановителя к окислителю по внешней цепи. Например, элемент Якоби-Даниэля:
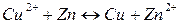 .
.
В принципе электрическую энергию может дать любая окислительно-восстановительная реакция. Однако число реакций, практически используемых в химических источниках электрической энергии, невелико.
Все обычные ХИЭЭ не свободны от недостатков: стоимость веществ, необходимых для их работы (Pb, Cd и т.д.) высока; отношение количества энергии, которую может дать элемент, к его массе мало.
Протекание окислительно-восстановительных процессов в сильной степени зависит от различных условий, прежде всего от природы реагирующих веществ, их концентрации, температуры и характера среды.
Так, концентрированная и разбавленная HNO3 по-разному восстанавливается при взаимодействии с одним и тем же восстановителем:
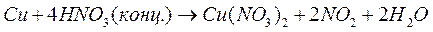 ;
;
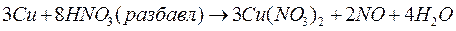 .
.
Классическим примером различия характера протекания реакций с одними и теми же окислителями и восстановителями является восстановление KМnO4 в зависимости от реакции среды:
рН < 7 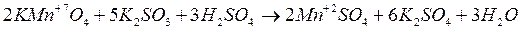
pH = 7 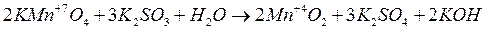
pH > 7 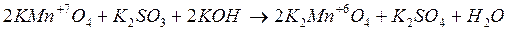
Как правило, для создания кислой среды используют относительно разбавленную Н2SO4 (реже HCl). Щелочная среда обычно создается с помощью растворов КОН и NaОН.
Изменение величины электродного потенциала каждой из двух полуреакций суммарного окислительно-восстановительного процесса и даже смена его направления могут быть достигнуты также за счет изменения температуры:
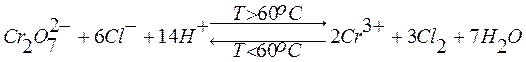 .
.
С помощью электродных потенциалов достаточно просто решается вопрос о составлении уравнений окислительно-восстановительных реакций, направлении и полноте их самопроизвольного протекания и т.п.
Как известно, термодинамическим условием самопроизвольного протекания химического процесса является отрицательное значение изменения изобарно-изотермического потенциала, т.е. DG < 0. Взаимосвязь между этой термодинамической функцией и э.д.с. гальванического элемента, составленного из двух окислительно-восстановительных систем, выражается формулой;
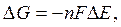
где n – число электронов, участвующих в суммарном окислительно-восстановительном процессе.
Из последнего выражения следует, что термодинамическим условием самопроизвольного протекания процесса в прямом направлении является положительное значение э.д.с (DЕ), когда система с более высоким значением электродного потенциала выступает в качестве окислителя, т.е. восстанавливается. Например, в гальваническом элементе, состоящем из двух электродов, характеризующихся следующими параметрами:
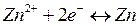
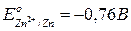
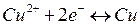
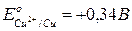
суммарный окислительно-восстановительный процесс самопроизвольно осуществляется при условии протекания восстановительной реакции только на медном электроде, а окислительной – на цинковом. Следовательно, в объединенном уравнении электродная реакция процесса с меньшим потенциалом записывается в обратном направлении, а процесса с большим потенциалом – в том виде, в каком она представлена в таблице, т.е. в форме процесса восстановления:
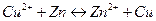
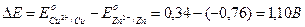 .
.
Если окислитель и восстановитель расположены достаточно далеко друг от друга в ряду стандартных электродных потенциалов, то направление окислительно-восстановительного процесса практически однозначно определяется их взаимным положением в этом ряду. При близких значениях Ео (разница меньше 0,3 В) необходимо учитывать, помимо рН среды и температуры, также концентрации реагирующих веществ, поскольку при изменении этих параметров процесса зачастую может изменяться и направление его протекания.
Применяя значение DЕо окислительно-восстановительной реакции, можно рассчитать ее константу равновесия. Для суммарного процесса типа 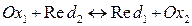 уравнение Нернста (при 298,15 К) имеет вид
уравнение Нернста (при 298,15 К) имеет вид
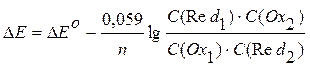 . (9.6)
. (9.6)
Отношение концентраций представляет собой выражение константы равновесия окислительно-восстановительного процесса:
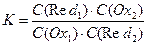
По мере протекания процесса концентрации Ох1 и Red2 уменьшаются, а Red1 и Ох2 – увеличиваются, что приводит в результате к значению DЕ = 0 и, следовательно, к DG = 0, характеризующему состояние равновесия:
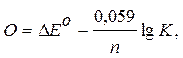
откуда К можно рассчитать по выражению:
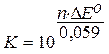 .
.
Литература
1. Глинка Н.Л. Общая химия. – Л.: Химия, 1978. – С. 270–290.
2. Шиманович И.Е., Павлович М.Л., Тикавый В.Ф., Малашко П.М. Общая химия в формулах, определениях, схемах. – Мн.: Унiверсiтэцкае, 1996. – С. 142 – 155.
3. Воробьев В.К., Елисеев С.Ю., Врублевский А.В. Практические и самостоятельные работы по химии. – Мн.: УП «Донарит», 2005. – С. 75-81.
Тема 9. Электродные потенциалы. Электродвижущие силы. Электролиз
Лекция 9/2 Электролиз
Рассматриваемые вопросы:
1. Электролиз с нерастворимыми и растворимыми электродами.
2. Законы Фарадея.
Электролиз – окислительно-восстановительный процесс, протекающий при прохождении постоянного электрического тока через раствор или расплав электролита.
При электролизе энергия электрического тока превращается в химическую энергию, иначе говоря, осуществляется процесс, обратный по характеру происходящему в гальваническом элементе. Как и в случае гальванического элемента, на аноде происходит окисление, а на катоде – восстановление. Но при электролизе анодом является положительный электрод, а катодом – отрицательный.
Характер протекания электродных процессов при электролизе зависит от многих факторов, важнейшими из которых являются состав электролита, материал электродов и режим электролиза (температура, плотность тока и т.д.).
Различают электролиз расплавов и растворов электролитов.
Электролиз расплавов электролитов.
 Электролиз расплава соли с использованием инертных электродов показан на следующей схеме:
Электролиз расплава соли с использованием инертных электродов показан на следующей схеме:
Анод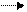
При высоких температурах расплав соли диссоциирует на ионы:
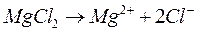 .
.
Прохождение электрического тока через расплав обусловлено тремя одновременно протекающими процессами:
1) направленное движение катионов Мg2+ к катоду, а анионов Cl- - к аноду;
2) восстановление, происходящее на катоде:
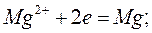
3) окисление, происходящее на аноде:
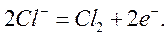
Суммарное уравнение электролиза после уравнивания числа отдаваемых и присоединенных электронов принимает вид:

Схематически весь процесс можно представить следующим образом:


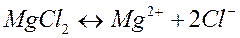
 Катод (-) Анод ( + )
Катод (-) Анод ( + )
Mg2+ 2Cl-
 Mg2+ + 2e- = Mg 2Cl- - 2e- = Cl2
Mg2+ + 2e- = Mg 2Cl- - 2e- = Cl2
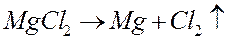
Электролиз растворов электролитов
Электролиз растворов электролитов более сложен из-за возможности участия в электродных процессах молекул воды в восстановлении на катоде:
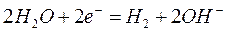
и окислении на аноде:
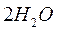
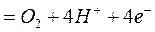 .
.
В тех случаях, когда на одном и том же электроде возможно протекание двух или большего числа процессов, наиболее вероятен тот, осуществление которого связано с минимальной затратой энергии. Это означает, что на катоде восстанавливаются в первую очередь окисленные формы окислительно-восстановительных систем с наибольшим электродным потенциалом, а на аноде окисляются восстановленные формы с наименьшим электродным потенциалом.
Для определения порядка протекания окислительно-восстановительных процессов на электродах при электролизе водных растворов можно руководствоваться следующими практическими правилами.
Катод.
1. В первую очередь восстанавливаются катионы металлов, имеющих стандартный электродный потенциал больший, чем у водорода, в порядке уменьшения Ео.
2. Катионы металлов с малым стандартным электродным потенциалом (от Li+ до Al3+ включительно) не восстанавливаются, а вместо них восстанавливаются молекулы воды (в кислой среде – ионы Н+).
3. Катионы металлов, имеющих стандартный электродный потенциал меньший, чем у водорода, но больший, чем у алюминия, восстанавливаются одновременно с молекулами воды.
Анод.
Характер окислительных процессов зависит также от материала электродов. Различают нерастворимые(инертные) и растворимые(активные)электроды.
Инертные электроды изготавливаются обычно из графита, угля, платины; в процессе электролиза они химически не изменяются, а служат лишь для передачи электронов во внешнюю цель.
При использовании инертных анодов следует учитывать следующее:
1. В первую очередь окисляются простые анионы в порядке возрастания их Ео, не превышающих + 1,5 В (S2-, J-, Br-, Cl-).
2. При электролизе водных растворов, содержащих анионы кислородосодержащих кислот (CO32-, NO3-, SO42-, PO43- и др.), на аноде окисляются не эти анионы, а молекулы воды.
3. В щелочных растворах на аноде окисляются ионы ОН-:
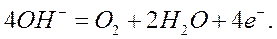
При использовании растворимых анодов (из Cu, Zn, Ag, Ni и др. металлов) электроны во внешнюю цель посылает сам анод за счет окисления атомов металла, из которого сделан анод:
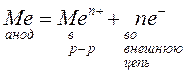 .
.
Рассмотрим конкретные примеры.
Электролиз водных растворов солей (инертные электроды)

 1)
1) 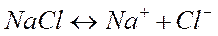

 ( - ) Катод Анод ( + )
( - ) Катод Анод ( + )
Na+, Н2О Cl-, H2O

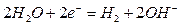
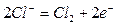
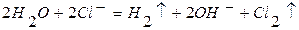
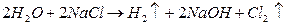

 2)
2) 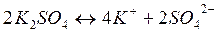

 ( - ) Катод Анод ( + )
( - ) Катод Анод ( + )
4К+, 4Н2О SO42-, Н2О

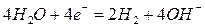
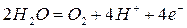
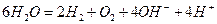
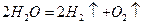
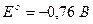


 3)
3) 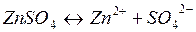
( - ) Катод Анод ( + )
Zn2+, H2O SO42-, H2O


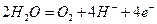
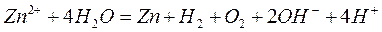
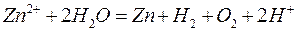
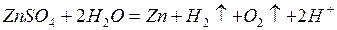
4) Электролиз водного раствора CuCl2 (активный медный анод)


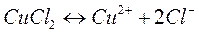

 ( - ) Катод Анод ( + )
( - ) Катод Анод ( + )
Cu2+, H2O 2Cl-, H2O



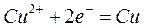
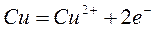
Количественные характеристики электролитических процессов устанавливаются двумя законами Фарадея:
I. Масса веществ, выделившихся на электродах при электролизе, прямо пропорциональна количеству электричества, прошедшего через раствор или расплав электролита.
II. При пропускании одинакового количества электричества через растворы или расплавы различных элементов масса веществ, выделяющихся на электродах, пропорциональна молярным массам их эквивалентов.
Экспериментально установлено, что для выделения на электроде одной молярной массы эквивалента вещества необходимо затратить одно и то же количество электричества, равное ~96500 Кл. Оно получило название постоянной Фарадея F.
Оба закона можно объединить общей формулой:
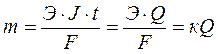 ,
,
где m – масса окисленного или восстановленного вещества, г; Э – молярная масса его эквивалента, г/моль; Q – количество электричества, прошедшее через элемент (Q = Jt, где J – сила тока, А; t – время, с).
Если Q = Jt = 1 Кл, то
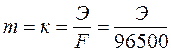 .
.
Величина К называется электрохимическим эквивалентом вещества. Она представляет собой массу вещества, окисляющегося или восстанавливающегося на электродах при прохождении через элемент 1 Кл электричества. Видно, что химический эквивалент связан с электрохимическим эквивалентом соотношением:
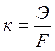 .
.
Показателем эффективности электролиза является выход по току η, %, определяемый как отношение массы вещества, фактически полученной в данных условиях электролиза mпракт, к массе вещества, теоретически вычисленной на основании закона Фарадея mтеор:
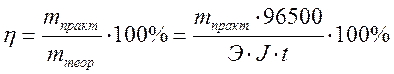 .
.
Области применения электролиза:
- получение металлов;
- очистка металлов от примесей (рафинирование);
- извлечение ценных компонентов;
- нанесение на поверхность металлических изделий слоев других металлов (гальваностегия);
- получение точных металлических копий с рельефных предметов электроосаждением металла (гальванопластика).
Пожарная опасность процессов электролиза.
- электролиз из расплавов предполагает присутствие высоких температур, что требует выполнения правил пожарной безопасности;
- процессы очень энергоемкие, с использованием электричества, что требует выполнения правил электробезопасности;
- возможность образования при протекании процессов водорода и кислорода, которые представляют собой пожароопасные и поддерживающие горение вещества;
- возможность образования кислот и щелочей, способных вызвать активную коррозию металлических конструкций электролизера;
- возможность образования хлора, который является отравляющим веществом.
Литература
1. Глинка Н.Л. Общая химия. – Л.: Химия, 1978. – С. 285 – 293.
2. Шиманович И.Е. и др. Общая химия в формулах, определениях, схемах. – Мн.: Унiверсiтэцкае, 1996. – С. 155 – 159.
3. Воробьев В.К., Елисеев С.Ю., Врублевский А.В. Практические и самостоятельные работы по химии. – Мн.: УП «Донарит», 2005. – С. 65-84.
ПРИЛОЖЕНИЯ
Приложение 1
Стандартные энтальпии образования (DНo) и энтропии (So) некоторых химических веществ
| Вещество | DНо, кДж/моль | So, Дж/(моль×град) |
| Неорганические вещества | ||
| С N2 O2 S Cl2 (г) H2 (г) F2 (г) P (бел) P (кр) Na (кр) I2 (кр) I2 (г) AlCl3 Al2O3 Al2(SO4)3 B2O3 (кр) BaO BaCO3 СО (г) СО2 (г) СОСl2 (г) CrO3 (кр) Cr2O3 (кр) HCl (г) HNO3 (ж) HF (г) H2O (г) H2O (ж) H2S (г) H I H2SO4 (ж) H3PO4 (ж) H3PO4 (кр) HClO4 KMnO4 (кр) KNO3 | -18,41 62,24 -698,0 -1676,0 -3434,9 1264,0 -556,6 -1215,0 -110,5 -393,5 -223,0 -594,5 -1141,0 -92,3 -173,0 -268,61 -241,84 -285,84 -20,1 25,9 -811,3 -1271,9 -1283,65 -814,53 -813,37 -492,7 | 5,7 191,5 205,0 31,9 223,0 130,5 202,9 44,35 22,8 51,42 116,73 260,58 167,0 50,9 - 53,85 70,4 112,3 197,5 213,6 289,2 81,1 186,7 156,16 173,51 188,74 69,96 205,64 200,0 156,9 200,83 176,15 171,95 171,71 132,93 |
| KOH (кр) K2Cr2O7 (кр) KNO2 K2O KO2 K2O2 KCl (кр) MnO (кр) NH3 NH4NO3 (кр) (NH4)2Cr2O7 (кр) (NH4)2SO4 NO (г) NO2 (г) N2O (г) NaOH NaOH (ж) Na2O (кр) Na2O2 (кр) NaF Na2CO3 Na2SO4 MgO (кр) MgCl2 MgCO3 PI3 (кр) PbO PbS SO2 (г) SO3 (г) CaO Ca(OH)2 CaCO3 CaCl2 Fe2O3 FeS2 ZnO SrO SrCO3 Ti TiO2 | -425,9 -2033,0 -380,87 -361,17 -209,76 393,73 -435,89 -384,93 -46,2 -365,1 -1885,6 -1179,0 90,37 33,89 81,55 -426,6 6,36 -430,6 -510,9 -570,09 -1129,0 -1380,0 -601,8 -641,8 -1096,2 -45,67 -217,9 -94,3 -296,9 -395,2 -638,0 -989,0 -1210,0 -799,0 -821,32 -177,4 -349,0 -591,0 -1220,0 -943,9 | 59,41 291,21 117,23 94,23 116,81 83,74 82,68 60,25 192,6 150,6 - 220,3 210,62 240,45 220,0 64,18 - 71,1 93,3 51,3 136,0 149,4 26,94 89,5 65,7 - 67,4 91,3 248,1 256,23 39,7 83,4 93,0 118,8 89,96 53,14 43,5 54,5 97,2 30,6 50,3 |
| Органические вещества | ||
| СН4 (г) С2Н2 (г) С2Н4(г) С3Н6 (г) С4Н6 (г) С6Н6 (ж) ССl4(г) ССl4(ж) С10Н8 С2Н5ОН(ж) СН3СОН (г) СН3СООН (ж) С2Н4(ОН)2 (ж) СН3СОСН3 (ж) С6Н5СН3(ж) С6Н5NO2 (ж) CH3OH(ж) | -74,85 226,75 52,3 -84,67 111,9 49,04 31,71 -0,72 -75,4 -272,6 -166,0 -484,9 -454,9 -247,7 8,1 11,2 -238 | 186,19 200,8 219,4 229,5 278,7 173,2 310,12 214,57 167,4 160,7 264,2 159,8 179,5 200,0 219,0 224,3 126,69 |
Приложение 2
| <== предыдущая страница | | | следующая страница ==> |
| Сущность разделения (разгонки) бинарных жидких растворов | | | Стандартные электродные потенциалы металлов при 293 К |
Дата добавления: 2014-04-24; просмотров: 942; Нарушение авторских прав

Мы поможем в написании ваших работ!