
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Биологически важные ароматические и гетероциклические соединения
Важнейшие биологически значимые гетероциклические и ароматические соединений, их синтезы и биосинтезы
Задание 1.Привести формулы и названия пятичленных гетероциклических соединений.
Ответ:
пиррол тиофен фуран индол
азол тиол оксол бензазол
Задание 2.Привести структуру важных производных пятичленных гетероциклов.
Ответ.Триптофан-предшественник гормонов –серотонина и мелатонина.
фурфурол – определяет запах свежеиспеченного хлеба, используется для синтеза антибактериальных средств
Задание 3. Привести схему биосинтеза серотонина и мелатонина, указать их биологическую роль.
Ответ.
| серотонин |
| ацилирование |
| гидроксилирование |
| мелатонин |
| триптамин |
| декарбоксилирование |
| алкилирование |
| триптофан |
Серотонин– синтезируется на свету, является гормоном радости, счастья, локально его концентрация возникает в местах воспаления, ушибов и вызывает боль. Мелатонинсинтезируется из серотонина ночью, определяяет сексуальную активность, способствует засыпанию (природное снотворное). Обладает антиоксидантным, геронтологическим, противоопухолевым действием.
Задание 4.Показать схему реакций нитрования бензола, фенола, триптофана. Продукты нитрования окрашены в желтый цвет, в щелочной среде – в оранжевый, поэтому реакция используется как качественная для доказательства ароматической природы соединений.
Ответ:
Для ароматических аминокислот реакция носит название ксантопротеиновой. В реакцию вступают фенилаланин, гистидин, триптофан. По реакции косвенно ценят о качественной ценности белка, содержащего ароматические и гетероциклические аминокислоты.
| фурфурол |
| рибоза |
| 5-нитрофурфурол |
| фурациллин |
| |
| гемоглобин |
| биллирубин |
Задание 7. Привести формулы пятичленных двухгетероатомных циклов и их производных. Указать их биологическую роль.
Ответ:
На основе гистидина (производного имидазола) синтезируется гистамин (отвечает за образование ряда биологических жидкостей (слезы, сопли), высокие уровни гистидина вызывают алергизацию организма.
| Пиразол (1,2-диазол) |
| Имидазол (1,3-диазол) |
| гистидин |
| амидопирин |
| анальгин |
| гистамин |
| |
Задание 8.Привести шестичленные одно- и двухатомные шестичленные гетероциклы и их биологически значимые производные..
Ответ. К шестичленным гетероциклам относится пиридин (азин), пиримидин (1,3-диазин), пиразин (1,4-диазин).
Большое значение имеют производные пиридина (никотиновая кислота), витамин В6 (пиридоксальфосфат), а также урацил, тимин, цитозин, входяцие в структуру нуклеиновых кислот.
| Никотиновая кислота пиридоксальфосфат (витамин В6) |
| Урацил цитозин тимин |
Соединения могут находиться в фенольной (лактимной) форме или в виде лактамов, последние в структуре нуклеиновых кислот преобладают.
1.
| Лактам-лактимная таутомерия производных пиримидина |
Задание 9.Привести гетероциклические соединения с несколькими гетероатомами.
Ответ.К производным пиримидина и тиазола относится витамин В1 (аневрин), который влияет на работу мышц (сердца, кишечника и др.), деятельность нервной системы. При недостатке возникает болезнь бери-бери. Содержится в оболочке злаковых культур, отруби обогащены витаминами группы В.
Производным птеридина является витамин Вс (фолевая кислота), участвующая в синтезе белка и кроветворении.
Производными пурина являются ряд соединений. Некоторые из них (аденин, гуанин) входят в структуру нуклеиновых кислот.
Продуктами окисления пурина являются гипоксантин, ксантин, мочевая кислота. Мочевая кислота не растворяется в воде и биологических и биологических жидкостях. При нарушении пуринового обмена мочевая кислота может откладываться в суставах, что приводит к подагре, а также в почках (мочекаменная болезнь).
К производным пурина относят теофиллин, теобромин, кофеин. Потребление большого количества шоколада, какао, кофе, чая может усугублять болезни, связанные с нарушением пуринового обмена.
II. Задания для самостоятельного решения.
Задание 1. Докажите ароматичность бензола, индола, пиридина, хинолина. Приведите продукты нитрования указанных соединений.
Задание 2Кислотно-основные свойства азотсодержащих гетероциклов (пиридина, хинолина, имидазола, пурина). Определение кислот и оснований по теории Бренстеда. Ряд основности. Получение солей
Задание 3.Напишите основные реакции превращения гистидина в организме человека (декарбоксилирование, дезаминирование), назовите продукты.
Задание 4. Тиофен. Структура гетероцикла. Биотин (витамин Н) - кофермент, участвующий в переносе карбоксильных групп.
Задание 5.Пиридин. Структура, критерии ароматичности, природа гетероатома. Биологически активные производные пиридина. Пиридоксаль, пиридоксальфосфат (витамин В6).
Задание 6..Пиримидин. Строение, природа гетероатомов, критерии ароматичности. Производные пиримидина: урацил, цитозин, тимин. Лактим-лактамная таутомерия.
Задание 7. Какой гетероцикл входит в составгема. Какие ферменты в качестве активного центра содержат порфириновый цикл?
Задание 8. Пурин. Структура, природа гетероатомов. Продукты окисления пурина (гипоксантин, ксантин, мочевая кислота). Таутомерия. Алкалоиды группы пурина (кофеин, теофиллин, теобромин). Применение в медицине.
Задание 9.
Выполнить превращения:
 Задание 10.
Задание 10.
| Окислительное дезаминирование |
А – β-индолилпировиноградная кислота
В - β-индолилуксусная кислота
Задание 11.
|
А – 5-гидрокситриптофан
В – серотони
С – мелатонин
Задание 12.Приведите формулы салициловой (I), пара-аминобензойной (II), сульфаниловой кислот (III). Укажите значение этих кислот для организма человека.
Ответ:
I II III
Салициловая кислота (I) синтезируется в организме, снижает свертываемость крови, проявляет жаропонижающее и противовоспалительное действие. На ее основе создано ряд препаратов. Пара-аминобензойная кислота (ПАБК) (II) является составной частью фолиевой кислоты, участвующей в кроветворении и синтезе белков. Замещенные производные ПАБК блокируют синтез белков у микроорганизмов и используются в качестве консервантов пищевых продуктов. На основе структуры фолиевой кислоты, включающей модифицированную (измененную) молекулу ПАБК, создана группа антибиотиков и противоопухолевых средств. Сульфаниловая кислота (III) близка по своим размерам ПАБК, на ее основе создана группа сульфаниламидных препаратов, используемых в качестве антибиотиков
Задания для самостоятельного решения.
Задание 1. Докажите ароматичность бензола, индола, пиридина, хинолина. Приведите продукты нитрования указанных соединений.
Задание 2Кислотно-основные свойства азотсодержащих гетероциклов (пиридина, хинолина, имидазола, пурина). Определение кислот и оснований по теории Бренстеда. Ряд основности. Получение солей
Задание 3.Напишите основные реакции превращения гистидина в организме человека (декарбоксилирование, дезаминирование), назовите продукты.
Задание 4. Тиофен. Структура гетероцикла. Биотин (витамин Н) - кофермент, участвующий в переносе карбоксильных групп.
Задание 5.Пиридин. Структура, критерии ароматичности, природа гетероатома. Биологически активные производные пиридина. Пиридоксаль, пиридоксальфосфат (витамин В6).
Задание 6..Пиримидин. Строение, природа гетероатомов, критерии ароматичности. Производные пиримидина: урацил, цитозин, тимин. Лактим-лактамная таутомерия.
Задание 7. Какой гетероцикл входит в составгема. Какие ферменты в качестве активного центра содержат порфириновый цикл?
Задание 8. Пурин. Структура, природа гетероатомов. Продукты окисления пурина (гипоксантин, ксантин, мочевая кислота). Таутомерия. Алкалоиды группы пурина (кофеин, теофиллин, теобромин). Применение в медицине.
Задание 9. Выполнить превращения:
Задание 10.
| Окислительное дезаминирование |
А – β-индолилпировиноградная кислота
В - β-индолилуксусная кислота
Тестовые задания для самостоятельного решения
1.Укажите формулу триптофана
а) б)
в) г)
2.Укажите формулу индола (бензпиррола).
а) б)
в) г)
3.Предшественником биосинтеза в организме мелатонина является:
а) фенилаланин б) триптофан
в) гистидин г) цистеин
4. Предшественником биосинтеза серотонина является
а) триптофан б) глицин
в) гистидин г) фенилаланин
5.Укажите формулу фурфурола (фуран-2-карбальдегида).
а) б)
в) г)
6. Выберите из предложенных формул никотиновую кислоту (пиридин-3-карбоновую кислоту).
а) б)
в) г)
7.Приведенное ниже соединение является витамином:
а) А б) В1
в) Н г) D
8. Приведенная ниже формула отражает структуру:
а) пурина б) гипоксантина
в) гемоглобина г) каталазы
9. Укажите формулу витамина РР (амида никотиновой кислоты).
а) б)
в) г)
10.Укажите формулу пиридоксина (лекарственной формы витамина В6)
а) б)
в) г)
11.Укажите формулу имидазола (1,3-диазола).
а) б)
в) г)
12. Салициловая кислота является
а) п.-сульфобензойной кислотой б) п.-аминобензойной кислотой
в) п.-бензолдикарбоновой кислотой г) о.-гидроксибензойной кислотой
13. Фолевая кислота в своей структуре содержит остаток:
а) п. –аминобнзойной кислоты б) терефталевой кислоты
в) сульфаниловой кислоты г) никотиновой кислоты
14. Витамин В1 в своей структуре включает гетероциклы:
а) пиридина и тиофена б) пиримидина и тиазола
в) пурина и имидазола г) пиперидина и тиазола
Важнейшие α-аминокислоты, пептиды.
ЦЕЛЬ:Сформировать знания о строении и свойствах важнейших a-аминокислот как химических основах структурной организации белковых молекул для дальнейшего изучения биологических функций белков на молекулярном уровне.
ЗНАТЬ:
1. Строение аминокислот. Классификация. Основы стереоизомерии.
2. Кислотно-основные свойства аминокислот. Биполярный ион, катионная, анионная формы. Изоэлектрическая точка. Показатель кислотности аминокислот.
3. Химические свойства аминокислот:
а) реакции по аминогруппе;
б) реакции по карбоксильной группе;
в) специфические и биологически важные реакции аминокислот (трансаминирование, окислительное дезаминирование, элиминирования, декарбоксилирование, окисление тиольных групп);
г) реакции в радикалах характеристических группах.
4. Образование, строение и свойства пептидной связи. Дипептиды, трипептиды, первичная структура белка.
5. Важнейшие пептиды: глутатион, карнозин, 6-аминопенициллоновая кислота, инсулин, окситоцин, вазопрессин, метионин - энкефалин, лейцин - энкефалин.
6. Первичная, вторичная, третичная, четвертичная структура белков. Функции белков в организме. Денатурация белков. Протеиды и протеины.
7. Свойства растворов высокомолекулярных соединений (ВМС).
УМЕТЬ:
1. Приводить структуры a-аминокислот, их классификацию по характеру бокового радикала.
2. Приводить схемы равновесия катионных, анионных, и диполярных форм для нейтральных, кислых и основных a-аминокислот.
2. Показывать химизм реакций декарбоксилирования, окислительного дезаминирования, элиминирования, окисления тиольных групп a-аминокислот.
3. Образовывать дипептиды, трипептиды, тетрапептиды..., уметь их называть, выделять пептидную связь с обозначением электронных эффектов.
4. Приводить схемы гидролиза пептидов.
ВЛАДЕТЬ:Навыками проведения цветных реакций (нингидринная, биуретовая, ксантопротеиновая, «формольное титрование», выявления меркаптогруппы) обнаружения a-аминокислот и пептидов с обоснованием результатов .
Обучающие упражнения
Задание 1. Один из стереоизомеров 2-амино-3-гидроксибутановой кислоты (треонин) входит в состав белков. Какие стереоизомеры возможны для треонина?
Ответ:в молекуле треонина два центра хиральности

Изобразим возможные стереоизомеры в виде проекционной формулы Фишера

| I | II | III | IV |
| L-алло-треонин | D-алло-треонин | D-треонин | L-треонин |
Для отнесения амино- и гидроксикислот к стереохимическим рядам, используется так называемый “гидроксильный ключ”, когда рассматривается конфигурация хирального центра с наименьшим номером.
По этому правилу стереоизомеры I и IV относятся к L ряду, а II и III к D-ряду. В состав белков входит L-треонин IV. Соединения I и II имеют эритроконфигурацию, т.е. заместители находятся в проекции Фишера по одну сторону углеродной цепи, в этом случае еще используется приставка алло-.
Заключение: I и II, III и IV - энантиомеры; I и III; I и IV; II и III; II и IV; диастереомеры.
Задание 2.На примере a-аланина и триптофана опишите схему образования биполярной структуры. Получите дипептиды образованные этими аминокислотами. Каковы особенности строения пептидной связи?
Ответ:
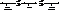
| катионная форма | биполярный ион | анионная форма |
В кислой среде a-аминокислоты существуют в виде катионной формы, в щелочной в виде анионной и в изоэлектрической точке в виде биполярного иона, т.е. одинаковое количество катионной и анионной форм.
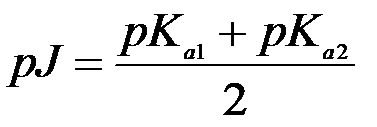 ,это формула для определения изоэлектрической точки
,это формула для определения изоэлектрической точки
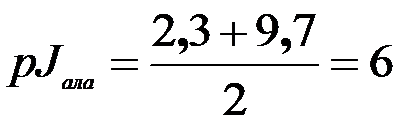
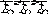
| катионная форма рКа1=2,4 | биполярный ион pJтри=5,9 | анионная форма рКа2=9,4 |
При взаимодействии триптофана и a-аланина могут образовываться четыре дипептида: Три-Ала, Ала-Три, Ала-Ала, Три-Три.
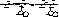
аланилтриптофан Ала-Три

аланилаланин Ала-Ала
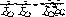
триптофанилтриптофан Три-Три
Строение пептидной связи
В составе пептидной (амидной) группы -СО-NH- атом углерода в sp2 гибридном состоянии, атом азота тоже в sp2 состоянии, неподеленная пара электронов атома азота вступает в сопряжение с p - электронами двойной связи С=О. Пептидная группа представляет собой трехцентровую p - р сопряженную систему, в которой электронная плотность смещена к кислороду, атомы С,О,N находятся в одной плоскости.
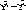
Вращение вокруг связи С-N затруднено, поэтому пептидная группа имеет плоскую, жесткую структуру.
Задание 3.Написать реакции внутри- и межмолекулярной конденсации a, b и g аминокислот.
Ответ:
а) a-аминокислоты при нагревании претерпевают межмолекулярную дегидратацию, при этом от двух молекул кислоты отщепляются две молекулы воды:
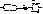
б) b-аминокислоты при нагревании отщепляют аммиак с образованием непредельных кислот:
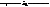
β-аминомасляная кислота кротоновая кислота
в) g - аминокислоты претерпевают внутримолекулярную дегидратацию:

γ-аминомасляная кислота γ-бутиролактон или пирралидон-2
Задания для самостоятельной работы
Задание 1. Напишите основные реакции превращения гистидина в организме человека. Назовите продукты.
Задание 2. Напишите схему метаболизма триптофана в организме человека (окислительное дезаминирование, декарбоксилирование, гидроксилирование), приводящие к образованию b-индолилпировиноградной кислоты, b-индолилуксусной кислоты, триптамина, серотонина и мелатонина.
Задание 4. На примере фенилаланина напишите уравнения реакций аминокислот с гидроксидом меди, азотной кислотой, формальдегидом. Получите дипептиды фенилаланина с глицином, назовите их.
Задание 5. Напишите реакции, образования дикетопиперазина и дипептида α-аланина.
Задание 6. Реакции гидроксилирования, как способ окисления непредельных и ароматических углеводородов. Продукты гидроксилирования фенилаланина, триптамина. Названия продуктов гидроксилирования.
Задание 7. Приведите уравнение реакции, по которой можно определить наличие в белке остатков аминокислот (цистеина, метионина), содержащих атомы серы.
Задание 8. Напишите структурные формулы цистеинилаланина.
Задание 9. Напишите строение трипептидного фрагмента - валил-глицил-аланина. Изобразите электронное строение пептидной группы.
Задание 10. Приведите строение дипептида гистидилаланина.
Задание 11. Напишите схему образования биполярной структуры аминокислот на примере триптофана и a-аланина. Получите дипептиды, образованные этими аминокислотами.
Задание 12. На пример a-аланина напишите уравнения реакций аминокислот с уксусным ангидридом, йодистым метилом, формальдегидом, метанолом(Н+).
Тестовые вопросы
1.Укажите формулу цистеина (2-амино3-меркаптопропановая кислота):
А) HSH2C–(NH2)HC–COOH;
Б) (H3C)2HC–(NH2)HC–COOH;
В) HОH2C–(NH2)HC–COOH;
Г) H2N–CH2–COOH
2. Какие из перечисленных аминокислот относят к ароматическим:
А) метионин (2-амино-3-метилтиопропановая кислота);
Б) лейцин (2-амино-5-метилпентановая кислота);
В) тирозин (2-амино-3-гидроксифенилпропановая кислота;
Г) пролин (2-карбоксипирролидин)
3. Изоэлектрическая точка белка рI=4,8. Какой заряд имеет этот белок в растворе с рН=6,7?
А) положительный -;
Б) отрицательный -  ;
;
В) нулевой
Г) не имеет заряда
4.Какое соединение образуется при декарбоксилировании серина
HO–H2C–(NH2)HC–COOH
А) 2-аминопропановая кислота;
Б) пропановая кислота;
В) 3-гидроксипропановая кислота;
Г) 2-аминоэтанол
5.По аминогруппе глицин H2N–CH2–COOH взаимодействует:
А) с метиламином Н2N - СН3;
Б) с уксусным ангидридом (СН3СОО)2О;
В) с пентахлоридом фосфора РCI5;
Г) с этанолом С2Н5ОН
6. В результате окислительного дезаминирования α-аланина образуется:
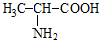
А) молочная кислота (2-гидроксипропановая кислота);
Б) этанол;
В) пропановая кислота;
Г) пировиноградная кислота (2-оксопропановая кислота)
7. Качественной реакцией обнаружения белков является:
А) реакция с нингидрином;
Б) биуретовая реакция;
В) ксантопротеиновая реакция;
Г) реакция серебрянного зеркала
8. Молекулы природных аминокислот являются:
А) L-стереоизомерами;
Б) D- стереоизомерами;
В) рацемической смесью D и L-стереоизомеров
Г) оптически неактивными
9. Какая аминокислота не участвует в образовании трипептида глутатион:
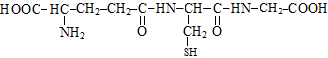
А) α-аланин;
Б) глицин;
В) цистеин;
Г) глутаминовая кислота
10. Название дипептида карнозин (содержится в мышечной ткани животных и человека) соответствует:
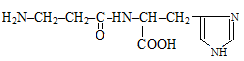
А) α-аланилгистидин; Б) гистидилаланин;
В) глицилгистидин; Г) β-аланилгистидин
| <== предыдущая страница | | | следующая страница ==> |
| Гетерофункциональные соединения (аминоспирты, гидрокси- и аминокислоты, оксокислоты) | | | Углеводы |
Дата добавления: 2014-09-10; просмотров: 1083; Нарушение авторских прав

Мы поможем в написании ваших работ!