
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Атомно-кристаллическое строение металлов
Тема 1. Строение металлов.
Введение
Право на забастовку, его гарантии и ограничения
Материаловедение — наука, изучающая связь между составом, строением и свойствами металлических сплавов и неметаллических материалов, а также рассматривающая закономерности их изменения под влиянием механических, физико-химических и других видов воздействий.
Металлы - простые вещества, обладающие высокой тепло- и электропроводностью, блеском, непрозрачностью и другими свойствами, характерными для металлов. Металлы и сплавы на их основе обладают комплексом механических, физических, химических и технологических свойств, обеспечивающих широкое их применение в различных отраслях техники.
Все металлы условно делят на черные (железо и сплавы на его основе — сталь, чугун) и цветные (все остальные).
Цель лекции:получить знания о металлических типах связи.
Твердые тела в зависимости от скорости охлаждения при кристаллизации делят на аморфные и кристаллические.
Аморфныйметалл получается при скоростях охлаждения 106...107 °С/с и более в виде тонких лент или мелких частиц. Атомы при этом не располагаются в правильном порядке, не образуют кристаллов. Аморфное твердое тело является изотропным, т.е.обладает одинаковыми свойствами во всех направлениях.
В кристаллическихтвердых телах (при меньших скоростях охлаждения) атомы расположены в геометрически правильном порядке, образуя кристаллы и создавая кристаллическую решетку или воображаемую пространственную сетку. Кристаллическим веществам свойственна анизотропия свойств, они имеют различные свойства в разных направлениях, т.е. число атомов, приходящееся на то или иное плоское сечение кристаллической решетки, неодинаково.
Металлы имеют кристаллические решетки различных типов. Чаще всего встречаются три типа: кубическая объемно-центрированная (ОЦК), кубическая гранецентрированная (ГЦК) и гексагональная плотноупако-ванная (ГПУ) кристаллические решетки.
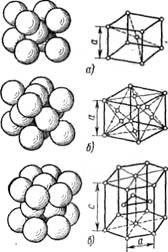 В элементарной ячейке кубической объемно-центрированной решетки (рис. 1, а) содержится девять атомов: восемь располагаются по узлам ячейки и один атом — в центре. Такой тип решетки имеют литий, натрий, калий, рубидий, ванадий, молибден, вольфрам, ниобий, тантал, α-железо и другие металлы.
В элементарной ячейке кубической объемно-центрированной решетки (рис. 1, а) содержится девять атомов: восемь располагаются по узлам ячейки и один атом — в центре. Такой тип решетки имеют литий, натрий, калий, рубидий, ванадий, молибден, вольфрам, ниобий, тантал, α-железо и другие металлы.
В элементарной ячейке кубический гранецентрированной решетки (рис. 1,б) находится четырнадцать атомов, которые расположены в углах ячейки и в центре каждой грани. Этот тип
решетки имеют свинец, никель, серебро, золото, медь, алюминий, платина, кальций, γ-железо, церий, α -кальций и др.
В элементарной ячейке гексагональной плотноупакованной решетки (рис.1, в) содержится семнадцать атомов, которые расположены в углах ячейки и центрах шестигранных оснований призмы и три атома в средней плоскости призмы. Такую решетку имеют магний, цинк, кадмий, рений, бериллий, гафний, титан (α -фаза), осмий и др.
Размеры кристаллической решетки характеризуются
Рис.1 Элементарные кристаллические
ячейки:
а) кубическая объемно-центрированная;
б) кубическая гранецентрированная;
в) гексогональная плотноупакованная
расстоянием между центрами соседних атомов, находящихся в вершинах элементарных ячеек, называемым параметром или периодом решетки. Кубическую решетку характеризует один параметр — длина ребра куба а, а гексогональную — два параметра а и с или их отношение с/а.
В кристаллах всегда имеются дефекты (несовершенства) строения, вызванные нарушением расположения атомов в кристаллической решетке. Дефекты кристаллического строения по геометрическим признакам подразделяют на точечные, линейные и поверхностные.
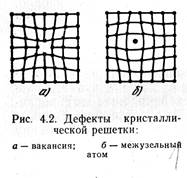
К точечным дефектам относят вакансии и межузельные атомы. Известно, что атомы находятся в колебательном движении около узлов решетки. Освободившееся место, где находился переместившийся атом, называется вакансией (рис.2,а). Число вакансий увеличивается с повышением температуры, при обработке давлением, облучении и других видах обработки. Межузельные дефекты образуются в результате перехода атома из узла решетки в межузлие кристаллической решетки.
Линейные дефекты называются дислокациями. Различают два вида дислокаций — краевые и винтовые.
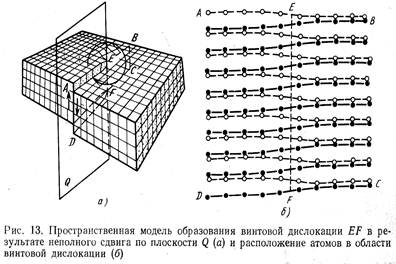
Краевая дислокация (рис.3,а) представляет собой местное искажение кристаллической решетки; винтовая дислокация образуется при неполном сдвиге кристалла по плоскост (рис.3,б). Дислокации образуются в процессе кристаллизации, при термической и химико-термической обработках, пластической деформации и других видах воздействий на структуру сплавов. Для дислокации характерна большая подвижность. Это связано с тем, что кристаллическая решетка в зоне нахождения дислокации упруго искажена, а смещенные атомы стремятся переместиться в равновесное положение. На свойства металлов влияет не только плотность дислокаций, но и их расположение в объеме.

Поверхностные дефекты представляют собой поверхности раздела между отдельными кристаллитами или их блоками. На границах зерен расположение атомов менее правильное, чем в зерне.
Металлы и сплавы находятся в трех агрегатных состояниях — твердом, жидком и газообразном. Переход металла из жидкого состояния в твердое (кристаллическое) называется кристаллизацией. Этот вид кристаллизации называется первичной в отличие от вторичной кристаллизации (перекристаллизации), которая имеет место в твердом металле. В чистых металлах твердое тело переходит в жидкое при температуре плавления, жидкое в газообразное – при температуре кипения. Температура плавления металлов колеблется от – 39 0С (для ртути, самого легкоплавкого металла) до + 3390 °С (для самого тугоплавкого металла вольфрама).
Схема кристаллизации металла (рис. 4). До тех пор, пока формирующийся вокруг центра кристаллизации кристалл окружен жидким расплавом металла, он имеет правильную геометрическую форму, но при столкновении и срастании кристаллов их
 |
правильная форма нарушается и образуются так называемые кристаллиты — зерна. Величина зерна зависит от числа центров кристаллизации и скорости роста. На образование центров кристаллизации влияет скорость охлаждения.__Чем больше степень охлаждения, тем больше центров кристаллизации и меньше размер зерна. Чем мельче зерно, тем выше механические свойства металла (сплава); особенно это сказывается на пластичности. На процесс кристаллизации оказывает влияние ультразвук; модифицирование; введение порошков, частицы которых служат центрами кристаллизации; поверхностно-активные вещества, облегчающие образование зародышей и др.
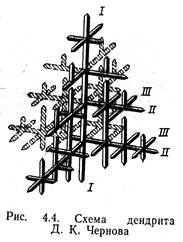
Механизм образования кристаллов носит дендритный характер. Это связано с тем, что развитие зародышей протекает главным образом в тех направлениях решетки, которые имеют наибольшую плотность упаковки атомов и минимальное расстояние между ними. В этих направлениях образуются ветви — оси первого порядка I (рис.5). От осей первого порядка начинают расти новые оси второго порядка II, от осей второго порядка — оси третьего порядка III и т. д.
Полиморфизмомили аллотропией и называют способность металла в твердом состоянии при изменении температуры перестраивать свою кристаллическую решетку. Различные аллотропические состояния называют модификациями. Каждой модификации свойственно оставаться устойчивой лишь в пределах определенного для данного металла интервала температур. Аллотропические формы обозначаются греческими буквами α, β, γ и т. д. На кривых охлаждения и нагрева переход из одного состояния в другое характеризуется остановкой (для чистых металлов) или изменением характера кривой (для сплавов).
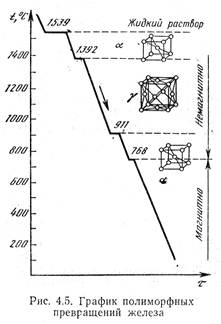
Железо известно в двух полиморфных модификациях (рис.6) – α и γ. В интервале температур 911...1392°С железо имеет кубическую гранецентрированную решетку γ -железа (Fеγ), а в интервале от 0 до 911 °С и от 1392 до 1539 °С— объемно центрированную решетку α -железа (Fеα). Железо меняет свои магнитные свойства: выше 768 °С железо немагнитно, а ниже — магнитно.
| <== предыдущая страница | | | следующая страница ==> |
| Начало коллективного трудового спора | | | Понятие о строении сплавов |
Дата добавления: 2014-02-26; просмотров: 1186; Нарушение авторских прав

Мы поможем в написании ваших работ!