
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Коррозия металлов
Коррозия металлов – это процесс их самопроизвольного разрушения при взаимодействии с окружающей средой.
Ежегодно из-за коррозии теряются огромные количества металла. По ориентировочным данным от 5 до 30% получаемых чёрных металлов разрушается в результате коррозии. Однако во многих случаях косвенные убытки от коррозии могут значительно превышать прямые потери за счёт растворения металла. Это и выход из строя металлических конструкций, сложных приборов и аппаратуры, простой оборудования, утечки нефти и газа из прокорродировавших трубопроводов, сопровождаемые при этом нанесением природе невосполнимого экологического ущерба. Поэтому изучение причин, вызывающих коррозию, установление влияния различных факторов на скорость коррозии имеют своей практической целью защиту металлов и сплавов от коррозионного разрушения при их обработке и эксплуатации.
Механизм коррозии. По механизму протекания коррозионного процесса различают химическую и электрохимическую коррозию.
Химическая коррозия характерна для сред, не проводящих электрический ток. В процессе химической коррозии происходит прямое гетерогенное взаимодействие металлов с окислителем окружающей среды, в результате которого между ними совершается обмен электронами, т.е. протекает обычная ОВР. Примером может служить окисление металлов кислородом воздуха при высоких температурах: Me + O2 ® MeO.
Электрохимическая коррозия возникает при контакте металлов с электролитами (во влажном воздухе, в почве, в растворах электролитов и т.п.) и является результатом протекания сопряжённых электродных процессов в образующихся короткозамкнутых гальванических элементах.
 Процессы электрохимической коррозии подобны процессам, протекающим в гальванических элементах. Основным отличием процессов электрохимической коррозии от процессов в гальваническом элементе является отсутствие внешней цепи. Электроны в процессе коррозии двигаются внутри металла от анодных участков к катодным, т.е. образуются короткозамкнутые гальванические элементы, в которых анодные и катодные участки замкнуты накоротко через сам металл.
Процессы электрохимической коррозии подобны процессам, протекающим в гальванических элементах. Основным отличием процессов электрохимической коррозии от процессов в гальваническом элементе является отсутствие внешней цепи. Электроны в процессе коррозии двигаются внутри металла от анодных участков к катодным, т.е. образуются короткозамкнутые гальванические элементы, в которых анодные и катодные участки замкнуты накоротко через сам металл.
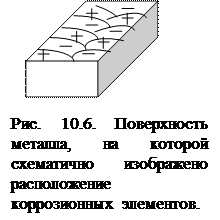
Отличающиеся по своим физическим и химическим свойствам участки корродирующей поверхности металла, на которых происходит анодный или катодный процессы, являются в зависимости от их размеров короткозамкнутыми макрогальваническими элементами (имеющими размеры, хорошо различимые невооружённым глазом) и микрогальваническими (обнаруживаемыми лишь при помощи микроскопа), т.е. явлются коррозионными элементами. Обычно поверхность корродирующего металла представляет собой многоэлектродный коррозионный элемент (чередование катодных и анодных участков – рис. 10.6). В первом приближении эту поверхность можно считать как двухэлектродную систему, т.е. состоящую из участков двух видов: анодных и катодных. Коррозионный элемент (короткозамкнутый гальванический элемент) схематично можно изобразить:
(–) А | коррозионная среда | К (+)
При работе коррозионных элементов, т.е. при электрохимической коррозии имеют место три основных процесса (рис. 10.7):
|
Me(K) – neˉ ® Men+(p)
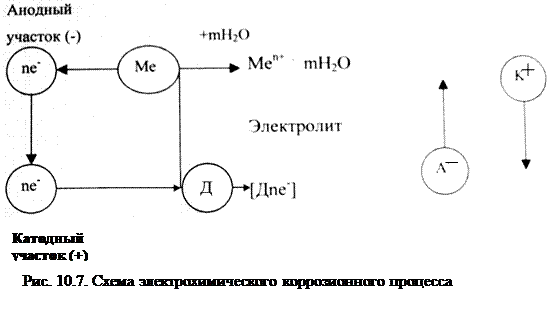
2. Процесс перетекания электронов по металлу от анодных участков к катодным и соответствующее перемещение катионов и анионов в растворе.
3. Катодный процесс – приём электронов каким – либо окислителем окружающей коррозионной среды (какими – либо ионами или молекулами – деполяризаторами) на границе раздела фаз металл -коррозионная среда:
Ох + neˉ ® Red или Д + neˉ ® [Дneˉ].
В коррозионных процессах окислитель часто называют деполяризатором1 (Д); [Дneˉ] – восстановленная форма окислителя.
Таким образом, электрохимическая коррозия на неоднородной (гетерогенной) поверхности металла аналогична работе короткозамкнутого гальванического элемента.
Наиболее распространёнными окислителями, деполяризаторами в коррозионном процессе являются ионы водорода и молекулы кислорода. Коррозия с участием ионов водорода называется коррозией с выделением водорода или коррозией с водородной деполяризацией. В наиболее простом виде электродные процессы для этого случая могут быть представлены уравнениями:
а) в кислых растворах (pH < 7)
А: Ме - neˉ ® Men+
K: 2Н+ + 2еˉ 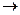 Н2
Н2  ;
;
б) в деаэрированных2 (удален растворенный кислород) нейтральных и щелочных растворах (рН 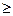 7)
7)
А: Ме - neˉ ® Men+
К: 2H2O + 2e- ® H2 + 2OH  .
.
Потенциал восстановления ионов водорода (потенциал водородного электрода) зависит от парциального давления водорода и рН. При 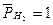 (101кПа) данный потенциал рассчитывается по уравнению:
(101кПа) данный потенциал рассчитывается по уравнению:
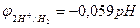 .
.
Например, при рН = 0 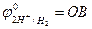 ;
;
рН = 7 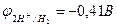 ;
;
рН = 14 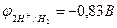 .
.
Коррозия с водородной деполяризацией возможна, если потенциал восстановления ионов водорода больше потенциала окисляемого металла, т.е. когда ЭДС образующегося короткозамкнутого гальванического элемента больше нуля: Еэ = jк - jа = jок-ль - jв-ль > О.
Скорость коррозии с водородной деполяризацией зависит от рН и температуры среды, природы металла.
Коррозия с участием кислорода называется коррозией с поглощением кислорода или коррозией с кислородной деполяризацией. Электродные процессы в этом случае могут быть представлены уравнениями:
А: Ме - neˉ ® Men+
K: О2 + 2H2O + 4eˉ ® 4OH 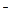 .
.
Необходимо отметить, что в обычных условиях во всех растворах есть растворённый кислород – О2. Потенциал восстановления кислорода (потенциал кислородного электрода) зависит от парциального давления кислорода и рН среды. При 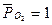 (101 кПа) данный потенциал рассчитывается по уравнению
(101 кПа) данный потенциал рассчитывается по уравнению
 .
.
Например, при рН = 0 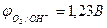 ;
;
рН = 7 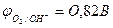 ;
;
рН = 14  .
.
|
|
|
|
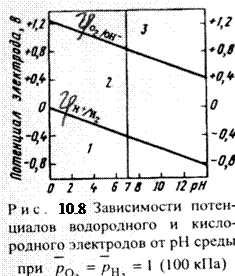 На рис. 10.8 представлена диаграмма потенциал – рН, позволяющая определять возможность коррозии различных металлов с водородной и кислородной деполяризацией. Если ЭДС коррозионного элемента Еэ > О, то коррозия возможна. Так как ЭДС равна разности потенциалов окислителя и восстановителя Еэ = jок-ль - jв-ль , то коррозия возможна при условии, что потенциал окислителя больше потенциала металла:
На рис. 10.8 представлена диаграмма потенциал – рН, позволяющая определять возможность коррозии различных металлов с водородной и кислородной деполяризацией. Если ЭДС коррозионного элемента Еэ > О, то коррозия возможна. Так как ЭДС равна разности потенциалов окислителя и восстановителя Еэ = jок-ль - jв-ль , то коррозия возможна при условии, что потенциал окислителя больше потенциала металла: 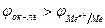 . На данной диаграмме выделяются три области.
. На данной диаграмме выделяются три области.
Область 1: если  <
< 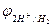 ;
; 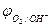 , то возможна коррозия металла с кислородной и водородной деполяризацией. К таким металлам относятся щелочные и щелочноземельные металлы, алюминий, цинк и др.
, то возможна коррозия металла с кислородной и водородной деполяризацией. К таким металлам относятся щелочные и щелочноземельные металлы, алюминий, цинк и др.
Область 2: если 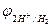 <
< 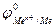 <
< 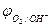 , то возможна коррозия металла с кислородной деполяризацией и невозможна с водородной деполяризацией. Потенциалы многих металлов лежат в области 2.
, то возможна коррозия металла с кислородной деполяризацией и невозможна с водородной деполяризацией. Потенциалы многих металлов лежат в области 2.
Область 3: если 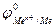 >
> 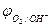 , то коррозия металла невозможна, исключая случаи наличия других деполяризаторов. Потенциалы золота, платины, например, в отсутствие комплексообразователя во всей области рН больше потенциала кислородного электрода, поэтому золото и платина корродировать с поглощением О2 и выделением Н2 не могут.
, то коррозия металла невозможна, исключая случаи наличия других деполяризаторов. Потенциалы золота, платины, например, в отсутствие комплексообразователя во всей области рН больше потенциала кислородного электрода, поэтому золото и платина корродировать с поглощением О2 и выделением Н2 не могут.
Катодами в коррозионных элементах, как правило, являются:
1. Включения металлов, имеющих больший электродный потенциал.
2. Токопроводящие неметаллические примеси (углерод, нитриды карбиды, оксиды). Например, чугун легко ржавеет во влажном воздухе из-за примеси углерода.
3. Хорошо окисленные участки металла при неодинаковой аэрации.
Коррозия возможна при неодинаковом доступе воздуха (аэрации) к различным частям металла. Наиболее окисленный участок металла является электрохимически более пассивным (электродный потенциал такого участка больше электродного потенциала неокисленного металла). Возникновением короткозамкнутых гальванических элементов вследствие неодинакового доступа кислорода воздуха можно объяснить ржавление железа, сложенного в пачки, внутри пачек; по этой же причине наблюдается ржавление проволочных тросов изнутри, а не снаружи.
4. Недеформированные, необработанные механически участки металла.
При обточке, сверлении, штамповке и других видах механической обработки затраченная энергия частично превращается в тепловую, а частично идёт на увеличение поверхностной энергии обработанного участка (явление наклёпа). В результате обработанная часть детали по сравнению с необработанной обладает повышенным запасом энергии и большей химической активностью и поэтому служит анодом. В присутствии электролита деформированный участок разрушается, катодный процесс восстановления окислителя происходит на поверхности необработанной части детали.
Практическими примерами разрушения металла в результате неодинаковой механической обработки являются ржавление кровельного железа на крыше в местах стыка, где листы подвергались ударам и изгибу, коррозия металлических деталей в местах сверлений.
В реальных условиях в химической устойчивости механических конструкций большую роль играют свойства поверхностных оксидных слоёв, приводящих к пассивации металла.
Пассивность металлов. Пассивностью металла называют состояние повышенной коррозионной устойчивости, вызываемое торможением анодного процесса в результате образования на поверхности металла защитных плёнок. Продукт окисления (коррозии) создает на поверхности металла плёнку, которая в дальнейшем влияет на процесс коррозии. Например, на поверхности алюминия образуется сплошная, хорошо сцепленная с металлом оксидная плёнка Al2O3, которая защищает его от дальнейшего окисления. Подобные защитные пленки имеются у хрома, цинка, титана и других металлов, что позволяет использовать их в качестве распространённых конструкционных материалов.
У других металлов, например у железа, в условиях контакта с воздухом и влагой образуется пористая, рыхлая, плохо сцепленная с металлом поверхностная плёнка ржавчины, не способная защитить металл от последующего окислительно-восстановительного взаимодействия с окружающей средой. Ржавчина образуется в ходе превращений:
Fe(OH)2 ® Fe(OH)3 ® nFe2O3 + mFeO +qH2O.
Таким образом, ржавчина – сложные гидратированные оксиды железа. Однако железо можно запассивировать с помощью обработки его концентрированной азотной кислотой:
2Fe + 6HNO3 = Fe2O3 + 6NO2 + 3H2O.
хол. конц.
При этом образуется плотный, предотвращающий дальнейшее разрушение поверхностный оксидный слой. Защиту железа обеспечивает также тонкий плотный слой ортофосфата железа, не растворимый в воде. Фосфатирование сталей и чугуна осуществляется в специальных растворах.
Рассмотрим примеры возникновения и работы короткозамкнутых гальванических элементов в результате контакта двух металлов.
Пример 1.Железо с медью находятся в контакте. Какой металл будет корродировать в растворе хлорида натрия?
Решение. На любом металле, находящемся в электролите, за счёт процессов обмена возникает электродный потенциал, величина которого отражает физико – химическую природу этого элемента и электролита. Чем активнее металл, тем отрицательнее его электродный потенциал. В большинстве случаев состав электролита и внешние условия отличаются от стандартных, поэтому возникающие потенциалы не будут стандартными. В данном случае нас интересуют лишь их относительные величины: какой из двух контактирующих металлов электроотрицательнее, какой – положительнее. Для получения ответа на этот вопрос можно пользоваться таблицей стандартных электродных потенциалов, помня, что потенциалы в этих случаях отличаются от стандартных:
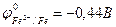 ;
; 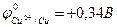 .
.
При контакте двух металлов, имеющих различные потенциалы, пойдёт локальный электрический ток – перемещение электронов от железа к меди (рис. 10.9). Несмотря на ушедшие к медному электроду электроны, потенциал железного электрода восстановит свою первоначальную величину за счёт процесса окисления, т.е. железо будет разрушаться с переходом ионовFe2+ из металлической решетки в электролит. Электроны, поступившие к меди, казалось бы должны изменить имеющийся у меди потенциал, но этот потенциал будет поддерживаться, т.к. поступившие к меди электроны израсходуются в ходе процесса, потребляющего электроны (процесса восстановления).
 Какой именно процесс восстановления будет протекать на меди - зависит от состава электролита. В нейтральном водном растворе NaCl, контактирующем с воздухом, энергетически выгодным будет процесс восстановления кислорода, растворённого в воде. Рис. 10.8 подтверждает термодинамическую возможность коррозии железа с кислородной деполяризацией:
Какой именно процесс восстановления будет протекать на меди - зависит от состава электролита. В нейтральном водном растворе NaCl, контактирующем с воздухом, энергетически выгодным будет процесс восстановления кислорода, растворённого в воде. Рис. 10.8 подтверждает термодинамическую возможность коррозии железа с кислородной деполяризацией: 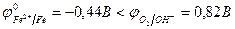 .
.
Схема работы коррозионного элемента для данного случая имеет вид
(-) Fe | водный раствор NaCl | Cu (+)
 A: Fe – 2eˉ = Fe2+ 2
A: Fe – 2eˉ = Fe2+ 2
K: O2 + 2H2O + 4eˉ = 4OH- 1
 2Fe + O2 + 2H2O = 2 Fe2+ + 4OH- = 2 Fe(OH)2$
2Fe + O2 + 2H2O = 2 Fe2+ + 4OH- = 2 Fe(OH)2$
Ответ: корродирует железо с кислородной деполяризацией; первичные продукты коррозии – Fe2+ и OH  ; вторичный продукт коррозии – Fe(OH)2.
; вторичный продукт коррозии – Fe(OH)2.
Образующийся гидроксид железа (II) подвергается дальнейшему окислению: 4Fe(OH)2  + O2 + 2H2O = 4 Fe(OH)3
+ O2 + 2H2O = 4 Fe(OH)3  .
.
Аналогичные электродные процессы будут протекать при коррозии железа во влажном воздухе.
Пример 2. Цинк с медью находятся в контакте. Какой металл будет корродировать в деаэрированном растворе хлорида натрия?
Решение.
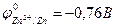 ;
; 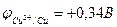
(-) Zn | деаэрированный раствор NaCl | Cu (+).
В растворе отсутствует окислитель О2, поэтому здесь можно ожидать коррозию цинка с водородной деполяризацией. Термодинамически этот процесс возможен (см. рис. 10.8), т.к. 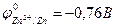 <
< 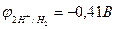 .
.
 A: Zn – 2eˉ = Zn2+
A: Zn – 2eˉ = Zn2+
K: 2H2O + 2eˉ = H2 + 2OH-
 Zn + 2H2O = Zn2+ + H2 + 2OH- = H2 + Zn(OH)2¯.
Zn + 2H2O = Zn2+ + H2 + 2OH- = H2 + Zn(OH)2¯.
Ответ: корродирует цинк с водородной деполяризацией. Первичные продукты коррозии – Н2, Zn2+ и OH 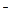 ; вторичный продукт коррозии – Zn(OH)2.
; вторичный продукт коррозии – Zn(OH)2.
Пример 3. Марганец содержит примесь меди. Какой металл будет корродировать в растворе соляной кислоты (pH=2)?
Решение:


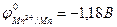 ;
; 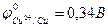
(-) Mn раствор HCl Cu(+)
pH=2
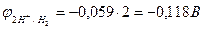 ; т.к.
; т.к. 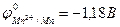 <
<  ,
,
то термодинамически возможна коррозия марганца с водородной деполяризацией (см. рис. 10.8).
A: Mn – 2eˉ = Mn2+
K: 2H+ + 2eˉ = H2
Mn + 2H+ = Mn2+ + H2
или
Mn + 2HCl = MnCl2 + H2
Ответ: происходит коррозия марганца с водородной деполяризацией, продукты коррозии – Mn2+ и Н2.
Если в условии задачи неизвестна концентрация кислоты, водородный показатель рН, то решение выполняется для рН=0.
| <== предыдущая страница | | | следующая страница ==> |
| Электролиз | | | Защита металлов от коррозии |
Дата добавления: 2014-09-29; просмотров: 1042; Нарушение авторских прав

Мы поможем в написании ваших работ!