
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Присоединение галогенов (галогенирование)
|
Читайте также: |
Неотложная помощь.
Клиническая діагностика.
Крапивница.
Неотложная помощь.
1. Немедленно прекратить поступление аллергена
.Назначить сорбенты(Энтеросгель, полифепан,полисорб в возр. дозах
2. Ввести антигистаминные препараты в/м или в/в:
- 2,5% р-р пипольфена 0,1- 0,15мл/год жизни или
- 2% р-р супрастина ОД* 0,15мл/год жизни.
3. Ввести 3% р-р преднизалона в дозе 1-2 мг/кг в/м или в/в.
4. По показаниям при нарастающем отеке гортани с обтурационной дыхательной
недостаточностью проведение интубации или трахеостомии.
5. Госпитализация в соматическое отделение.
Крапивница - аллергическая реакция немедленного типа, характеризующаяся быстрым появлением уртикарных высыпаний на коже и реже на слизистых оболочках.
Причины возникновения крапивницы те же, что и при отеке Квинке. У ребенка появляются ощущение жара, кожный зуд, изменения кожи, как «после ожога крапивой». Элементы крапивницы - волдыри и папулы - могут иметь разнообразную форму и величину, нередко с их слиянием и образованием гигантских элементов. Цвет элементов крапивницы от бледно - розового до красного. Высыпания локализуются на любых участках тела и слизистых оболочках, чаще на животе, спине, груди, бедрах. Могут быть общие симптомы: лихорадка, возбуждение, артралгии, коллапс.
1. Немедленно прекратить поступление аллергена.
2. Ввести антигистаминные препараты внутрь (кларитин, кестин, зиртек, телфаст) или в/м (см. отек квинке).
3. При распространенной или гигантской крапивнице с лихорадкой ввести 3% р-р преднизалона 1-2 мг/кг в/м или в/в.
4. Повести энтеросорбцию активированным углем в дозе 1г/кг в сут.
Госпитализация в соматическое отделение показана при отсутствии эффекта от проводимой терапии. Также подлежат госпитализации больные, которым на догоспитальном этапе в связи с тяжестью состояния вводился преднизалон.
При действии на этиленовые углеводороды галогенов в результате присоединения их по месту двойной связи образуются дигалогенпроизводные предельных углеводородов с атомами галогена при соседних углеродных атомах. Например:
СН2 СН2—Cl
II + Cl2 ¾® ½
CH2 CH2—Cl
этилен 1,2-дихлорэтан
СН2=СН—СН3 + Br2 ¾® CH2—CH—CH3
пропилен ½ ½
Br Br 1.2-дибромпропан
Б) реакции отщепления (элиминирования)
(R—CHBr—CH2—R' + KOH ® R—CH = CH—R' +KBr + H2O)
Отщепление воды от спиртов (реакция дегидратации)
При действии на одноатомные спирты различных водоотнимающих средств происходит отщепление молекулы воды. При этом атом водорода отщепляется от углеродного атома, соседнего с тем, при котором находится гидроксильная группа спирта, что приводит к образованию непредельного углеводорода:
СН2—Н СН2
½ ¾® II +Н2О
СН2—ОН Н2SO4 CH2
этанол этилен
В этой реакции также проявляется правило Зайцева, если есть выбор, водород отщепляется преимущественно от того, который содержит меньшее число атомов водорода.
В) реакции замещения (RH + Cl2 ® RCl + HCl)
Взаимодействие алканов с галогенами
Взаимодействие насыщенных углеводородов с хлором или бромом ускоряется при нагревании и, особенно, при действии света. И атомы галогена постепенно замещают в углеродных молекулах атомы водорода. При этом образуются смеси галогенпроизводных углеводородов; реакция сопровождается выделением галогенводорода. Например, при действии хлора на метан происходит постепенное замещение всех атомов водорода и образуется смесь хлорпроизводных:
СН4 + Сl2 ® СН3Cl + HCl
свет хлористый метил
СН3Cl + Cl2 ® CH2Cl2 + HCl
свет дихлорметан
CH2Cl2 + CL2 ® CHCl3 + HCl
свет трихлорметан
(хлороформ)
СНCl3 + Cl2 ® CCl4 + HCl
свет тетрахлорметан
(четыреххлористый углерод)
Г) реакции изомеризации (CH3—CH2—CH2—CH3 ® CH3—CH—CH3
ï
По механизму протекания: CH3
А) Гетеролитические (полярные и ионные) реакции
Нуклеофильные реакции (R :Cl+ :OH- ® R: OH + :Cl-)
Реакции присоединения по карбонильной группе
Присоединение большинства реагентов по двойной связи С=О происходит как ионная реакция по механизму нуклеофильного присоединения AN (от англ. nucleophile addition).
1. Присоединение циановодородной (синильной) кислоты HCN:
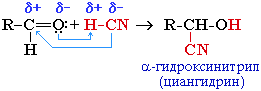
Эта реакция используется для удлинения углеродной цепи, а также для получения α-гидроксикислот R-CH(COOH)OH
Электрофильные реакции
Электрофильной называется реакция, в которой молекула органического вещества подвергается действию электрофильного реагента. Электрофильные ("любящие электроны") реагенты или электрофилы - это частицы (катионы или молекулы), имеющие свободную орбиталь на внешнем электронном уровне.
Примеры NO2+, ZnCl2, AlCl3 электрофильных частиц:
H+, CH3+ и другие карбокатионы, . Незаполненность внешнего электронного уровня в электрофиле показана на примере AlCl3.
Электрофильноеприсоединение:
CH2=CH2 + HCl 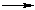 CH3CH2Cl (электрофил - H+ в составе HCl)
CH3CH2Cl (электрофил - H+ в составе HCl)
Стадии:
I. CH2=CH2 + Hδ+Clδ- 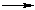 CH3CH2+ + Cl (медленная)
CH3CH2+ + Cl (медленная)
II. CH3CH2+ + Cl 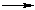 CH3CH2Cl (быстрая)
CH3CH2Cl (быстрая)
Электрофильноезамещение:
C6H6 + NO2+  C6H5NO2 + H+ (электрофил - NO2+)
C6H5NO2 + H+ (электрофил - NO2+)
Катион NO2+ образуется в смеси конц. кислот HNO3 и H2SO4.
Обозначение механизма - SE (S – substitution [замещение]).
Электрофильные реакции ( R—NH2 + H+ ® R—NH3+)
СН2=СН—СН3 + Br2 ¾® CH2—CH—CH3
пропилен ½ ½
Br Br 1.2-дибромпропан
Б) Гомолитические (радикальные) реакции
Сl : Cl + hn ® 2Cl×
CH4 + Cl× ® ×CH3 + HCl
×CH3 + Cl2 ® CH3Cl + Cl×
3) По количеству молекул, участвующих в элементарной стадии, протекаю-
щей с наименьшей скоростью:
Мономолеклярные,
Бимолекулярные и т.д.
Эти классы реакций неразрывно связаны между собой, ибо реакции присоединения могут протекать по электрофильному, нуклеофильном или радикальному механизму, а реакции нуклеофильного замещения при насыщенном атоме углерода могут осуществляться посредством мономолекулярного, либо бимолекулярного механизма.
| <== предыдущая страница | | | следующая страница ==> |
| | | Вопрос 1. Древнегреческая философия: периодизация и основные черты |
Дата добавления: 2014-02-26; просмотров: 687; Нарушение авторских прав

Мы поможем в написании ваших работ!