
Вопрос 6
Date: 2015-10-07; view: 626.
Основные положения квантовой механики, на которых базируется современная теория строения атома: квантовый характер излучения и корпускулярно – волновой характер электрона (уравнения М. Планка и де Бойля), принцип неопределённости Гейзенберга, следствие из него. Понятие об электронной орбитали (электронном облаке).
Вопрос 5
Основные соли - продукты неполного замещения гидроксогрупп основания (OH-) кислотными остатками ((CuOH)2CO3). Они образуются в условиях избытка основания или недостатка кислоты.
Основные соли образуются только из многокислотных оснований. Одноокислотные основания таких солей образовать не могут.
Аналогично, для образования названий основных солей используются приставки гидроксо- ((FeOH)NO3 — гидроксонитрат железа(II)) Cu2(OH)2CO3 - Дигидроксокарбонат меди(II)
Средние соли – это продукты полного замещения водорода в кислоте на атомы металла или гидроксогруппы ОН- в основании на кислотный остаток.
Примеры (Na2CO3 - карбонат натрия ; PbSO4 – сульфат свинца ; FeS – сульфид железа (II) ; Ca(NO3)2 - нитрат кальция
Квантовый характер излучения а поглощения энергии. Примерно в начале XX в. исследования ряда явлений (излучений раскаленных тел, фотоэффект, атомные спектры) привели к выводу, что энергия распространяется и передается, поглощается и испускается не непрерывно, а дискретно, отдельными порциями — квантами. Энергия системы микрочастиц также может принимать только определенные значения, которые являются кратными числами квантов.
Предположение о квантовой энергии впервые было высказано М. Планком (1900) и позже обосновано А. Эйнштейном (1905). Энергия кванта E зависит от частоты излучения v:
E = hv ; где h – постоянная Планка
Корпускуля́рно-волново́й дуали́зм (или Ква́нтово-волново́й дуали́зм) — принцип, согласно которому любой объект может проявлять как волновые, так и корпускулярные свойства. Был введён при разработке квантовой механики для интерпретации явлений, наблюдаемых в микромире, с точки зрения классических концепций. Дальнейшим развитием принципа корпускулярно-волнового дуализма стала концепция квантованных полей в квантовой теории поля. Французский ученый Луи де Бройль (1892—1987), осознавая существующую в природе симметрию и развивая представления о двойственной корпускулярно-волновой природе света, выдвинул в 1923 году гипотезу об универсальности корпускулярно-волнового дуализма. Он утверждал, что не только фотоны, но и электроны и любые другие частицы материи наряду с корпускулярными обладают также волновыми свойствами.

Формула де Бройля устанавливает зависимость длины волны  , связанной с движущейся частицей вещества, от импульса
, связанной с движущейся частицей вещества, от импульса  частицы:
частицы:
Принцип неопределенности Гейзенберга (1927 г.): невозможно утверждать, что e, имеющий определенную скорость, находится в той или иной точке пространства. Вероятность нахождения электрона в определенной области пространства описывается волновой функцией , которая характеризует амплитуду волны, как функцию координат электрона. В наиболее простом случае эта функция зависит от трех пространственных координат и называется орбиталью.
Следствие: Взаимодополнительные величины (например, энергия и время, потенциальная и кмнетическая энергия и т.д.) определить одновременно принципиально невозможно
Электронная орбиталь - пространство около ядра, в котором можно обнаружить электрон. За пределами этого пространства вероятность встретить электрон достаточно мала (менее 5%).
Уравнение Шредингера, особенности его решения.ψ – функция общего вида для атома водорода, физический смысл квадрата пси - функции ψ2 , квантовые числа.
Уравне́ние Шрёдингера — уравнение, описывающее изменение в пространстве (в общем случае, в конфигурационном пространстве) и во времени чистого состояния, задаваемого волновой функцией, в гамильтоновых квантовых системах. Играет в квантовой механике такую же важную роль, как уравнение второго закона Ньютона в классической механике. Установлено Эрвином Шрёдингером в 1926 году.
Особенности решения в трехмерном случае:
В трёхмерном случае пси-функция является функцией трёх координат и  в декартовой системе координат заменяется выражением
в декартовой системе координат заменяется выражением

тогда уравнение Шрёдингера примет вид:

Общий вид:

ψ – функция общего вида для атома водорода
Рассмотрим сейчас решение уравнения Шрёдингера для атома водорода. Так как потенциальная функция электрона в атоме водорода имеет вид  где e — заряд электрона (и протона), r — радиус-вектор, то уравнение Шрёдингера запишется следующим образом:
где e — заряд электрона (и протона), r — радиус-вектор, то уравнение Шрёдингера запишется следующим образом:

Здесь ψ — волновая функция электрона в системе отсчёта протона, m — масса электрона, 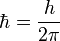 — постоянная Планка, E — полная энергия электрона,
— постоянная Планка, E — полная энергия электрона, 
Так как потенциальная функция зависит от r, а не от координат по отдельности, удобно будет записать лапласиан в сферической системе координат  В ней он выглядит следующим образом:
В ней он выглядит следующим образом:

физический смысл квадрата пси - функции ψ2
В координатном представлении волновая функция  зависит от координат (или обобщённых координат) системы. Физический смысл приписывается квадрату её модуля
зависит от координат (или обобщённых координат) системы. Физический смысл приписывается квадрату её модуля  , который интерпретируется как плотность вероятности
, который интерпретируется как плотность вероятности  (для дискретных спектров — просто вероятность) обнаружить систему в положении, описываемом координатами
(для дискретных спектров — просто вероятность) обнаружить систему в положении, описываемом координатами  в момент времени
в момент времени  :
:
 .
.
Состояние каждого электрона в атоме обычно описывают с помощью четырех квантовых чисел: главного (n), орбитального (l), магнитного (m) и спинового (s). Первые три характеризуют движение электрона в пространстве, а четвертое - вокруг собственной оси.
Главное квантовое число (n). Определяет энергетический уровень электрона, удаленность уровня от ядра, размер электронного облака. Принимает целые значения (n = 1, 2, 3 ...) и соответствует номеру периода. Из периодической системы для любого элемента по номеру периода можно определить число энергетических уровней атома и какой энергетический уровень является внешним.
Орбитальное квантовое число (l) характеризует геометрическую форму орбитали. Принимает значение целых чисел от 0 до (n - 1). Независимо от номера энергетического уровня, каждому значению орбитального квантового числа соответствует орбиталь особой формы. Набор орбиталей с одинаковыми значениями n называется энергетическим уровнем, c одинаковыми n и l - подуровнем.
Магнитное квантовое число (m) характеризует положение электронной орбитали в пространстве и принимает целочисленные значения от -I до +I, включая 0. Это означает, что для каждой формы орбитали существует (2l + 1) энергетически равноценных ориентации в пространстве.
Спиновое квантовое число (s) характеризует магнитный момент, возникающий при вращении электрона вокруг своей оси. Принимает только два значения +1/2 и -1/2 соответствующие противоположным направлениям вращения.