
Геометрическая изомерия
Date: 2015-10-07; view: 770.
Оптическая изомерия
Пространственная изомерия (стереоизомерия)
Изомерия положения Пример: 2-хлорбутановая кислота и 4- хлорбутановая кислота
Изомерия функциональной группы (межклассовая изомерия)
Структурная изомерия
1 Изомерия углеродной цепи (углеродного скелета)
4 Метамерия Пример: CH3CH2OCH2CH3 — диэтиловый эфир и CH3OCH2CH2CH3 — метилпропиловый эфир
5 Валентная —изомеры можно перевести друг в друга за счёт перераспределения связей. бензол бицикло[2.2.0]гекса-2,5-диен («бензол Дьюара»), призман ( «бензол Ладенбурга»), бензвален (VIII).
1 Заторможенная конформация
2 Заслоненная конформация
Проекция Ньюмана — Передний атом углерода называют ближайшим и представлен точкой, а задний атом углерода называют отдалённым от центра и представлен кругом.

Энантиомеры — пара стереоизомеров, представляющих собой зеркальные отражения друг друга, не совмещаемые в пространстве[1]. Классической иллюстрацией двух энантиомеров могут служить ладони, имеющие одинаковую структуру, но различную пространственную ориентацию.
Существование энантиомерных форм связано с наличием у молекулы хиральности — свойства не совпадать в пространстве со своим зеркальным отражением.
В ахиральной (симметричной) среде энантиомеры имеют одинаковые химические и физические свойства, кроме способности вращать плоскость поляризацииплоскополяризованного света на одинаковую величину угла, но в противоположных направлениях. Данное свойство энантиомеров получило название оптической активности.
Рацемат — эквимолярная смесь двух энантиомеров. Рацематы отличаются по свойствам от индивидуальных энантиомеров. Являются продуктами нестереоселективных реакций.
R,S - Вид номенклатуры основывается на присвоении хиральному атому углерода обозначения R или S на основании взаимного расположения четырёх связанных с ним заместителей. Для каждого из заместителей определяют старшинство в соответствии с правилами Кана — Ингольда — Прелога (Атом с большим атомным номером старше атома с меньшим атомным номером.), затем молекулу ориентируют так, чтобы младший заместитель был направлен в сторону от наблюдателя. Если старшинство уменьшается по часовой стрелке, то конфигурацию атома углерода обозначают R (лат. rectus — правый). В противоположном случае конфигурацию обозначают S (лат. sinister — левый).
При наличии в молекуле не одного, а нескольких хиральных центров направление вращения определяется суммарным эффектом при каждом из них. В молекуле с двумя асимметрическими центрами, имеющими одинаковые заместители, но различными по их взаимному расположению, оптическая активность как бы теряется. Оптический изомер с такого рода "вырожденной" активностью называется мезо-формой. Причиной того, что в растворе оптически активного соединения не наблюдается оптической активности, может быть также и одновременное присутствие в нем равных количеств право- и левовращающего изомера. Такая смесь называется рацемической.
Диастереомеры — стереоизомеры, не являющиеся зеркальными отражениями друг друга. Диастереомерия возникает, когда соединение имеет несколько стереоцентров. Если два стереоизомера имеют противоположные конфигурации всех соответствующих стереоцентров, то они являются энантиомерами. Однако, если конфигурация различается лишь у некоторых (а не у всех) стереоцентров, то такие стереизомеры являются диастереомерами. Если диастереомеры отличаются конфигурацией лишь одного стереоцентра, то они называются эпимерами.
Названия эритро- и трео- происходят от названий углеводов эритрозы и треозы. Эти названия употребляют для указания взаимного положения заместителей у соединений с двумя асимметрическими атомами: эритро-изомерами называют те, у которых два одинаковых боковых заместителя стоят в стандартной проекционной формуле на одной стороне (справа или слева); трео-изомеры имеют одинаковые боковые заместители на разных сторонах проекционной формулы

Отсутствие свободного вращения вокруг связей С-С в цикле создает предпосылки для существования пространственных изомеров у некоторых замещенных циклоалканов. Например, в молекуле 1,2-диметилциклопропана две группы СН3 могут находиться по одну сторону от плоскости цикла (цис-изомер) или по разные стороны (транс-изомер).
Чтобы построить название изомера в Z-E номенклатуре, необходимо определить старшинство заместителей по атомному номеру у атомов углерода при двойной связи (или у атомов углерода в цикле). Если старшие заместители у атомов углерода при двойной связи (или у атомов углерода в цикле) расположены с одной стороны от плоскости -связи (или плоскости цикла), это Z-изомер, если по разные - Е-изомер.
Электронными эффектами называют смещение электронной плотности в молекуле под влиянием заместителей.
Смещение электронной плотности по цепи s-связей называется индуктивным эффектом и обозначается I.
Электроноакцепторные заместители, т.е. атом или группа атомов, смещающие электронную плотность s-связи от атома углерода к себе, проявляют отрицательный индуктивный эффект (-I-эффект).
+I-эффект проявляют алифатические углеводородные радикалы, т.е. алкильные радикалы (метил, этил и т.д.). Большинство функциональных групп проявляют -I-эффект: галогены, аминогруппа, гидроксильная, карбонильная, карбоксильная группы.
Влияние заместителя на распределение электронной плотности, передаваемое по p-связям, называют мезомерным эффектом (М). Мезомерный эффект также может быть отрицательным и положительным. В структурных формулах его изображают изогнутой стрелкой, начинающейся у центра электронной плотности и завершающейся в том месте, куда смещается электронная плотность.
Наличие электронных эффектов ведет к перераспределению электронной плотности в молекуле и появлению частичных зарядов на отдельных атомах. Это определяет реакционную способность молекулы.
По размеру цикла различают малые циклы (С3-С4), обычные циклы (С5-С7), средние циклы (С8-С11), макроциклы (С13 и более).
По числу циклов в молекуле различают моно- и полициклические соединения.
Для циклоалканов характерны следующие виды напряжений:
Торсионное (Пи гцеровское) напряжение — связано со взаимодействием химических связей в заслоненной или частично заслоненной конформациях;
Напряжение Ван-дер-Ваальса — обусловлено взаимным отталкиванием заместителей при сближении на расстояние, близкое сумме их вандерваальсовых радиусов;
Угловое (Байеровское) напряжение — присуще отдельным циклоалканам и связано с отклонением валентных углов между углерод-углеродными связями в цикле от нормального (тетраэдрического) значения.
По химическим свойствам малые и обычные циклы существенно различаются между собой. Циклопропан и Циклобутан склонны к реакциям присоединения, то есть сходны в этом отношении с алкенами. Циклопентан и Циклогексан по своему химическому поведению близки к алканам, так как вступают в реакции замещения.
1. Циклопропан и циклобутан способны присоединять бром:
С3H6 + Br2 → BrCH2—CH2—CH2Br
2. Циклопропан, циклобутан и циклопентан могут присоединять водород, давая соответствующие нормальные алканы. Присоединение происходит при нагревании в присутствии никелевого катализатора:
С4H8 + H2 → CH3—CH2—CH2—CH3
Вследствие взаимного отталкивания электронных облаков углерод-углеродных связей максимальная электронная плотность перекрывающихся орбиталей атомов углерода в молекуле циклопропана расположена не по прямой, соединяющей центры связываемых атомов, а за пределами треугольника молекулы.
Образующиеся связи называют «банановыми» или т-(греч. «тау») связями.
 8
8
Инициирование цепного процесса:

Развитие цепного процесса:
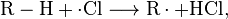


Образовавшиеся сульфонилхлориды широко применяются в производстве ПАВ.





Реакция катализируется перекисями,
Считается, что данный эффект характерен исключительно для бромоводорода HBr и не наблюдается в случае других галогеноводородов (HF, HCl и HI) за счёт того, что молекулы HF и HCl слишком прочны для гомолитического разрыва, а молекула HI хотя и имеет более низкую энергию связи, но образующийся атом йода недостаточно реакционноспособен и не может развить цепную реакцию.
Реакции радикального присоединения галогеноводородов к алкенам протекают как анти-присоединение, что объясняется образованием циклического бромониевого радикала, раскрытие которого происходит «с тыла». При повыщении температуры селективность снижается, поскольку становится возможным вращение С-С-связи в промежуточном алкильном радикале. Для циклоалканов, в молекулах которых такое вращение невозможно, наблюдается образование только транс-продуктов. 
Направление радикального галогенирования NBS или хлорсукцинимидом определяется относительной стабильностью радикала, образующегося в качестве интермедиата. Радикальное галогенирование алкенов в аллильное положение обусловлено более низкой энергией С-Н-связи в аллильном положении по сравнению с энергией других C-H-связей.





NBS селективно бромирует и циклические алкены только по аллильному атому углерода:




В зависимости от взаимного расположения двойных связей, диены подразделяются на три группы:
· сопряженные диены, в которых двойные связи разделены одинарной (1,3-диены)
· аллены с кумулированными двойными связями (1,2-диены)
· диены с изолированными двойными связями, в которых двойные связи разделены несколькими одинарными.
Гетероаналоги диенов, в которых один из ненасыщенных углеродных атомов замещёнгетероатомом, называются гетеродиенами[1].
Обычно к диенам относят ациклические и циклические 1,3-диены, образующиегомологические ряды общих формул  и
и  соответственно, ациклические диены являются структурными изомерами алкинов.
соответственно, ациклические диены являются структурными изомерами алкинов.

Центральный sp-гибридизованный атом углерода в алленах является электрофильным центром, поэтому, в отличие от не активированных электронакцепторными заместителями алкенов, аллены реагируют с мягкими нуклеофилами, образуя винильные и аллильные производные:
CH2=C=CH2 + PhSH  CH2=C(SPh)-CH3 + CH2=CH-CH2SPh
CH2=C(SPh)-CH3 + CH2=CH-CH2SPh
Электрофильность sp-гибридизованного атома алленов повышается электроноакцепторными группами, в этом случае присоединение нуклеофила идет исключительно по этому атому:
CH2=C=CHCOOR + NuH  CH2=CNuCH2COOR + CH3C(Nu)=CHCOOR
CH2=CNuCH2COOR + CH3C(Nu)=CHCOOR
| <== previous lecture | | | next lecture ==> |
| I.Запомните (вспомните) формы следующих нестандартных глаголов | | | Реакции 1,3-диенов |