
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Реакции нуклеофильного замещения
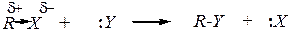
Нуклеофильными частицы:
HО-, RO-, -NH2, F-, Cl-, Br-, I-, CN-, H-, -CH2-R
H2O, ROH, NH3, RNH2, RR¢NH, H2S, RSH
Механизм бимолекулярного нуклеофильного замещения
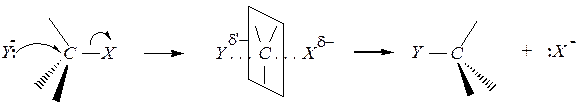
Механизм мономолекулярного замещения
1) 
2) 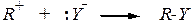
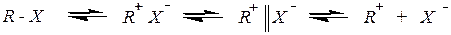
I II III IV V,
где II — тесная ионная пара
III — рыхлая ионная пара
IV и V — диссоциированные ионы
Факторы, влияющие на механизм и скорость нуклеофильного замещения
1. Влияние структуры субстрата.
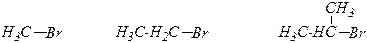
бромметан бромэтан 2-бромпропан
Скорость SN2-реакции:
18000 145 1
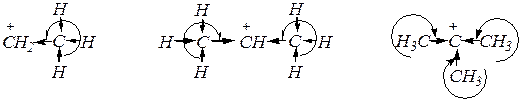 ,
,
Поэтому высокая скорость реакций нуклеофильного замещения может быть характерна и для первичных, и для третичных алкилгалогенидов.
В первом случае — за счёт лёгкости взаимодействия по SN2-механизму (свободный доступ реакционного центра, нет стерических препятствий),
во втором — по SN1-механизму (лёгкость диссоциации субстратов, стабильность образующегося карбокатиона).
Вторичные алкилгалогениды в большинстве случаев должны реагировать по смешанному механизму, причём скорость реакций у них будет относительно небольшой, так как есть препятствия для протекания и мономолекулярного, и бимолекулярного замещения.
2. Влияние природы нуклеофила.
Скорости мономолекулярных реакций не зависят от природы нуклеофила, так как он не принимает участия в лимитирующей стадии.
Активность наиболее распространённых нуклеофилов уменьшается в ряду (для SN2-реакций в протонных растворителях):
RS->C2H5S->I->CN->HO->Br->C2H5O->Cl->CH3COO->H2O
3. Влияние растворителей и катализаторов.
В качестве катализаторов в реакциях нуклеофильного замещения используются кислоты, в том числе кислоты Льюиса, то есть галогениды бора, алюминия, железа, цинка, кадмия, ртути, меди и другие. Эти вещества способны акцептировать анионы из раствора за счёт валентных орбиталей металла, и их применение может лишь замедлить процесс бимолекулярного замещения, но способствует протеканию SN1-процесса, так как облегчает диссоциацию субстрата, при этом катализатор не взаимодействует с образующимися карбокатионами субстрата.
4. Влияние природы уходящей группы.
При отрыве галогенид-ионов стабильность этих анионов уменьшается в ряду I->Br->Cl->F-. Однако этот порядок соблюдается в апротонной среде. Напротив, в протонных растворителях или в присутствии кислотных катализаторов легче всего отщепляются анионы слабых кислот, поэтому порядок отщепления будет обратный (HF самая слабая кислота из всех галогеноводоводных кислот).
| <== предыдущая страница | | | следующая страница ==> |
| | | Большинство мономолекулярных реакций протекает в кислой среде |
Дата добавления: 2015-07-26; просмотров: 248; Нарушение авторских прав

Мы поможем в написании ваших работ!