
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Большинство мономолекулярных реакций протекает в кислой среде
Факторы, способствующие протеканию SN1-реакции:
1) образование стабильного карбокатиона,
2) применение высокополярного протонного растворителя и кислотных катализаторов,
3) стабильность уходящей группы.
Нуклеофильность атакующей частицы существенного значения не имеет.
Факторы, способствующие протеканию SN2-реакции:
1) доступность электрофильного центра субстрата,
2) применение апротонного растворителя,
3) высокая нуклеофильность реагента.
Природа уходящей группы существенного значения не имеет.
Примеры реакций нуклеофильного замещения
1) Гидролиз галогеналканов — это превращение их в спирты по схеме:
R-Х + H2O ® R-OH + HХ
Механизм реакции: SN1или SN2 — определяется, в основном, структурой субстрата, а также другими факторами. Например, щелочной гидролиз бромэтана (SN2-механизм):
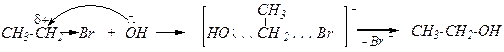
Кислотный гидролиз 2-бром-2-метилпропана (SN1-механизм):
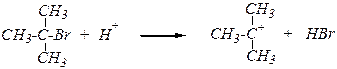
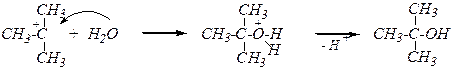
2) Алкоголиз галогеналканов — это взаимодействие галогеналканов с алкоголятами металлов (реакция Вильямсона*), приводящее к образованию простых эфиров:
R-Hal + R¢-O-Na+ ® R-O-R¢ + NaHal
Нуклеофильная частица — алкоголят-анион R¢-O-.
При этом при синтезе смешанных эфиров (с разными R и R¢) необходимо осуществить правильный выбор галогеналкана и алкоголята (RHal и R¢-O-или R¢Hal и R-O- — в зависимости от структуры углеводородных радикалов) для того, чтобы реакция протекала с наибольшей скоростью и возможность образования алкена (протекание конкурирующей реакции отщепления) была бы сведена к минимуму.
3) Аммонолиз галогеналканов — это взаимодействие галогеналканов с аммиаком, приводящее к получению аминов (или их солей) — алкилирование аминов по Гофману
R-Hal + NН3 ®[R-NН3]+Hal- 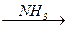 R-NН2 + NН4Hal
R-NН2 + NН4Hal
4) Замена одного атома галогена на другой. При реакции галогеналканов с галогеноводородом или с галогенид-ионом, где атом галогена отличается от субстратного по своей природе, происходит превращение одного галогеналкана в другой, например:
R-Br + I-® R-I + Br-
кислая среда и протонные растворители — замещение атома фтора
высокополярные апротонные растворители, наоборот, атома йода, так как нуклеофильность галогенид-ионов уменьшается в ряду I->Br->Cl->F-
5) Взаимодействие с цианидами — это взаимодействие галогеналканов с солями синильной кислоты, приводящее к образованию органических цианидов (нитрилов) или изоцианидов. Цианид-ион является амбидентным нуклеофилом, то есть, способен проявлять свои нуклеофильные свойства, как за счёт атома углерода, так и за счёт атома азота:
-:CºN ®:C=N: -
Механизм SN1 — приводит к образованию изоцианидов (изонитрилов):
R+ + :C=N: -® R-N=С:
Механизм SN2:
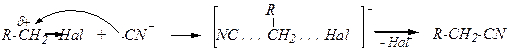
При этом образуются цианиды (нитрилы).
6) Взаимодействие с нитритами.
Нитрит-анион также является амбидентным нуклеофилом.
Поэтому его взаимодействие с галогеналканами может привести либо к нитросоединениям, либо к эфирам азотистой кислоты:
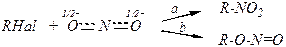
| <== предыдущая страница | | | следующая страница ==> |
| Реакции нуклеофильного замещения | | | Реакции отщепления (элиминирования) |
Дата добавления: 2015-07-26; просмотров: 293; Нарушение авторских прав

Мы поможем в написании ваших работ!