
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
VII. Процессы нитрования
|
Читайте также: |
В химии душистых веществ процессы нитрования применяются в синтезе соединений, обладающих мускусным запахом. Так, например мускус амбровый является динитропроизводным метилового эфира требутилметакрезола.
Нитрование проводят смесью азотной кислоты с уксусным ангидридом. В нитратор загружают уксусный ангидрид и при перемешивании и температуре –5…0 0С приливают в течение 1,5 ч концентрированную азотную кислоту.

Затем к нитрующей смеси при –3…–5 0С в течение 5 ч приливают предварительно приготовленный раствор метилового эфира требутилметакрезола в уксусном ангидриде.Реакционную смесь нагревают до 30 0С и перемешивают при этой температуре 0,5 ч, затем спускают в кристаллизатор с охлажденной водой и промывают до нейтральной реакции.
VIII. Процессы галоидирования
Процессы галоидирования, то есть присоединение галогеноводородов к веществам с этиленовой связью, протекают чаще всего при низких температурах самопроизвольно или в присутствии катализаторов. Практическое значение имеет, в основном, гидробромирование и гидрохлорирование ненасыщенных органических соединений.
Присоединение галогеноводородов по двойной связи может протекать «нормально» по правилу Морковникова, когда водород присоединяется к наиболее гидрогенизированному атому углерода. «Нормальное» присоединение ускоряется в присутствии полярных растворителей, таких, как вода, сильные кислоты, и катализаторов — галогенидов металлов (TiCl4, SnCl4, A1C13, FeC13, CuCl и другие). Примером является процесс гидрохлорирования изопрена газообразным хлористым водородом. Полученный первичный гидрохлорид изопрена без очистки используют на следующей стадии в синтезе цитраля.
Под влиянием небольших количеств кислорода, перекисей или фотохимически может происходить «аномальное» присоединение галогеноводорода. Эта реакция характерна для бромистого водорода.
Примером «аномального» присоединения бромистого водорода по двойной связи является получение 11-бромундекановой кислоты — промежуточного продукта в синтезе пентадеканолида — одного из наиболее ценных душистых веществ с запахом мускуса.
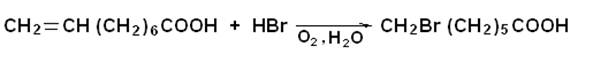
Ундециленовая кислота 11-бромундекановая кислота
Для получения 11-бромундекановой кислоты из ундециленовой кислоты и бромистого водорода необходимо присутствие в реакционной массе перекисных соединений. Однако, процесс хорошо протекает при условии интенсивного пропускания в массу влажного воздуха.
Гидробромирование ундециленовой кислоты осуществляют в колонном аппарате непрерывного действия, что дает целый ряд преимуществ по сравнению с периодическим процессом: сокращение времени реакции в 6—8 раз, уменьшение почти в 2 раза расхода брома (рис.2).
Толуольный раствор ундециленовой кислоты из мерника поступает через дозирующее устройство в колонну для гидробромирования.
Колонна непрерывного действия представляет собой систему из трех 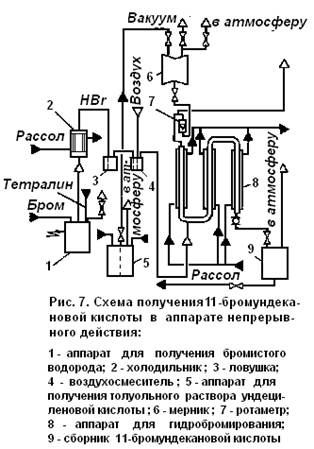 теплообменников, последовательно соединенных между собой. В рубашки теплообменников подаётся рассол для охлаждения реакционной смеси до 10—12 0С. Аппарат работает по принципу прямотока. В первый теплообменник сверху подаётся толуольный раствор ундециленовой кислоты, в нижнюю часть второго поступает бромистый водород, который предварительно в воздухосмесителе смешивается с влажным воздухом. По второму и третьему теплообменнику движется толуольный раствор ундециленовой кислоты в контакте с бромистым водородом. Движение жидкости во втором теплообменнике снизу вверх, в первом и третьем — сверху вниз. Полученный толуольный раствор 11-бромундекановой кислоты непрерывно выводится из реактора в приемник, а затем в сборник.
теплообменников, последовательно соединенных между собой. В рубашки теплообменников подаётся рассол для охлаждения реакционной смеси до 10—12 0С. Аппарат работает по принципу прямотока. В первый теплообменник сверху подаётся толуольный раствор ундециленовой кислоты, в нижнюю часть второго поступает бромистый водород, который предварительно в воздухосмесителе смешивается с влажным воздухом. По второму и третьему теплообменнику движется толуольный раствор ундециленовой кислоты в контакте с бромистым водородом. Движение жидкости во втором теплообменнике снизу вверх, в первом и третьем — сверху вниз. Полученный толуольный раствор 11-бромундекановой кислоты непрерывно выводится из реактора в приемник, а затем в сборник.
IX. Процессы конденсации
Реакции конденсации весьма разнообразны и многочисленны. Ниже рассмотрены лишь некоторые, чаще всего используемые в технологии получения, как промежуточных продуктов, так и самих душистых веществ.
Характерным примером альдольно-кротоновой конденсации в синтезе душистых веществ является получения различных иононов взаимодействием синтетического цитраля с кетонами (псевдоионона, псевдометилионона, изопсевдометилионона). Иононы – душистые вещества с запахом фиалки.
Реакция взаимодействия ароматических альдегидов с алифатическими альдегидами или кетонами протекает с выделением воды в присутствии щелочей и приводит к образованию ненасыщенных альдегидов или кетонов жирноароматического ряда. По этому методу получают из бензальдегида и уксусного альдегида коричный альдегид – душистое вещество с запахом корицы.
Конденсация бензальдегида с энантолом приводит к образованию жасминальдегида. В разбавленном виде он обладает запахом жасмина.
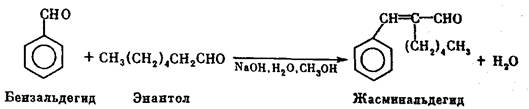
В аппарат к смеси метанола, воды, раствора гидроксида натрия и бензальдегида приливают при перемешивании в течение 5 ч энантол, поддерживая температуру 30…35 0С, затем выдерживают в этих условиях 2 ч. Реакционную смесь разбавляют водой, отделяют метанольно-щелочные воды, органический слой нейтрализуют раствором серной кислоты, промывают солевым раствором до нейтральной реакции и очищают вакуумной ректификацией.
Другим примером конденсации с выделением воды является хлорметилирование ароматических соединений. Этим методом получают кумилхлорид – исходное вещество в синтезе цикламенальдегида, триизопропилбензилхлорид – исходное вещество в синтезе триизопропилбензилового спирта с муксусным запахом.
Примером конденсации с выделением органической кислоты может служить реакция ацилирования при получении таких душистых веществ как ацетиланизол, мускус-кетон.
| <== предыдущая страница | | | следующая страница ==> |
| VI. Процессы алкилирования | | | X. Процессы изомеризации |
Дата добавления: 2014-05-19; просмотров: 988; Нарушение авторских прав

Мы поможем в написании ваших работ!