
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Влияние катализатора
Изменение скорости реакции под воздействием малых добавок особых веществ, количество которых в ходе процесса не меняется, называется катализом.
Вещества, изменяющие скорость химической реакции, называются катализаторами (вещества, изменяющие скорость химических процессов в живых организмах – ферменты). Катализатор в реакциях не расходуется и в состав конечных продуктов не входит.
Химические реакции, протекающие в присутствии катализатора, называются каталитическими. Различают положительный катализ – в присутствии катализатора скорость химической реакции возрастает - и отрицательный катализ (ингибирование) – в присутствии катализатора (ингибитора) скорость химической реакции замедляется.
Примеры:
1. Окисление сернистого ангидрида в присутствии платинового катализатора:
Pt
2SO2 + O2 = 2SO3 – положительный катализ.
2. Замедление процесса образования хлороводорода в присутствии кислорода:
О2
H2 + Cl2 = 2HCl – отрицательный катализ.
Различают: а) гомогенный катализ – реагирующие вещества и катализатор образуют однофазную систему; б) гетерогенный катализ – реагирующие вещества и катализатор образуют систему из разных фаз.
Механизм действия катализатора. Механизм действия положительных катализаторов сводится к уменьшению энергии активации реакции. При этом образуется активный комплекс с более низким уровнем энергии и скорость химической реакции сильно возрастает. На рис. 6.3 представлена энергетическая диаграмма химической реакции, протекающей в отсутствие (1) и в присутствии (2) катализатора.
Если медленно протекающую реакцию А + В = АВ вести в присутствии катализатора К, то катализатор вступает в химическое взаимодействие с одним из исходных веществ, образуя непрочное промежуточное соединение: А + К = АК.
Энергия активации этого процесса мала. Промежуточное соединение АК – реакционноспособно, оно реагирует с другим исходным веществом, при этом катализатор высвобождается и выходит из зоны реакции:
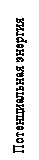  |
АК +В = АВ + К.
Суммируя оба процесса, получаем уравнение быстро протекающей реакции: А + В + (К) = АВ + (К).
Пример. Окисление сернистого ангидрида с участием катализатора NO: 2SO2 + O2 = 2SO3 – медленная реакция;
При введении катализатора – NO – образуется промежуточное соединение: 2NO + O2 = 2NO2.
Далее: SO2 + NO2 = SO3 + NO – быстрая реакция.
В гетерогенном катализе ускоряющее действие связано с адсорбцией. Адсорбция – явление поглощения газов, паров, растворенных веществ поверхностью твердого тела. Поверхность катализатора неоднородна. На ней имеются так называемые активные центры, на которых происходит адсорбция реагирующих веществ, что увеличивает их концентрацию.
Некоторые вещества снижают или полностью уничтожают активность твердого катализатора – каталитические яды (к ним относятся соединения свинца, мышьяка, ртути, цианистые соединения). Особенно чувствительны к каталитическим ядам платиновые катализаторы.
Есть и такие вещества, которые усиливают действие катализатора, хотя сами катализаторами не являются. Эти вещества называются промоторами.
| <== предыдущая страница | | | следующая страница ==> |
| Исходные вещества Активированный комплекс Продукты реакции | | | Общие представления о химическом равновесии. Константа химического равновесия |
Дата добавления: 2014-09-29; просмотров: 402; Нарушение авторских прав

Мы поможем в написании ваших работ!