
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Диаграмма состояния
Сразу всем раздать диаграмму железо- углерод
Это графическое изображение фазового состава сплавов в состоянии равновесия (или близком к нему) во всем диапазоне температур и концентраций компонентов.
Диаграмма состояния показывает устойчивые состояния, т.е. состояния, которые при данных условиях обладают минимумом свободной энергии. Поэтому ее также называют диаграммой равновесия, так как она показывает, какие при данных условиях существуют равновесные фазы.
Термический анализ — раздел материаловедения, изучающий изменение свойств материалов под воздействием температуры. Обычно выделяют несколько методов, отличающихся друг от друга тем, какое свойство материала измеряется:
Объединяющей сущностью всех перечисленных методов является то, что отклик образца записывается в зависимости от температуры (и времени).
Обычно изменение температуры осуществляется по заранее заданной программе — либо это непрерывное увеличение или уменьшение температуры с постоянной скоростью (линейный нагрев/охлаждение), либо серия измерений при различной температуре (ступенчатые изотермические измерения). Используются и более сложные температурные профили, использующие осциллирующую (обычно в виде синусоидальных или прямоугольных колебаний) скорость нагревания (Термический анализ с модулированной температурой) или изменяющие скорость нагревания в ответ на изменение свойств системы (Термический анализ контролируемый образцом).
В дополнение к управлению температурой образца также важно управлять средой, в которой проводятся измерения (например, атмосферой). Измерения могут быть выполнены на воздухе или в среде инертного газа (например, аргона или гелия). Также используется восстановительная или химически активная газовая среда, образцы помещаются в воду или другую жидкость.
Последовательность построения диаграмм термическим методом (компоненты А и В, фазы a , L) (смотрят, при каких температурах исследуемые свойства изменяются не линейно, а скачком):
- изготавливают несколько сплавов с известной концентрацией (сплав I, II, III, компоненты А и В);
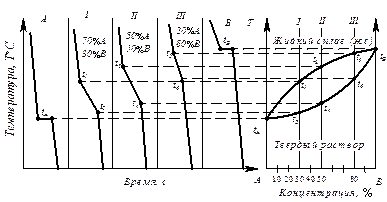
Рис. Диаграмма состояния с образованием неограниченных твердых растворов, построенная термическим методом (диаграмма II рода)
- строят кривые охлаждения для каждого сплава в координатах температура – время, по которым определяют температуры начала и конца кристаллизации сплава (наблюдаются точки перегиба и температурные остановки);
- переносят критические точки, найденные для каждого сплава, в систему координат концентрация – температура;
- строят диаграмму состояния системы (для всего диапазона концентраций), соединяя критических точки плавными кривыми.
По диаграмме состояния можно определить температуры фазовых превращений, изменение фазового состава, приблизительно, свойства сплава, виды обработки, которые можно применять для сплава.
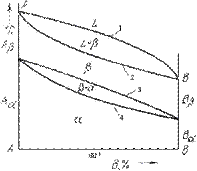
Рис. Диаграмма состояния
Шкала концентраций показывает содержание компонента В (но часто нет стрелочки). Оси ординат соответствуют чистым компонентам (100 % А и 100 % В).
Линии диаграммы являются совокупностями критических точек для всех промежуточных концентраций. Основными линиями являются линии ликвидус (1) и солидус (2), а также линии соответствующие фазовым превращениям в твердом состоянии (3, 4).
Пример. Записать все диапазоны и превращения.
Вертикальная линия, соответствующая чистому компоненту А(0% В), является диаграммой состояния компонента А. При нагревании чистого компонента А до он находится в виде модификации a (А-a). При переходе через Т А1 происходит фазовое превращение в твердом состоянии, а именно полиморфное превращение в модификацию β (А-β). При дальнейшем нагреве при температуре Т А2, которая является температурой плавления (соответственно и температурой кристаллизации) компонент А-β плавится и выше этой критической точки находится в жидком состоянии.
Вертикальная линия, соответствующая чистому компоненту В (100 % В), является диаграммой состояния компонента В. Критические точки – Т В1 и Т В2.
Вертикальная линия С, соответствует сплаву с содержанием 20 % В (80 % А). Так же, как и другие сплавы системы, имеет четыре критические точки: две точки начала и конца полиморфного превращения Т С1 и Т С2 + две точки начала и конца: точка солидус Т С3 и точка ликвидус Т С4. Т.е. и первичное превращения сплава происходят не при постоянной температуре, а в интервале температур.
В областях 1, 2, 3 – сплав однофазен (жидкая фаза, твердые фазы - a и β). Линия Т А2- Т С4- Т В2 – линия ликвидус. Линия Т А2- Т С34- Т В2 – линия солидус.
В областях 4, 5 – сплав двухфазен (жидкая фаза+твердая фаза-a, две твердые фазы a и β).
Система в узком смысле – это металлический сплав заданной концентрации в данное время, т.е. при данной температуре – это фактически точка на диаграмме состояния. Он и представляет собой совокупность фаз, согласно данному выше теоретическому определению
Допустим, в качестве исследуемой системы мы выбрали сплав с соотношением компонентов А и В 50 на 50 при комнатной температуре. В качестве метода исследования выбрали микроскоп. Сделали шлиф. Смотрим и видим – чередование белых и черных зерен. Очевидно, это эвтектика. Называем ее эвтектика АВ, отмечаем на диаграмме состояния. Берем сплавы левее – растет число белых зерен и правее – число черных. Вдруг, увидели какую-то новую фазу. Это будет означать, что мы пересекли линию диаграммы.
Система в более широком смысле – это совокупность всех сплавов, возможных для данных компонентов в диапазоне температур обычно от комнатной до несколько превышающей температуру плавления самого тугоплавкого компонента.
Резюме (фактически):
- Диаграмма состояния сплава с заданной концентрацией компонентов – это совокупность критических точек сплава, отмеченных на соответствующей вертикальной линии.
- Диаграмма состояния сплавов всего диапазона концентраций – совокупность линий, образованных всеми критическими точками системы.
Железоуглеродистые сплавы.
Диаграмма железоуглеродистых сплавов может быть представлена в двух вариантах:
- метастабильном, отражающем превращения в системе «железо-карбид железа» (иначе железо-цементит (Fe-Fe3C).
- стабильном, отражающем превращения в системе «железо-графит» (Fe-C).
Цементит – это химическое соединение. Устойчивое химическое соединение можно рассматривать как компонент, а диаграмму – по частям. Так как на практике применяют металлические сплавы с содержанием углерода до 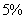 , то рассматриваем часть диаграммы состояния от железа до химического соединения цементита, содержащего
, то рассматриваем часть диаграммы состояния от железа до химического соединения цементита, содержащего 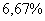 углерода.
углерода.
Особенности железоуглеродистых сплавов определяются полиморфизмом железа и углерода, а также ферромагнетизмом железа. Эти элементы взаимодействуют, образуя различные фазы.
Практическое применение диаграммы Fe – Fe3C:
1. Определение температур фазовых превращений (плавления, кристаллизации, полиморфных превращений, температуры растворимости фаз);
2. Определение температурных интервалов термической обработки, горячей и холодной обработки металлов давлением.
Основные фазы диаграммы Fe – Fe3C.
Фазы в углеродистых сталях определенным образом располагаются в их объемах, образуя в зависимости от массовой доли углерода, ту или иную структуру. Равновесные структуры углеродистых сталей указываются на структурной диаграмме «железо – цементит».
1. Жидкая фаза
Представляет собой неограниченный раствор железа и углерода, распространяющийся выше линии ликвидус АСD – от 0 до 6.67 %С.
2. Твердые фазы.
2.1 Твердые растворы.
В данной системе имеются твердые растворы железа с углеродом на основе двух кристаллических модификаций железа. Они являются твердыми растворами внедрения, т.е. атомы железа занимают узлы пространственной решетки, а атомы углерода размещаются в междоузлиях. В каждой модификации железа растворяется строго определенное количество углерода.
Феррит (обозначают Ф или Fe-α (С)) – твердый раствор внедрения углерода в Fe-α. Имеет ОЦК – решетку. Очень мягок, пластичен, ферромагнитен до Т=768 оС. Существует при низких температурах и в области высоких температур.
Аустенит (обозначают А или Fe-g (С)) - твердый раствор внедрения углерода в Fe-g. Имеет ГЦК – решетку. Прочен, пластичен, парамагнитен. При нормальной температуре в равновесном состоянии не существует.
2.2 Химическое соединение
Цементит (Ц или Fe3C) – карбид железа. Имеет сложную кристаллическую решетку (орторомбическая). Очень тверд, хрупок, очень низкая пластичность. Слабо ферромагнитен до 210 ºC.
В железоуглеродистых сплавах присутствуют фазы: цементит первичный (ЦI), цементит вторичный (ЦII), цементит третичный (ЦIII).
Состав этих фаз одинаков, отличаются их размеры, количество и расположение в структуре сплава, что существенно влияет на его свойства.
2.3 Механические смеси
- перлит – эвтектоид феррита и цементита. Содержит 0,8 % С (точка S);
- ледебурит – эвтектика аустенита и цементита в интервале температур 1147 – 727 оС или перлита и цементита при температурах ниже 727 оС. Содержит 4,3 % углерода (точка С).
| <== предыдущая страница | | | следующая страница ==> |
| Виды фазовых превращений | | | Основы термообработки и поверхностного упрочнения сплавов |
Дата добавления: 2014-12-09; просмотров: 355; Нарушение авторских прав

Мы поможем в написании ваших работ!