
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Подлинность
Перед испытанием на подлинность оксид цинка растворяют в кислотах. С сульфидом натрия образует белый ( в отличии от других тяжелых металлов ) осадок сульфида свинца:
ZnSO4 + Na2S → ZnS↓ + Na2SO4
При взаимодействии с гексацианоферратом калия образует белый гелеобразный осадок, растворимый в щелочах, но не растворимый в кислотах:
ZnSO4 + K4[Fe(CN)6] → K2[ZnFe(CN)6]↓ + K2SO4
Специфическая реакция на цинк во всех его соединениях – реакция образования зелени Ринмана, при прокаливании с нитратом кобальта (II):
2ZnO +2Co(NO3)2→ 2CoZnO2+4NO2↑+O2↑
Количественное определение.
Комплексонометрическое титрование трилоном Б в аммиачном буфере в присутствии индикатора (эриохромовый черный)
Биологическое действие и применение.
Оба препарата за счёт образования альбуминатов оказывает вяжущее антисептическое и местное противовоспалительное действие, цинка оксид, как не растворимое соединение, оказывает подсушивающее действие. Применяют цинка оксид в виде присыпок, мазей при дерматитах, экземах, геморрое, тропической язве, опрелостях кожи. Цинка сульфат в виде водных растворов применят при конъюнктивите, ларингите, для спринцевания при уретрите и вагините.
Hydrargyri dichloridun (HgCl2) – ртути дихлорид (сулема).
Свойства: белый тяжёлый порошок или белые кристаллы. Растворим в воде, спирте, эфире, кислотах.
Получают при нагревании смеси паров ртути и хлора при 345÷355°C:
Hg + Cl2 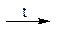 HgCl2,
HgCl2,
| <== предыдущая страница | | | следующая страница ==> |
| Препараты цинка | | | Количественное определение. К водному раствору препарата добавляют избыток йодида калия, при этом образуется свободный йод, который оттитровывают тиосульфатом натрия |
Дата добавления: 2014-12-09; просмотров: 297; Нарушение авторских прав

Мы поможем в написании ваших работ!