
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Лабораторная работа № 1. «Определение молярной массы магния»
«Определение молярной массы магния»
Цель работы
Определить молярную массу металлического магния по его реакции с соляной кислотой. Сравнить полученное экспериментальное значение с теоретическим и вычислить ошибку эксперимента.
Теоретическая часть
Молярная масса (М) – величина, равная отношению массы вещества к его количеству.  [г/моль], т.е. это масса одного моля. Моль – количество вещества, содержащее
[г/моль], т.е. это масса одного моля. Моль – количество вещества, содержащее  (число Авогадро) структурных единиц (атомов, молекул, ионов и т.д.). Молярная масса численно равна относительной молекулярной массе (Мrelativ), вычисленной по таблице Д.И. Менделеева.
(число Авогадро) структурных единиц (атомов, молекул, ионов и т.д.). Молярная масса численно равна относительной молекулярной массе (Мrelativ), вычисленной по таблице Д.И. Менделеева.
Например: 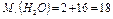
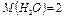 г/моль.
г/моль.
Реакция магния с соляной кислотой протекает по уравнению:

1моль 2моля 1моль 1моль
при этом: 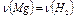 (1), т.е.
(1), т.е.  (2)
(2)
т.к.  г/моль
г/моль
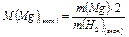 (3)
(3)
Для определения молярной массы магния навеску металла взвешивают на аналитических весах с точностью 0.0001 г. и растворяют в избытке HCl. Выделяющийся газообразный водород собирают и вычисляют его массу по уравнению Менделеева – Клайперона.
 (4)
(4)
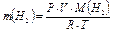 (5)
(5)
Затем по уравнению (3) вычисляют экспериментальное значение молярной массы магния.
Экспериментальная часть
Опыт проводится в установке, схема которой приведена на рисунке.
 |
Mg HCl
Рис. Схема установки
1 – реакционный сосуд; 2 – пробка с резиновым шлангом; 3 – мерная бюретка с калиброванным шаром; 4 – уравнительная склянка с водой; 5 – кран сообщения с атмосферой
Ход работы:
1. В малое колено реакционного сосуда поместить навеску магния (например, 0, 2570 г.).
2. В большое колено осторожно по стенке налить 15 мл 15% раствора HCl.
3. Удерживая сосуд горизонтально закрыть его пробкой 2.
4. При открытом кране 5 поднять уравнительную склянку с водой 4 и установить уровень воды в мерной бюретке к нулевому делению (верхний обрез шара).
5. Закрыть кран 5, опустить уравнительную склянку на стол и проверить герметичность прибора. За 1 минуту уровень воды в бюретке не должен заметно опускаться.
6. Осторожно наклонить реакционный сосуд и по каплям приливать кислоту к магнию. Наблюдать бурное выделение водорода и вытеснение воды из мерной бюретки.
7. По окончании реакции передвигать уравнительную склянку вдоль шкалы бюретки до совпадения уровней воды и записать объем выделившегося водорода (например, 312 мл).
8. Разобрать прибор, промыть реакционный сосуд дистиллированной водой.
Пример расчета экспериментального значения молярной массы магния
Исходные данные:
m (Mg) = 0,2570 г.
Р = 731 мм рт.ст. (по барометру).
Т = 298 К (25°С по термометру).
R = 8,31 Дж/моль∙К.
По уравнению Менделеева-Клайперона масса водорода равна:
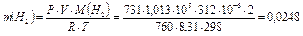 г
г
Экспериментальная молярная масса магния равна:
 г/моль
г/моль
Теоретическая молярная масса магния по таблице Менделеева равна
 г/моль
г/моль
Расчет ошибок эксперимента:
1. Абсолютная ошибка:
 г
г
2. Относительная ошибка:

Выводы:
1. Экспериментально определено значение молярной массы магния, равное 20,72 г/моль.
2. Относительная погрешность составила 14,7 %.
| <== предыдущая страница | | | следующая страница ==> |
| Порядок сдачи и проверки отчета | | | Лабораторная работа № 2. Определить направление смещения химического равновесия для реакций, протекающих в жидкой и газообразной фазе |
Дата добавления: 2015-06-30; просмотров: 266; Нарушение авторских прав

Мы поможем в написании ваших работ!