
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Контрольная работа 1. 1. Определите ΔrH˚298 реакции синтеза акриловой кислоты
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 18
1. Определите ΔrH˚298 реакции синтеза акриловой кислоты:
СНºСН (г) + СО (г) + Н2О (ж) ® СН2=СНСООН (ж),
если известны теплоты сгорания веществ – участников реакции:
| Вещество | СНºСН (г) | СО (г) | Н2О (ж) | СН2=СНСООН (ж) |
ΔсH˚298, 
| -1299,63 | -282,92 | -1368,03 |
2. Вычислите ΔfH˚298 MgCO3 (кр), пользуясь следующими данными:
С (гр) + О2 (г) ® СО2 (г); ΔrH˚298 = -393,5 кДж
2Mg (кр) + О2 (г) ® 2MgO (кр); ΔrH˚298 = -1203,6 кДж
MgО (кр) + СО2 (г) ® MgCO3 (кр); ΔrH˚298 = -117,7 кДж
3. Можно ли восстановить Fe2O3 алюминием до свободного металла при температуре 500 К. Ответ аргументируйте расчётом.
4. Сформулируйте принцип Ле-Шателье. В какую сторону смещается равновесие в системе при повышении давления, при понижении температуры?
5. Энергия активации реакции разложения йодида водорода при использовании катализатора (Pt) уменьшится с 168 до 59 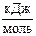 . Во сколько раз возрастёт скорость реакции при 500 К?
. Во сколько раз возрастёт скорость реакции при 500 К?
6. Для реакции Н2 (г) + Br2 (г) « 2HBr (г) при некоторой температуре К = 1. Определите состав (в процентах по объёму) равновесной реакционной смеси, если 1 л исходной смеси содержал 3 моля Н2 и 2 моля Br2.
| <== предыдущая страница | | | следующая страница ==> |
| Контрольная работа 1. Химическая термодинамика | | | Контрольная работа 1. 1. Тепловой эффект реакции: СО (г) + 2Н2 (г) ® СН3ОН (ж) ΔrН˚298 = -128,1 кДж |
Дата добавления: 2015-06-30; просмотров: 162; Нарушение авторских прав

Мы поможем в написании ваших работ!