
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Коагуляция – процесс объединения коллоидных частиц с образованием более крупных агрегатов из-за потери коллоидным раствором агрегативной устойчивости
Коагуляцию можно вызвать различными внешними агентами:
Þ действием небольших количеств электролита (наиболее важный фактор);
Þ изменением температуры (сильное нагревание или охлаждение);
Þ концентрированием коллоидного раствора;
Þ действием ультразвука, электромагнитного поля и др.
Согласно правилу Шульце – Гарди: коагулирующим действием обладает тот ион электролита, который имеет заряд, противоположный заряду гранулы. Коагулирующее действие ионов  тем сильнее, чем выше заряд иона – коагулятора (правило значимости).
тем сильнее, чем выше заряд иона – коагулятора (правило значимости).
Однако от правилаШульце – Гарди встречаются отклонения, поскольку на порог коагуляции кроме заряда иона- коагулянта влияет радиус этого иона и природа иона,сопутствующего иону-коагулянту.
Поэтому влияние электролитов на коагуляцию коллоидных растворов необходимо учитывать при введении растворов солей в живые организмы. При этом важно помнить, что имеет значение не только концентрация электролита, но и заряд иона. Так, изотонический 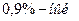 раствор
раствор 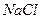 нельзя заменить изотоническим раствором
нельзя заменить изотоническим раствором  , так как двухзарядные ионы обладают более высоким коагулирующим действием, чем однозарядные.
, так как двухзарядные ионы обладают более высоким коагулирующим действием, чем однозарядные.
Кроме того, коагуляция в ряде случаев зависит и от способа прибавления электролита–коагулятора. Экспериментально доказано, что если электролит добавлять к золю небольшими порциями, то в итоге коагуляция наступает при более высокой концентрации электролита, чем при внесении сразу большого его количества и такое явление называют привыканием золей. Причиной привыкание золей может быть образование петизатора или адсорбция ионов, заряженных одноименно с частицей, что приводит к повышению первоначального заряда частиц.
В целом, принимая во внимание эти данные, следует заметить, что растворы электролитов необходимо водить внутривенно или внутримышечно очень медленно, чтобы не вызвать коагуляцию. При быстром введении из-за медленной скорости диффузии может произойти локальное накопление электролита, превышающее пороговую концентрацию, что приведет к коагуляции биосубстратов. При медленном введении электролит уносится с током крови, диффундирует в соседние ткани. Пороговая концентрация при этом не достигается и коагуляция не наступает.
Задача №2. Золь бромида серебра, получаемой по реакции:
 при некотором избытке
при некотором избытке  , коагулируют растворами сульфата калия /
, коагулируют растворами сульфата калия / 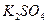 / и ацетата кальция /
/ и ацетата кальция / 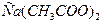 /. Какого электролита коагулирующее действие сильнее?
/. Какого электролита коагулирующее действие сильнее?
Решение.
1. Строение мицеллы золя 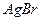 следующее:
следующее:
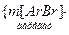
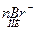
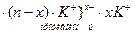
2. Согласно правиле Шульце – Гарди, коагуляция золя 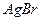 с отрицательно заряженными гранулами (потенциалопределяющий ион – анион
с отрицательно заряженными гранулами (потенциалопределяющий ион – анион 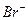 ) происходит за счет действия положительно заряженных ионов. Так как заряд иона
) происходит за счет действия положительно заряженных ионов. Так как заряд иона 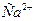 выше заряда иона
выше заряда иона 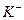 , то наилучшим коагулирующим действием будет обладать раствор
, то наилучшим коагулирующим действием будет обладать раствор 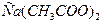 .
.
Ответ. Раствор 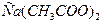 .
.
Дата добавления: 2015-07-26; просмотров: 218; Нарушение авторских прав

Мы поможем в написании ваших работ!