
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Прибор для титрования
| № пробирки | Объем раствора кислоты, мл | Индикатор, число капель | Объем израсходованного объема щелочи, мл |
| 5 мл HCl + 15 мл H2О | 1,5 | ||
| 5 мл HCl + 15 мл H2О | |||
| 5 мл HCl + 15 мл H2О | 2,1 | ||
| Среднее значение: | 1,87 |
Титруем (добавляем медленно по капле) 0,1 нормального раствора NaOH раствор HCl неизвестной концентрации до изменения окраски индикатора (метиловый оранжевый) с розовой до желтой с оранжевым оттенком.
Уравнение реакции:
HCl + NaOH = NaCl + H2O;
H+ + Cl- + Na+ + OH- = Na+ + Cl- + H2O;
Н + + OH- = H2O
Расчеты проводим по уравнению закона эквивалентов:
Сн (HCl) × V(HCl) = Сн (NaOH) × V(NaOH),отсюда:Сн (HCl) = 
Сн (HCl) = 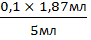 = 0,0374 мл
= 0,0374 мл
Вывод: определил концентрацию раствора соляной кислоты (HCl) титрованием раствором щелочи гидроксида натрия (NaOH). Она равна 0,0374 мл.
Опыт 2
Отобрали пипеткой в коническую колбу 5 мл раствора кислоты, добавили дистиллированной воды 15-20 мл, внесли 3 капли индикатора. Раствор щелочи поместили в бюретку, довели уровень в бюретке до нуля. Провели ориентировочный опыт – титрование H2SO4 раствором NaOH добавляя небольшими порциями щелочь из бюретки в колбу до изменения окраски.
Затем 4 конические колбы отобрали по 5 мл раствора кислоты, добавили дистиллированной воды и внесли индикатор. Оставили одну колбу в качестве контрольной, а с 3 – повторили титрование, но более точно. Последние порции щелочи прибавляли по каплям. Определили объем, израсходованной щелочи и заполнили таблицу:
| № | Объем раствора кислоты, мл | Индикатор , число капель | Объем израсходованного раствора щелочи, мл |
| 5,1 | 5,5 | ||
| Среднее значение: 5,25 |
 H2SO4+NaOH=Na2SO4+H2O
H2SO4+NaOH=Na2SO4+H2O
CЩ=2,64
Сн (H2SO4) = 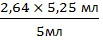 = 2,772 мл
= 2,772 мл
Вывод: определил концентрацию раствора соляной кислоты (H2SO4) титрованием раствором щелочи гидроксида натрия (NaOH). Она равна 2,772 мл.
| <== предыдущая страница | | | следующая страница ==> |
| Логическое проектирование баз данных | | | ЛИПОПРОТЕИНЫ |
Дата добавления: 2015-07-26; просмотров: 186; Нарушение авторских прав

Мы поможем в написании ваших работ!