
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
СВИНЦОВЫЙ АККУМУЛЯТОР
Пластины свинцового аккумулятора отливают из свинца. Количество энергии, которое можно накопить в аккумуляторе, пропорционально размерам поверхности его пластин, омываемой электролитом. Для увеличения этой поверхности аккумулятор имеет по нескольку положительных и отрицательных пластин. Все положительные и отрицательные пластины объединены в два отдельных полублока (рис. 183). Пластины изготовляют в виде решеток с ячейками. Ячейки заполняют пористой активной массой. Благодаря этому еще больше увеличивается поверхность соприкосновения пластин с электролитом.
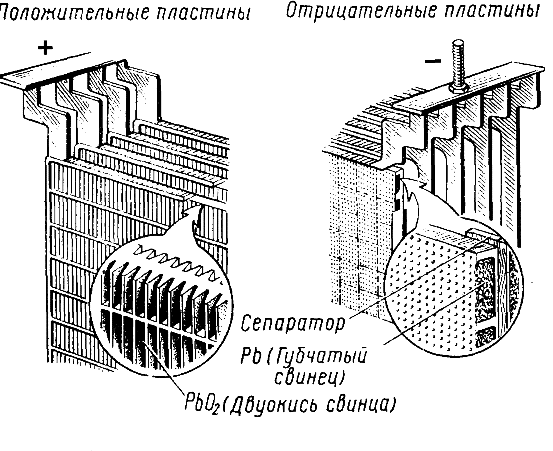
Рис. 182. Пластины свинцового аккумулятора
При сборке аккумулятора после каждой отрицательной пластины вставляется положительная. По краям с двух сторон стоят отрицательные пластины, так как положительные пластины склонны к короблению. Поэтому в свинцовом аккумуляторе отрицательных пластин всегда на одну больше, чем положительных. Во избежание касания пластины в процессе сборки аккумулятора отделяют друг от друга прокладками-сепараторами. Сепараторы должны обеспечивать свободный доступ электролита к пластинам (за счет пористости), обладать высокой химической стойкостью и большой механической прочностью.
Здесь, как и во многих других областях техники, на помощь пришла химия. Были созданы синтетические аккумуляторные сепараторы —полихлорвиниловые, стекловойлочные и ряд других. Для получения необходимой пористости в полихлорвиниловых сепараторах делается большое количество мелких отверстий. Поэтому такие сепараторы называют перфорированными. Полихлорвиниловые сепараторы могут быть микропористыми (поровинил). Хорошим материалом для сепараторов служит стекловойлок, состоящий из тончайших нитей стекла. Стекловойлок обладает наибольшей пористостью и химически инертен. Однако механическая стойкость стекловойлока мала. Сепараторы из стекловойлока успешно применяются в комбинации с сепараторами из других материалов, имеющих большую механическую прочность.
Собранный блок положительных и отрицательных аккумуляторных пластин опускают в сосуд, называемый баком или банкой. Эти сосуды изготовлены из кислотоупорных материалов, чаще всего из эбонита или специальных пластмасс. Во избежание расплескивания электролита аккумуляторная банка сверху закрыта крышкой. В крышке имеются отверстия, через которые выводятся наружу контактные штыри-выводы аккумулятора.
Электролитом в свинцовых аккумуляторах служит раствор чистой серной кислоты (ее химическая формула H2SO4) в дистиллированной воде. Серная кислота имеет плотность 1,83 г/см3, вода — 1 г/см3. Поэтому плотность электролита превышает 1 г/см3, обычно она находится в пределах 1,2— 1,4 г/см3.
Полностью собранный и заполненный электролитом аккумулятор подключают для заряда к источнику электрической энергии. Режимы заряда каждого типа аккумулятора указаны в инструкции, прилагаемой к нему. В процессе первого специального заряда нового аккумулятора, который называют формовкой аккумулятора, в результате электрических процессов активная масса положительных пластин превращается в перекись свинца РЬО2, т. е. соединение свинца с кислородом, богато насыщенное последним. Активная масса отрицательных пластин переходит в чистый пористый свинец РЬ, называемый губчатым. Кроме того, при этих процессах выделяется серная кислота H2SO4, поэтому плотность электролита повышается.
Когда необходимо использовать энергию, накопленную в аккумуляторе, его включают в соответствующую электрическую цепь. Аккумулятор отдает энергию, вырабатываемую за счет химических процессов, в результате которых активная масса положительных и отрицательных пластин превращается в сернокислый свинец PbSO4, называемый также сульфатом свинца. При этих реакциях выделяется вода, разбавляющая электролит, поэтому его плотность падает.
Напряжение на зажимах аккумулятора в начале разряда составляет 2,1—2 В. Измерять напряжение аккумулятора нужно под нагрузкой с помощью специальной нагрузочной вилки с вольтметром. Лишь в этом случае мы определим действительное его значение. По мере разряда оно медленно снижается до 1,8—1,7 В. Дальнейший разряд аккумулятора должен быть прекращен, хотя при этом будет использовано лишь около 1/3 активной массы пластин. Более глубокие разряды аккумулятора губительно отзовутся на нем вследствие сульфатации пластин. Образование сульфата свинца на поверхности, в порах активной массы положительных и отрицательных пластин аккумулятора при его разряде является естественным химическим процессом, в результате которого происходит отдача электрической энергии. В первый период разряда аккумулятора образуются мелкие кристаллы сульфата свинца. Такие кристаллы не закупоривают поры в активной массе пластин. При последующем заряде аккумулятора они полностью превращаются в двуокись свинца на положительных пластинах и губчатый свинец на отрицательных пластинах. В случае глубоких разрядов аккумуляторов, а также при систематических недозарядах, загрязнении электролита, хранении в незаряженном состоянии и вследствие некоторых других причин сульфат свинца перекристаллизовывается и приобретает крупнокристаллическое строение. Пластинысульфатируются — покрываются белым слоем крупнокристаллического сульфата свинца, который имеет плохую электропроводность. Крупные кристаллы сульфата свинца закупоривают поры в активной массе пластин. В результате прекращается доступ электролита во внутренние слои активной массы пластин, повышается внутреннее сопротивление аккумулятора, снижается его емкость. Образование крупнокристаллического сульфата, занимающего большой объем, приводит также к разбуханию, выпучиванию и выпадению активной массы пластин. При заряде аккумулятора крупнокристаллический сульфат медленно и не полностью превращается в исходную активную массу пластин. Поэтому необходим своевременный заряд аккумуляторов. После включения на заряд напряжение на выводах аккумулятора быстро повышается с 1,7 — 1,8 до 2,1— 2,2 В и затем очень медленно до 2,3 В. В конце заряда происходит повышение напряжения до 2,6 — 2,8 В и начинается «кипение» аккумулятора, т. е. бурное выделение газов (водорода и кислорода) вследствие разложения воды электрическим током. Резкое повышение напряжения и «кипение» аккумулятора свидетельствуют об окончании заряда. После отключения аккумулятора от источника электрической энергии его напряжение почти сразу падает приблизительно до 2, Г В.
Выделение водорода и кислорода, хотя и менее интенсивное, происходит и при других режимах работы аккумуляторов. Известно, что водород и кислород образуют взрывчатую смесь, называемую гремучим газом. Поэтому категорически запрещается входить с огнем в аккумуляторные помещения.
Количество электричества, которое отдает в цепь аккумулятор при разряде, всегда меньше, чем полученное им при заряде, так как часть энергии теряется на нагревание электролита и побочные химические процессы. Отношение количества электричества в ампер-часах, отданного при разряде аккумулятора (емкости), к полученному при заряде количеству электричества называется коэффициентом отдачи аккумулятора по емкости. Для кислотных аккумуляторов эта величина достигает 90—95%.
Коэффициентом отдачи аккумулятора по энергии, т. е. коэффициентом полезного действия, называется отношение количества энергии в киловатт-часах, отданной при разряде, к количеству энергии, затраченной при заряде аккумулятора. К. п. д. кислотных аккумуляторов составляет 70—80%.
| <== предыдущая страница | | | следующая страница ==> |
| АККУМУЛЯТОР — ХИМИЧЕСКИЙ ИСТОЧНИК ТОКА | | | ЩЕЛОЧНОЙ АККУМУЛЯТОР |
Дата добавления: 2015-07-26; просмотров: 205; Нарушение авторских прав

Мы поможем в написании ваших работ!