
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Реакции термического разложения некоторых кислых солей ( NaHCO3, NaH2PO4, Na2HPO4, NaHSO4)
2NaHCO3 =(t) Na2CO3 + CO2+ H2O NaH2PO4=(t) NaPO3 + H2O
2Na2HPO4=(t) Na4P2O7 + H2O
2NaHSO4=(t) Na2S2O7 + H2O
-
29. Гидролиз солей (по катиону, по аниону, одновременный гидролиз двух солей).
Поляризационное взаимодействие катионов и анионов с сильно полярными молекулами воды ведет к особой химической реакции ионного обмена, называемой гидролизом солей.
Молекулярная причина гидролиза – поляризационное взаимодействие ионов с сильно полярной молекулой воды. В результате катионы «вырывают» из молекулы воды ОН-, а анион – Н+. Другими словами, катионы и анионы вторгаются в равновесие диссоциации воды, нарушают его, в результате в случае катиона р-р становится кислым (гидролиз по катиону), в случае аниона – щелочным (гидролиз по аниону).
Гидролиз соли по катиону и по аниону одновременно можно представить в общем виде следующим образом:
Kt+ + A- + H2O=KtOH + HA
Константа гидролиза имеет вид:
К гидр=Kw/(Kдис осн*Кдис кисл)
Пусть общая концентрация соли, гидролизованной одновременно по катиону и аниону, равна с моль/л, степень гидролиза составляет h. Тогда:
[KtOH]=[HA]=hc
[Kt+]=[A-]=c-hc отсюда
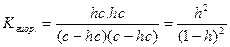 .
.
Гидролиз по катиону:
Продукты гидролиза подавляют вторую ступень, поэтому гидролиз реально протекает лишь по первой ступени: Ktn+ + H2O=KtOH(n-1)+ + H+
Кгидр=Kw/Kдис осн
Константа гидролиза − константа равновесия процесса гидролиза. Пусть с – общая концентрация катиона (общ. концентрация соли в случае симметричного электролита); h – степень гидролиза катиона Kt. Равновесные концентрации составляют:
[KtOH(n-1)+]=[H+]=hc;
[Ktn+]=c-hc
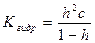 .
.
Способы подавления гидролиза:
1) охлаждение раствора;
2) добавление кислоты в раствор для подавления гидролиза по катиону, добавление щелочи в раствор для подавления гидролиза по аниону.
Гидролиз по аниону: Продукты гидролиза подавляют вторую ступень, поэтому гидролиз реально протекает лишь по первой ступени: Am- + H2O= HA(m-1)- + OH- .
Kгидр=Kw/Kдис кисл
Константа гидролиза − константа равновесия процесса гидролиза. Пусть с – общая концентрация катиона (общ. концентрация соли в случае симметричного электролита); h – степень гидролиза аниона Аn. Равновесные концентрации составляют: [HA(m-1)-]=[OH--]=hc
[Am-]=c-hc
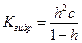 .
.
Способы усиления гидролиза солей:
1) разбавление раствора соли;
2) нагрев раствора, поскольку энтальпии гидролиза положительны;
3) добавление щелочи в раствор для усиления гидролиза по катиону, добавление кислоты в раствор для усиления гидролиза по аниону.
| <== предыдущая страница | | | следующая страница ==> |
| Образование аммиакатов и гидроксокомплексов металлов и их разрушение кислотами и при нагревании | | | История способа Байера |
Дата добавления: 2015-07-26; просмотров: 640; Нарушение авторских прав

Мы поможем в написании ваших работ!