
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Практическое применение тиофена и его производных
Циклическая система тиофена встречается в природе в некоторых продуктах растительного происхождения, но гораздо большее значение имеет это соединение в составе синтетических лекарственных препаратов и красителей.
Производные тиофена находят практическое применение в производстве различных красителей, пластификаторов, пластмасс, аналитических реагентов, инсектицидов. Уже давно начала успешно развиваться и приобрела большое промышленное значение химия тиоиндигоидных красителей. В основе этого класса красителей лежит сернистый аналог индиго – тиоиндиго.
Тиоиндиго – кубовый краситель красного цвета. Синтез тиоиндиго проводится по методам, очень близким к методам синтеза самого индиго. Класс тиоиндигоидных красителей включает красители разнообразных цветов и оттенков. На примере этих красителей изучается зависимость глубины окраски и изменения цвета от электронного взаимодействия тиоиндигоидного скелета с различными заместителями.
Используют тиофен в органическом синтезе.
Пиррол. Важнейший представитель пятичленных гетероциклов с одним гетероатомом. Он является родоначальником важных природных соединений, к которым принадлежат гем (компонент гемоглобина крови) и хлорофилл.

История открытия пиррола.Пиррола был обнаружен в костяном масле (продукт сухой перегонки костей) и в небольшом количестве в каменноугольной смоле (Рунге, 1834 г.). Строение его установлено А. Байером в 1870 г.
Электронное строение.Молекула пиррола плоская, что свидетельствует о гибридизации как атомов углерода, так и гетероатома азота. Причем три гибридизованные орбитали атома азота, принимающие участие в образовании σ-связей, лежат в плоскости кольца. Негибридизованная р-орбиталь гетероатома, расположенная перпендикулярно плоскости кольца, несет неподеленную пару электронов. При перекрывании p-орбитали кольцевого азота с негибридизованными ρ-орбиталями четырех атомов углерода кольца, несущих по одному электрону, образуется единая молекулярная система, содержащая в общей сложности шесть электронов (ароматический секстет):

Рисунок 2 – Строение молекулы пиррола
Таким образом, пиррол, как и бензол, и пиридин, подчиняется правилу ароматичности Хюккеля для п = 1.
Рассчитанное π-электронное распределение в молекуле пиррола показывает, что рассматриваемая система электроноизбыточна (шесть электронов перераспределены между пятью атомами кольца) и четыре атома углерода обладают большей π-электронной плотностью, чем атомы углерода бензола, хотя наибольшая электронная плотность сосредоточена на азоте.
Физические свойства.Пиррол легко растворяется в большинстве органических растворителей; на воздухе темнеет и постепенно осмоляется. При действии на пиррол минеральных кислот образуется полимерная масса темного цвета, не имеющая практического применения. Такая неустойчивость пиррола в сильнокислой среде называется ацидофобностью (что означает «кислотобоязнь»). Эту особенность следует учитывать при экспериментальной работе с пирролом.
| Свойства пиррола | Показатели |
| агрегатное состояние | жидкость |
| температура плавления | – 18 оС |
| температура кипения | 130 оС |
| растворимость в воде | слабо растворим |
| растворимость в спирте и эфире | легко растворим |
| запах | хлороформа |
| цвет | бесцветный |
Прототропная таутомерия пиролла – изомеризация, сопровождаю-щаяся миграцией протонизированного атома водорода от одного атома молекулы к другому (нуклеофильному) атому молекулы с одновременным перемещением кратной связи:
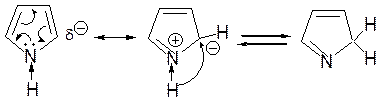
| <== предыдущая страница | | | следующая страница ==> |
| | | Основные способы получения |
Дата добавления: 2015-07-26; просмотров: 206; Нарушение авторских прав

Мы поможем в написании ваших работ!