
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Методика и порядок выполнения работы. 1. Пипетку Мора на или тщательно промыть дистиллированной водой и ополоснуть раза раствором буры
1. Пипетку Мора на 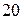 или
или  тщательно промыть дистиллированной водой и ополоснуть
тщательно промыть дистиллированной водой и ополоснуть  раза раствором буры.
раза раствором буры.
2. В колбы для титрования отобрать аликвотную часть  раствора буры и добавить по
раствора буры и добавить по  капли индикатора метилового оранжевого, раствор перемешать.
капли индикатора метилового оранжевого, раствор перемешать.
Порядок операций при отборе аликвоты раствора. При наборе раствора пипетку держать, по возможности, вертикально. Раствор в пипетке удерживать, закрывая ее верхнее отверстие указательным пальцем.
- Набрать раствор в пипетку выше уровня мениска с помощью груши или осторожно всасывая его ртом.
- Медленно спустить раствор до совпадения нижнего края мениска с риской; положение мениска определяют на уровне глаз. При установке мениска конец пипетки не должен касаться уровня раствора в мерной колбе.
Следите, чтобы раствор не попадал в рот! При необходимости, немедленно прополощите рот и проведите нейтрализацию химического вещества.
- Перенесите аликвоту в колбу для титрования, для чего, держа пипетку вертикально недалеко от дна, начинайте слив раствора, стараясь избежать его разбрызгивания. Раствор не выдувать!
После слива раствора, его остаток снимают следующим образом:
- колбу слегка наклонить, чтобы освободить от раствора часть дна;
- осторожно прикоснуться кончиком пипетки дна и выдержать 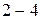 секунды пока не остановится мениск (часть раствора перейдет в колбу);
секунды пока не остановится мениск (часть раствора перейдет в колбу);
- быстро убрать кончик от дна колбы и положить пипетку на подставку или в колбу с раствором. В носике пипетки остается незначительное количество раствора, которое было учтено при ее калибровке (мертвый объем).
3. Бюретку на  промыть дистиллированной водой и ополоснуть
промыть дистиллированной водой и ополоснуть 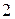 раза новыми порциями приготовленного раствора
раза новыми порциями приготовленного раствора  , сливая затем его в стакан. Заполнить бюретку раствором
, сливая затем его в стакан. Заполнить бюретку раствором  , удалив из ее носика воздух, и выставить положение мениска на нуль. Перед титрованием проверить, чтобы в носике бюретки не было пузырьков воздуха.
, удалив из ее носика воздух, и выставить положение мениска на нуль. Перед титрованием проверить, чтобы в носике бюретки не было пузырьков воздуха.
4. В каждую колбу добавить по  капли индикатора метилового оранжевого. Оттитровать раствор буры в 1-й колбе рабочим раствором
капли индикатора метилового оранжевого. Оттитровать раствор буры в 1-й колбе рабочим раствором  до перехода окраски индикатора от одной капли титранта с желтой на оранжевую. Сопоставьте полученную окраску с окраской раствора сравнения, при необходимости добавьте еще одну каплю титранта.
до перехода окраски индикатора от одной капли титранта с желтой на оранжевую. Сопоставьте полученную окраску с окраской раствора сравнения, при необходимости добавьте еще одну каплю титранта.
5. Определить израсходованный объем  в этой точке с точностью до
в этой точке с точностью до  . Повторить титрование раствора буры до получения трёх сходящихся результатов.
. Повторить титрование раствора буры до получения трёх сходящихся результатов.
6. По результатам титрования рассчитать среднее значение объема 
 , пошедшее на титрование аликвоты и вычислить концентрацию рабочего раствора
, пошедшее на титрование аликвоты и вычислить концентрацию рабочего раствора  по закону эквивалентов:
по закону эквивалентов:
 , (7.1)
, (7.1)
где  – объем аликвоты титруемого раствора (буры),
– объем аликвоты титруемого раствора (буры),  ;
; 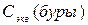 – молярная концентрация эквивалента титруемого раствора (буры),
– молярная концентрация эквивалента титруемого раствора (буры),  ;
;  – средний объем титранта
– средний объем титранта  ,
,  ;
;  – молярная концентрация эквивалента раствора титранта
– молярная концентрация эквивалента раствора титранта  ,
,  .
.
Запись данных опыта. Отчет оформить на новом листе, где привести все расчеты в общем и численном виде, а результаты занести в таблицу 7.1.
Таблица 7.1 – Стандартизация раствора  по буре
по буре
Концентрация
раствора буры,
 , , 
| Объем аликвоты
 (бура), (бура), 
| Объем раствора  , , 
| Концентрация раствора  , ,
 , , 
| |||

| 
| 
| 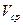
| |||
Содержание отчета и его форма
Каждый студент должен иметь лабораторный журнал, который является документом, отражающим всю его работу.
Все наблюдения и выводы по экспериментальной работе, проделанной в лаборатории, студент заносит в лабораторный журнал непосредственно после ее выполнения.
Рекомендуется следующая схема записи:
1. Дата.
2. Номер и название лабораторной работы.
3. Цель работы.
4. Название и описание хода опытов.
5. Наблюдения.
6. Уравнения химических реакций.
7. Выводы и расчеты (формулы, таблицы, графики).
Вопросы для защиты работы
1. Как устроена пипетка Мора? К какому виду посуды она относится? Какие еще виды пипеток применяют для отбора пробы?
2. Как правильно работать с пипеткой Мора?
3. Что такое аликвота? Для чего необходимо знать ее точный объем?
4. Перечислите основные виды титрования и приведите формулу закона эквивалентов для каждого из них. В каком случае их применяют?
5. Что понимают под: а) точкой эквивалентности; б) концом титрования; в) скачком кривой титрования?
6. Перечислите основные способы фиксации Т.Э. В чем их достоинства и недостатки?
7. Дайте определение индикатора. Какими свойствами он должен обладать?
8. Какой вид индикаторов применяют в протолитометрии и каким свойством они обладают?
9. Что такое стандартизация? С какой целью необходимо проводить эту операцию?
10. Укажите интервал перехода и цвет индикатора метилового оранжевого в каждом интервале.
11. Какой цвет будет иметь индикатор метиловый оранжевый в растворах  ,
, 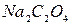 ,
,  ,
,  ,
,  ?
?
12. Какие растворы называют титрантом и титруемым? Как определяют их объемы?
13. Рассчитайте значения  и
и  для
для 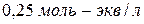 раствора
раствора  .
.
14. Рассчитайте  для раствора серной кислоты с
для раствора серной кислоты с  .
.
| <== предыдущая страница | | | следующая страница ==> |
| Приборы и реактивы. Бюретка на , химический стакан на или , пипетки Мора на или | | | Теоретическое обоснование. Стандартизация раствора выполняется методом пипетирования по вторичному стандарту |
Дата добавления: 2015-07-26; просмотров: 193; Нарушение авторских прав

Мы поможем в написании ваших работ!