
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Общие сведения, номенклатура ацетиленовых углеводородов
Ацетиленовые углеводороды – это ненасыщенные углеводороды, имеющие в своем составе одну тройную связь. Общая формула алкинов -СnH2n-2 . По систематической номенклатуре ацетиленовые углеводороды называют, заменяя в названиях суффикс -ан в предельных углеводородах на суффикс -ин.
Таблица 3
Углеводороды ряда ацетилена
| Предельные углеводороды | Этиленовые углеводороды |
| Метан СН4 | - |
| Этан С2Н6 | Этин (ацетилен) С2Н2 |
| Пропан С3Н8 | Пропин С3Н4 |
| Бутан С4Н10 | Бутин С4Н6 |
| Пентан С5Н12 | Пентин С5Н8 |
| Гексан С6Н14 | Гексин С6Н10 |
| и.т.д. | и.т.д. |
Тройная связь – это сочетание одной s- и двух p-связей.
В молекулах алкинов ненасыщенные (sp-гибридизованные) атомы углерода находятся ближе друг к другу, чем в алкенах (0,12 нм и 0,134 нм соответственно). p-электроны тройной связи несколько втянуты внутрь молекулы, поляризуемость этих электронов тройной связи уменьшена. Алкины труднее, чем алкены, присоединяют электрофильные реагенты. Алкины способны образовывать ацетилениды, вступая в реакции SN замещения (SN - от латинских слов substitution – замещение и nucleophilic – любящий ядро).
Атомы водорода в ацетилене обладают слабокислотными свойствами. Это объясняется тем, что электроотрицательность атома углерода находится в зависимости от его валентного состояния и изменяется в ряду:

 =3,2 относительных единиц
=3,2 относительных единиц
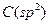 =2,8 относительных единиц
=2,8 относительных единиц
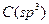 =2,5 относительных единиц
=2,5 относительных единиц
Таким образом, связь С – Н сильно поляризована в ацетилене и его моноалкилпроизводных приобретают некоторую подвижность в отличие от алкенов и алканов.

Стрелками показано смещение общей электронной плотности к более электроотрицательному атому углерода от менее электроотрицательного атома водорода.
| <== предыдущая страница | | | следующая страница ==> |
| Химические свойства алкенов | | | Химические свойства ацетиленовых углеводородов |
Дата добавления: 2015-07-26; просмотров: 269; Нарушение авторских прав

Мы поможем в написании ваших работ!