
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Химические свойства. В химическом отношении алканы малоактивны, за что и были названы парафинами (от лат
В химическом отношении алканы малоактивны, за что и были названы парафинами (от лат. parum affinis – лишенные сродства). Это объясняется прочностью s-связей, устойчивость которых обусловлена малым размером атома С и его тетраэдрической конфигурацией, что способствует максимальной концентрации электронной плотности между ядрами атомов. s-Связь
С–Н мало поляризована вследствие близости электроотрицательностей атомов С и Н. В силу этого алканы – малополярные вещества и труднополяризуемые, на них не действуют кислоты, щелочи, обычные окислители (например, КМnО4), металлы.
Для алканов возможен гомолитический (радикальный) разрыв связей, при этом происходят реакции замещения атомов Н, расщепления углеродного скелета (крекинг), окисления (частичного или полного).
1. Реакции замещения.
– Хлорирование.
В качестве примера реакций замещения рассмотрим реакцию хлорирования метана, которая относится к цепным радикальным реакциям. Процесс протекает энергично на свету или при нагревании (до 250–400оС). Первая стадия называется зарождением, или инициированием, цепи:
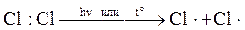
(под действием энергии квантов света или высокой температуры некоторые молекулы хлора гомолитически расщепляются на 2 атома, имеющих неспаренные электроны, – свободные радикалы).
Далее происходит развитие (рост) цепи:
Сl× + CН4 ® НСl + ×СН3 (метил); ×СН3 + Сl2 ® СН3Сl + ×Сl и т.д.
Обрыв цепи происходит, если сталкиваются два свободных радикала; при этом могут образоваться молекулы С2Н6, СН3Сl, Сl2.
При хлорировании других алканов легче всего замещение идет у третичного атома углерода (атома, который затрачивает на С–С-связь 3 валентности), затем у вторичного и в последнюю очередь – у первичного. При образовании полигалогензамещенных соединений атомы хлора преимущественно замещают атомы водорода у одного и того же или у соседних атомов углерода. – Закономерности В.В. Марковникова.
– Нитрование (реакция М.И. Коновалова, 1888 г.).
 .
.
Реакцию проводят 10%-ной азотной кислотой при температуре около 140°С и небольшом давлении.
2. Окисление.
В промышленности алканы окисляют кислородом воздуха на марганцевых катализаторах при температуре около 200°С. При этом расщепляются С–С-связи и получаются низкомолекулярные кислородсодержащие соединения – спирты, альдегиды, кетоны, карбоновые кислоты (см. Природные источники). Алканы горят на воздухе с выделением большого количества теплоты. Поэтому они широко используются в быту и технике в качестве высококалорийного топлива.
СН4 + 2О2 ® СО2 + 2Н2О + 890 кДж.
Алкены
Алкены (этиленовые углеводороды) – ненасыщенные углеводороды, молекулы которых содержат одну двойную связь С=С.
Общая формула алкенов – СnH2n.
Двойная связь образуется при помощи двух пар обобщенных электронов. Атомы углерода, связанные двойной связью, находятся в состоянии sp2-гибридизации, каждый из них образует 3 s-связи, лежащие в одной плоскости под углом 120°. Негибридные р-орбитали атомов углерода расположены перпендикулярно плоскости s-связей и параллельны друг другу и вследствие «бокового» перекрывания образуют p-связь, электронное облако которой расположено частично над, а частично под плоскостью молекулы.
| <== предыдущая страница | | | следующая страница ==> |
| Способы получения. Важнейшие синтетические методы получения | | | Способы получения. Пиролиз – процессы химических превращений органических соединений, происходящие при высокой температуре |
Дата добавления: 2015-07-26; просмотров: 293; Нарушение авторских прав

Мы поможем в написании ваших работ!