
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Гидрирование диеновых и ацетиленовых углеводородов
|
Читайте также: |
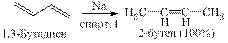
Данная реакция региоспецифична (образуется только один изомер, 2-бутен), однако при этом не стереоспецифична.
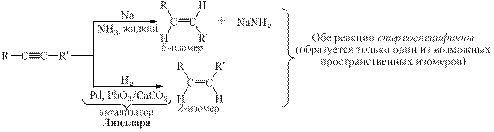
Строение алкенов
С точки зрения теории химической связи и теории гибридизации атомы углерода при двойной связи находятся в sp2-гибридном состоянии и образуют по 3σ- и одну π-связь. σ-Связи располагаются в одной плоскости по углом 120° (тригональная конфигурация). π-Связь образована путём бокового перекрывания p-орбиталей в плоскости, перпендиклярной плоскости образования σ-связей, что исключает свободное вращение вокруг C-C-связей и приводит к появлению геометрической изомерии.
Характеристики двойной связи
| Тип связи | Длина связи | Энергия связи, ккал/моль | Полярность Μ (D) | Вывод |
| C=C | 0.134 нм | 0-для симметричных не равно 0 -для несимметричных | Π-связь менее прочная, чем σ-связь, легче поляризуется, склонна к лёгкому разрыву и реакциям присоединения | |
| C-C (sp3) | 0,154 нм |
Физические и химические свойства алкенов
Алкены C2-C4 – газы, C5-C18 – жидкости, далее твёрдые вещества, нерастворимы в воде, но хорошо растворяются в бензоле, эфире, хлороформе.
Для алкенов в первую очередь характерны реакции присоединения, протекающие с разрывом π-связи (реакции ионного присоединения и реакции радикального присоединения). Также возможны реакции радикального замещения атома водорода и реакции окисления. Наиболее разнообразными и важными реакциями являются:
1. Реакции электрофильного присоединения – AdE.
Общая схема реакций электрофильного присоединения:
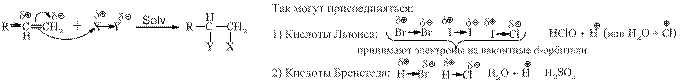
1) Присоединение брома (Br2)
Реакция бромирования протекает легко. Обесцвечивание раствора брома является качественной на двойную связь.
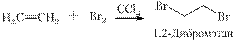
О механизме реакции судят по следующим экспериментальным данным:
а) Реакция ускоряется в полярных растворителях, способных ионизировать связь, т.е. реакция ионная,протекает ступенчато.
б) В присутствии солей NaCl или LiCl или в присутствии воды образуются смешанные продукты:
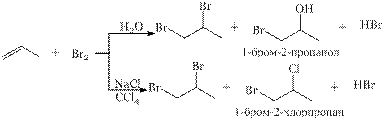
в) Реакция имеет второй порядок по реагентам, т.е. скорость реакции выражается уравнением: V=k[CH2=CH2][Br2] и трактуется, как бимолекулярный, т.е. в медленной стадии реакции участвует субстрат и реагент.
г) Реакция стереоспецифичная и протекает, как транс-присоединение (анти-присоединение), что согласуется со следующим механизмом:
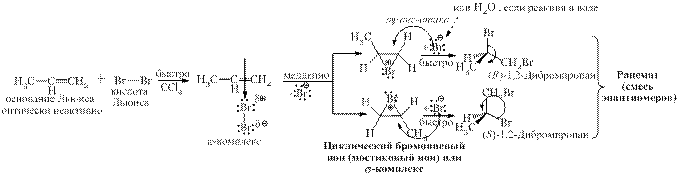
На первой стадии механизма образуется π-комплекс, представляющий собой донорно-акцепторный комплекс (ДАК), где π-орбиталь субстрата частично перекрывается с d-орбиталью брома. Затем этот π-комплекс превращается в циклический бромониевый ион (образуется только при бромироввании), который атакуется анионом брома с противоположенной стороны относительно присоединившегося электрофильного атома брома, в результате чего образуется рацемическая модификация.
Однако в случае циклогексена образуется только один пространственный изомер – транс-изомер, который может существовать в виде пары энантиомеров:
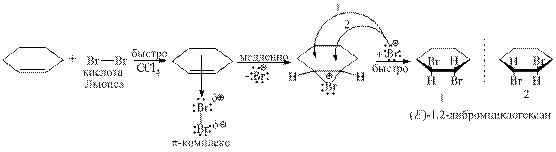
Стереоспецифичная реакция привела к одному геометрическому изомеру, но получился рацемат, т.к. исходное соединение оптически неактивно. Аналогичная ситуация в случае замещённых алкенов, из которых может образоваться соединение с двумя хиральными центрами:
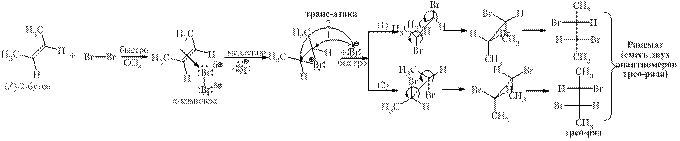
2) Присоединение хлора (Cl2)
Хлор высоко электроотрицательный и малополяризуемая молекула в реакциях электрофильного присоединения, не образует циклического иона, а образуется открытый карбокатион, который неустойчив и реакция приводит к образованию хлоралкена.
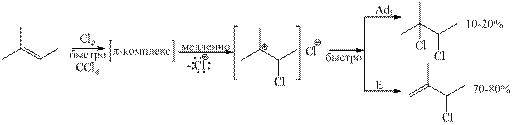
Активность галогенов убывает в ряду: F2>Cl2>Br2>I2
Практическое значение имеет реакция бромирования.
| <== предыдущая страница | | | следующая страница ==> |
| Дегидрогалогенирование галогеналканов | | | Присоединение галогеноводородов (HI, HBr, HCl) |
Дата добавления: 2014-04-05; просмотров: 558; Нарушение авторских прав

Мы поможем в написании ваших работ!