
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Реакции ионного обмена
Реакции обмена между ионами называются реакциями ионного обмена.
Реакции ионного обмена протекают до конца, если в результате реакции образуется осадок, газ или слабый электролит (например, вода).
При составлении ионных уравнений сильные растворимые электролиты записывают в ионной форме, а слабые электролиты, малорастворимые и газообразные вещества – в молекулярной форме. В молекулярной форме записывают также оксиды.
Примеры. 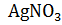 +
+ 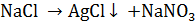 ,
,
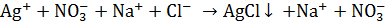 ,
,
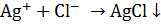 .
.
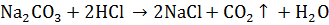 ,
,
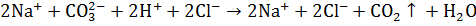 ,
,
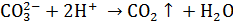 .
.
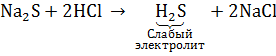 ,
,
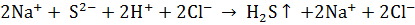 ,
,
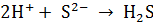 .
.
ЗАКЛЮЧЕНИЕ
Растворы, проводящие электрический ток, получили название растворов электролитов. Они условно разделены на две группы: слабые и сильные электролиты. Слабые электролиты диссоциированы частично и подчиняются закону разбавления Оствальда. Сильные электролиты диссоциированы полностью, для их характеристики вместо концентрации используют активность. Разработана теория разбавленных электролитов, которая позволяет рассчитывать активности ионов, однако теории растворов, охватывающей весь диапазон концентраций, пока не существует.
Равновесие в растворах электролитов смещается в сторону образования слабых электролитов, труднорастворимых и газообразных соединений.
| <== предыдущая страница | | | следующая страница ==> |
| Свойства кислот, оснований и солей с точки зрения теории электролитической диссоциации | | | Семейное право |
Дата добавления: 2014-05-03; просмотров: 278; Нарушение авторских прав

Мы поможем в написании ваших работ!