
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Липиды
|
Читайте также: |
Обучающие упражнения
Задание 1. Привести формулы важнейших высших жирных кислот с учетом индекса кислоты.
| 1.1 олеиновая кислота (18:1) | 1.3 арахидоновая кислота (20:4) |
| 1.2 линолевая кислота (18:2) | 1.4 эйкозапентаеновая кислота (20:5) |
Ответ:формулы высших жирных кислот, входящих в структуру природных липидов, могут быть приведены с учетом сведений, приведенных в табл. 1.
Таблица 1
Высшие жирные кислоты, входящие в состав природных липидов
| N п/п | Историческое (травиальное) название кислоты | Индекс ЖК (кол-во атомов С:количество p-связей) | Семейство ЖК* | Положение p-связей D** |
| Пальмитиновая | 16:0 | |||
| Стеариновая | 18:0 | |||
| Олеиновая | 18:1 | w9 | D9 | |
| Линолевая | 18:2 | w6 | D9,12 | |
| Линоленовая | 18:3 | w3 | D9,12,15 | |
| Арахидоновая | 20:4 | w6 | D5,8,11,14 | |
| Эйкозапентаеновая | 20:5 | w3 | D5,8,11,14,17 | |
| w6 | D2,5,8,11,14 | |||
| Докозапентаеновая | 22:5 | w6 | D4,7,10,13,16 | |
| Докозагексаеновая | 22:6 | w3 | D4,7,10,13,16,19 |
*-w-число атомов углерода в концевой углеводородной цепи после последней p-связи
**-номера углеродных атомов, после которых расположены p-связи
Формула олеиновой кислоты (18:1) может быть изображена
СН3-(СН2)7-СН=СН-(СН2)7-СООН
Формула линолевой кислоты с индексом (18:2)
СН3-(СН2)4-СН=СН-СН2-СН=СН-(СН2)7-СООН
Аналогично изобразить формулы остальных жирных кислот.
Задание 2. Привести структурные формулы линоленовой кислоты семейства w3(омега-3), w6 (омега-6) ряда.
Ответ: символом w обозначается количество углеродных атомов с конца молекулы, после которых начинаются двойные связи. В биологическом отношении наибольшее значение имеют кислоты w3 ряда.
18 17-14 13 12 11 10 9 8 6 2-5 1
СН3-(СН2)4-СН=СН-СН2-СН=СН-СН2-СН=СН-(СН2)4-СООН
линоленовая кислота (18:3 w6) цис-цис-цис-октадекатриен-6,9,12-овая кислота
18 17 16 15 14 13 12 11 10 9 2-8 1
СН3-СН2-СН=СН-СН2-СН=СН-СН2-СН=СН-(СН2)7-СООН
линоленовая (18:3 w3) цис-цис-цис-октадекатриен-9,12,15-овая кислота
Задание 3. Привести формулы p-диастереомеров высших жирных кислот с индексом 18:1 (олеиновой и элаидиновой кислот)
Ответ:
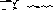
олеиновая кислота (цис-изомер или Z-диастереомер)

элаидиновая кислота (транс-изомер или Е-диастереомер)
Задание 4.Изобразить формулы нейтральных липидов и фосфолипидов по их названию.Написать следующие структурные формулы:
4.1) 2-О-линоленоил-3-О-олеил-1-пальмитоилглицерол
4.2) 2-докозагексаеноил-1-О-миристоил-3-О-олеоилглицерол
4.3) дипальмитоилфосфатидилэтаноламина.
Ответ:названия высших жирных кислот приводятся в алфавитном порядке с указанием их положения у атомов углерода в глицериновом фрагменте молекулы. Символ"О" обозначает замещение у атома кислорода.
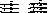
2-О-Линоленоил-3-О- олеоил- 2-докозагексаеноил-1-О-миристоил-
1-О-пальмитоилглицерол 3-О-олеоилглицерол
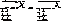
ионизированная форма неионизированная форма
дипальмитоилфосфатидилэтаноламин
Задание 5. Приведите механизм зарождения свободных радикалов.
Ответ: в активном центре гемоглобина в результате переноса электрона от катиона железа к кислороду образуются супероксид-ион радикалы
Fe2+ - e ¾®Fe3+, О2 + е ¾¾¾® О2·
При диспропорционировании супероксид-иона образуется пероксид водорода.
О2 · + О2 · + 2 Н+ ¾¾® Н2О2 + О2
При реакции супероксид-иона и пероксидом водорода образуется гидроксил-радикал.Н2О2 + О2 · ¾¾® 2 ОН· + О2
В реакции супероксид-иона с гидроксил-радикалом образуется синглентный кислород:
ОН· + О2 ·¾¾® *О2(синглентный) + ОН- Образование высокоактивного ОН· радикала происходит также по реакции Фентона: H2O2 + Fe2+¾® Fe3++ OH- + ОН·
Гидроксил-радикал атакует молекулы фосфолипидов (R-Н) - основных структурных компонентах биологических мембран, при этом появляются радикалы нового сорта - алкильные, которые мгновенно присоединяют кислород и превращаются в пероксидные радикалы (RO2·).
R-H + OH· ¾¾® R· + H2O
R· + O2 ¾¾® RO2·
Задание 6. Приведите механизм действия ферментативной антиоксидантной системы.
Ответ: ферменты каталаза и глутатионпероксидаза защищают аэробные клетки от окисления, предотвращая возможность радикального разрушения пероксидов. Субстратом для каталазы преимущественно служит пероксид водорода.
2 Н2О2 ¾¾® 2Н2О + О2
В состав простетической группы каталазы входит гемовое железо, в активном центре происходит окисление (Fe2+ - e ¾® Fe3+).
Глутатионпероксидаза вместе с глутатионом разрушают пероксид водорода и гидропероксиды, защищая клетки от повреждающего действия радикалов, образующихся при гомолитическом разрыве связей RО-ОH.
Глутатион представляет собой трипептид, образованный глутаминовой кислотой, цистеином и глицином :
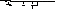
Реакционоспособной группой глутатиона(R-SH)является тиольная группа. Глутатион взаимодействует с пероксидом водорода и гидропероксидами липидов:
2 R-SH + H2O2 ¾® 2 H2O + R-S-S-R
2 R-SH + R1OOH ¾® H2O +R1OH + R-S-S-R
Окисленный глутатион способен восстанавливаться:
R-S-S-R + 2H+ + 2 e 2 R-S-H
Активный центр глутатионпероксидазы содержит остаток селеноцистеина, в котором атом серы цистеина заменен на атом селена: 
Полагают, что действие глутатионовой ферментной системы может быть описано совокупностью реакций:
R-Se-H +H2O2 ¾¾® R-Se-OH + H2O (I)
R-Se-OH + 2 R-S-H ¾¾® R-Se-H + R-S-S-R + H2O (II)
R-S-S-R + НАДФ-Н ¾¾® 2 R-S-H + НАДФ+ (III)
Задание 7. Написать схему реакции пероксидного окисления на примере олеиновой и линолевой кислоты.
Ответ: в молекулах фосфолипидов связи С-Н, расположенные между двумя p-связями (в a-положении к ним), атакуются гидроксильными или пероксильными радикалами. Рассмотрим этот процесс на примере линоленовой кислоты:
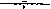
В результате образуются новые радикалы, существующие в двух мезомерных формах:

Радикал стабилизируется за счет делокализации электронной плотности в сопряженной системе: СН3-(СН2)4-СН. . . СН. . . СН. . . СН. . .СН-(СН2)7-СООН
Схематично описанный выше процесс представляется как
RH + OH· ¾® H2O + R· инициирование (0)
Таким образом, инициируется процесс неферментативного окисления липидов биологических мембран.
Образующийся алкильный радикал присоединяет молекулу кислорода (за время 10-6сек) и превращается в очень активный пероксидный (пероксильный) радикал:
R·+ O2 ¾® RО2· рост цепей (1)
Пероксидный радикал RО2· взаимодействует с соседними углеводородными фрагментами молекулы фосфолипидов, что приводит к образованию гидропероксидов (RООН) и новому алкильному радикалу R·, вновь присоединяющему молекулу О2 согласно реакции 1.
RО2· + RH ¾® RООH + R· продолжение цепей (2)
Гидропероксиды способны разрушаться с разрывом О-О связей, что приводит к вторичному иницированию и, как следствие, ускорению окисления:
RООH ¾® RО· + ОН· вырожденное разветвление (3)
Последняя реакция крайне нежелательна для организма. Поэтому существуют ферментативные антиоксидантные системы, регулирующие в организме концентрацию активных кислородсодержащих ионов и радикалов.
Свободные радикалы взаимодействуют между собой, обрывая цепи окисления в соответствии с элементарными реакциями :
RO2·+ RO2· ¾® молекулярные продукты
RO· + RO· ¾® молекулярные продукты
R· + R· ¾¾® молекулярные продукты
Задание 8. Показать механизм действия антиоксидантов
Ответ: в присутствии относительно низких концентраций ингибиторов фенольного типа (IпН) (10-6 - 10-3 моль/л) обрыв цепей происходит на молекулах антиоксидантов согласно реакции:
IпН +RO2·¾¾¾¾®ROOH + Iп· (обрыв цепей) (VII)
Радикал ингибитора (Iп·) обычно неактивен и не участвует в продолжении цепей, в связи с чем антиоксидант выполняет роль ловушки свободных радикалов и способствует значительному торможению окисления.
формула основного липидного антиоксиданта - a-токоферола:
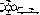
В последние годы антиоксиданты применяются в клинической практике (антиоксидантотерапия).
Задание 9. Показать схему этерификации холестерина (холестерола) с участием фермента фосфатидилхолинхолестеринацетилтрансферазы (ЛХАТ).
Ответ:остатки ненасыщенных и полиненасыщенных высших жирных кислот, входящих в структуру фосфолипидов, например, фосфатидилхолина, этерифицируют -ОН группу холестерина с участием фермента ЛХАТ. При этом образуются эфиры холестерина, в форме которых холестерин выводится из организма.
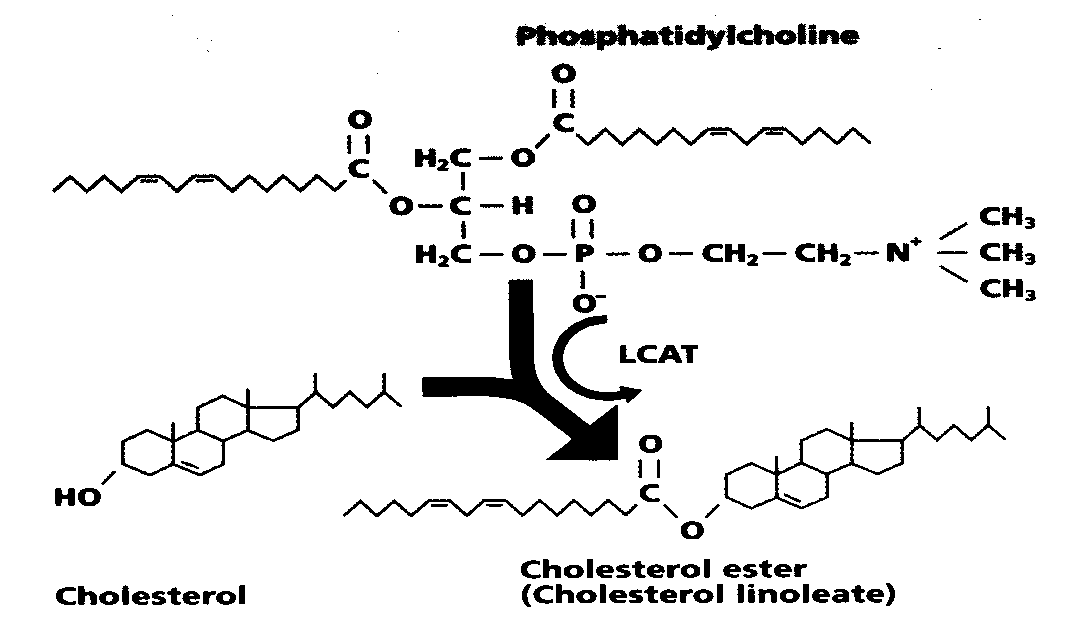
Задания для самостоятельной работы
Задание 1. Привести формулы:
| а) 2-О-линолеил-1-О олеилфосфатидилэтаноламина | б) в)1,2-дистеароил-фосфатидилинозитола |
Задание 2. Напишите ряд формул высших монокарбоновых кислот: олеиновой, линолевой, линоленовой.
Задание 3. Изобразите структуру фосфатидилэтаноламина, включающего пальмитиновую и олеиновую кислоты.
- к нейтральным или полярным липидам относится данное соединение?
- приведите реакцию гидролиза (омыления) липида.
Задание 4. Напишите строение фосфатидилэтаноламина с ацильными остатками линолевой и олеиновой кислот. Приведите реакцию гидролиза фосфатидилэтаноламинов.
Задание 5. Приведите общую формулу фосфатидилхолина. Укажите полярный фрагмент молекулы. Благодаря каким свойствам фосфолипиды являются структурными компонентами биологических мембран.
Задание 6. Напишите формулу1-О-линолеил-2-О-линоленоилфосфатидилхолина. Укажите полярный фрагмент молекулы. Изобразите схему формирования бислойной структуры биологических мембран
Задание 7. Приведите реакцию взаимодействия свободных радикалов с ингибитором процессов окисления (антиоксидантом).
Задание 8. Напишите формулу нейтрального липида триолеилглицерола. Приведите реакцию гидролиза данного соединения в щелочной среде (омыление) и реакцию его восстановления. Назовите продукты.
Задание 9. В состав активного центра фермента глутатионпероксидазы входит глутатион (R-SH), который наряду с ферментом участвует в реакции с пероксидом водорода. Глутатион представляет собой трипептид, образованный глутаминовой кислотой, цистеином и глицином. Изобразите его структуру и приведите химизм реакции глутатиона c пероксидом водорода.
Задание 10.Покажите механизм образования активных форм кислорода (О2·, ОН·, О2*, Н2О2). Приведите реакцию взаимодействия липида (RH) с гидроксильными радикалами (реакция инициирования пероксидного окисления липидов).
Тестовые вопросы
1. Укажите название нейтрального триглицерида:
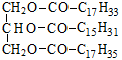
| А) 2-линолеил-1-олеил-3-пальмитоилглицерин; Б) 3-линолеил-2-линоленоил-1-олеилглицерин; В) 1-олеил-2-пальмитоил-3-стеароилглицерин; Г) 3-линолеил-2-пальмитоил-1-стеароилглицерин |
2. Выберите аминоспирт, входящий в структуру полярного липида дипальмитоилфосфатидилхолина:
А) 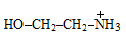
| Б)
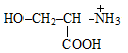
| В) 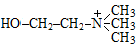
| Г) 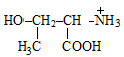
|
3. Какие из представленных карбоновых кислот относятся к эссенциальным высшим жирным кислотам:
А) арахидоновая кислота С19Н31СООН;
Б) масляная кислота С3Н7СООН;
В) пальмитиновая кислота С15Н31СООН;
Г) линоленовая кислота С17Н29СООН
4. Полярный фрагмент молекулы фосфолипида включает:
А) остаток фосфорной кислоты и аминоспирта;
Б) остаток фосфорной кислоты и глицерина;
В) остатки фосфорной и ненасыщенных высших жирных кислот;
Г) остатки аминокислот и насыщенных высших жирных кислот
5. Ненасыщенная высшая жирная кислота принадлежит семейству ряда ω-6 (омега-6) если:
А) в структуре 6 двойных связей;
Б) двойная связь располагается после шестого углеродного атома с дистального (наиболее удаленного от СООН-группы) конца углеводородной цепи;
В) двойная связь располагается после шестого углеродного атома от –СООН-группы;
Г) углеводородная цепь состоит из шести атомов углерода
6. Укажите продукт полного восстановления на платиновом катализаторе 1- линоленоил-3- олеил -2-стеароилглицерина:
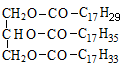
А)
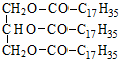
| Б)
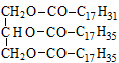
| В)
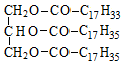
| Г)
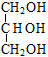
|
7. В результате реакции гидролиза (омыления) липидов образуются:
А) глицерол и соль высшей жирной кислоты (мыло);
Б) этиленгликоль и высшая жирная кислота;
В) холестерин и соль высшей жирной кислоты (мыло);
Г) глицерин и смесь солей высших жирных кислот;
8. Выберите реакцию, приводящую к образованию гидропероксида.
А) RH + OH● → R● + Н2О; Б) О2● + 2OH● → О2* + ОН¯;
В) RH + RO2● → ROOH + R●; Г) О2● + О2● → Н2О2 + О2
9. Какие из представленных соединений наиболее легко подвергаются процессам перекисного окисления:
А) линоленовая кислота; Б) холестерин;
В) олеиновая кислота; Г) стеариновая кислота
10. К ферментам антиоксидантной защиты липидов относятся:
А) глутатионпероксидаза; Б) α-токоферол;
В) β-каротин; Г) каталаза
Название тем рефератов для самостоятельной работы студентов
| № зан. | Название реферата | Вид работы | Форма контроля |
| 1.1.2 | Основы биоэнергетики. Сопряженные биохимические процессы, структура и биологическая роль АТФ. | Реферат | Защита реферата |
| 1.1.2 | Жизнь и деятельность Германа Ивановича Гесса. | Реферат | Защита реферата |
| 1.1.2 | Жизнь и деятельность Джозайя Виларда Гиббса. | Реферат | Защита реферата |
| 1.1.2 | История открытия II начала термодинамики. Работы Рудольфа Клаузиуса, Вильяма Томсона, Людвига Больцмана.. | Реферат | Защита реферата |
| 1.1.3 | Сванте Аррениус и теория электролитической диссоциации. | Реферат | Защита реферата |
| 1.1.3 | Законы растворения газов в биологических жидкостях. Принципы лечения в барокамере. | Презентация | Показ и защита презентации |
| 1.1.4 | Нарушение кислотно-основного равновесия в организме. Компенсированный и некомпенсированный ацидоз и алкалоз. Медикаментозные способы их преодоления. | Реферат | Защита реферата |
| 1.1.4 | Буферные системы организма. Роль и механизм действия бикарбонатной буферной системы. | Реферат | Защита реферата |
| 1.1.5 | Основы фармакокинетики. | Реферат | Защита реферата |
| 1.2.1 | Биологический антагонизм: натрий-калий; кальций-магний. | Реферат | Защита реферата |
| 1.2.1 | Периодическая система химических элементов. Жизнь и деятельность Дмитрия Ивановича Менделеева. | Реферат | Защита реферата |
| 1.2.1 | Натрий-калиевый насос. Биологическая роль. | Реферат | Защита реферата |
| 1.2.1 | Кальций в организме – от младенчества до старости. | Реферат | Защита реферата |
| 1.2.1 | Биологическая роль магния. Антагонизм магния и кальция. | Реферат | Защита реферата |
| 1.2.2 | Транспорт кислорода. Особенности строения гемоглобина. | Реферат | Защита реферата |
| 1.2.2 | Селен. Биологическая роль. Реальность и мифы. | Реферат | Защита реферата |
| 1.2.2 | Роль кремния в организме человека. | Реферат | Защита реферата |
| 1.2.2 | Роль фосфора в организме человека | Реферат | Защита реферата |
| 1.2.2 | Сера. Биологическая роль и применение соединений серы в медицине. | Реферат | Защита реферата |
| 1.2.2 | Биологическая роль оксидов азота, выделяемых эндотелием сосудов. NO-синтаза. Токсичность оксидов азота. | Реферат | Защита реферата |
| 1.2.2 | Кислотные дожди. Экологические аспекты выделения оксидов серы и азота в атмосферу. | Реферат | Защита реферата |
| 1.2.2 | Активные формы кислорода. Действие на организм. Ферментативная и антиоксидантная защита. | Реферат | Защита реферата |
| 1.2.2 | Галогены и галогениды. Положительное и отрицательное воздействие на организм. | Реферат | Защита реферата |
| 1.2.2 | Эндемические заболевания. Профилактика и лечение. | Реферат | Защита реферата |
| 1.2.3 | Цинк. Гипотеза о цинке как панацее – подтверждается. | Реферат | Защита реферата |
| 1.2.3 | Тяжелые металлы. Механизмы токсического действия тяжелых металлов на организм человека. | Реферат | Защита реферата |
| 1.2.3 | Внутрикомплексные соединения, структура, свойства. Хелатотерапия. | Реферат | Защита реферата |
| 1.2.3 | Железо, медь и кобальт в процессе кроветворения. Норма и патология. | Реферат | Защита реферата |
| 1.2.3 | Марганец и хром. Биологическая роль., нормы потребления. Пищевые источники микроэлементов. | Реферат | Защита реферата |
| 1.2.3 | Голубая кровь как искусственный носитель кислорода. История открытия и применения перфторанов в медицине (кровезаменители перфторан, перфукол). | Реферат | Защита реферата |
| 1.2.3 | Золото в медицине. От древней Эллады до современности. | Реферат | Защита реферата |
| 1.2.3 | Соединения платины и онкозаболевания. | Реферат | Защита реферата |
| 1.2.3 | Роль меди в организме человека. Синергизм цинка, железа и меди. | Реферат | Защита реферата |
| 1.2.4 | Адсорбция. Виды адсорбционной терапии. | Реферат | Защита реферата |
| 1.2.5 | Диализ. Искусственная почка, функции и перспектива. | Презентация | Показ и защита презентации |
| 1.2.5 | Мицеллообразование. Явление солюбилизации в медицине и фармации. | Реферат | Защита реферата |
| 1.2.5 | Применение ПАВ в хирургии. Строение ПАВ. Механизм действия. | Реферат | Защита реферата |
| 1.2.5 | Электрокинетические свойства дисперсных систем. Электрофорез в медицине. | Реферат | Защита реферата |
| 1.2.5 | Явления коагуляции, коллоидной защиты и пептизации в живом организме. | Реферат | Защита реферата |
| 1.3.7 | Полиненасыщенные жирные кислоты семейства «омега-3». Биологическая роль | Реферат | Защита реферата |
| 1.3.7 | Реакции свободно радикального окисления липидов (ПОЛ). Значение реакций ПОЛ в развитии патологии. Роль природных антиоксидантов. | Реферат | Защита реферата |
| <== предыдущая страница | | | следующая страница ==> |
| Нуклеиновые кислоты | | | ОСОБЕННОСТИ УХОДА ЗА ЗДОРОВЫМИ И БОЛЬНЫМИ ДЕТЬМИ |
Дата добавления: 2014-09-10; просмотров: 1246; Нарушение авторских прав

Мы поможем в написании ваших работ!