
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Металлопротеины
К металлопротеинам относят биополимеры, которые, помимо белка, содержат простетическую группу (компонент небелкового характера), включающую ионы металлов.
Отдельную группу металлопротеинов составляют гемопро-теины, содержащие в качестве простетической группы соединения железа. Одним из важнейших гемопротеинов является гемоглобин. Он состоит из белка (глобина) и комплекса железа с порфирином (гема). В геме ион Fe2+ (комплексообразователь), связан с двумя атомами азота, принадлежащими порфириновому кольцу, ковалентной связью, а еще с двумя - координационной. Координа-ционное число Fe2+ равно шести: в порфириновом комплексе пятое координационное место занимает гистидиновая группа белка, образуя координационую связь атома азота с Fe2+. В отсутствие кислорода шестым лигандом является вода. В случае, когда вода замещается на кислород, образуется оксигемоглобин. Кроме воды и кислорода ион Fe2+ может связывать и некоторые другие лиганды, например, СО, CN- и оксиды азота. Так, с молекулами угарного газа гемоглобин образует карбоксигемоглобин, а с оксидами азота - метгемоглобин, содержащий ионы Fe3+. Накопление этих видов гемоглобина в крови приводит к снижению снабжения тканей кровью.
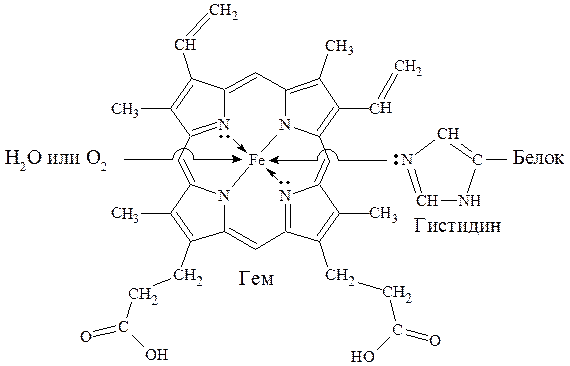
Схема образования связей в гемоглобине
Гем в виде гем-порфирина является простетической группой производных гемоглобина: миоглобина, каталазы, пероксидазыи цитохромов.
Отличительной особенностью гемоглобина (миоглобина) являет-ся постоянство степени окисления железа Fe2+. Равновесие:
О2 + гемоглобин ⇄ оксигемоглобин
в легких смещено вправо, а в клетках – влево.
Таким образом, гемоглобин (миоглобин) является переносчиком молекул (Н2О, О2).
Транспортные функции выполняют и цитохромы,в которых связь между гемом и полипептидной цепью осуществляется при помощи остатков цистеина белковой цепи.
Однако, в отличие от гемоглобина и миоглобина, механизм их действия основан на изменении степени окисления железа:
Fe2+ - 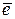
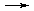 Fe3+,
Fe3+,
Fe3+ + 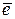
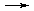 Fe2+.
Fe2+.
Передавая электроны от цитохрома b к цитохромооксидазе, ионы железа участвуют в процессе окислительного фосфорилирования.
С кислородом и СО цитохромы не взаимодействуют.
| <== предыдущая страница | | | следующая страница ==> |
| Комплексонометрия | | | Витамины |
Дата добавления: 2015-06-30; просмотров: 278; Нарушение авторских прав

Мы поможем в написании ваших работ!