
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Теория валентных связей
С 33. Теория валентных связей была первой из квантовомеханических теорий, использованной для приближенного объяснения характера химических связей в КС. В основе ее применения лежала идея о донорно-акцепторном механизме образования ковалентных связей между лигандом и комплексообразователем.
1) Лиганд считается донорной частицей, способной передать пару электронов акцептору – комплексообразователю, предоставляющему для образования связи свободные квантовые ячейки (АО) своих энергетических уровней.
2) Для образования ковалентных связей между комплексообразователем и лигандами необходимо, чтобы вакантные s-, p- или d-атомные орбитали комплексообразователя подверглись гибридизации определенного типа. Гибридные орбитали занимают в пространстве определенное положение, причем их число соответствует КЧ комплексообразователя.
3) При этом часто происходит объединение неспаренных электронов комплексообразователя в пары, что позволяет высвободить некоторое число квантовых ячеек – АО, которые затем участвуют в гибридизации и образовании химических связей.
4) Неподеленные пары электронов НЭП лигандов взаимодействуют с гибридными орбиталями комплексообразователя, и происходит перекрываниесоответствующих орбиталей комплексообразователя и лиганда с появлением в межъядерном пространстве повышенной электронной плотности. Электронные пары комплексообразователя, в свою очередь, взаимодействуют с вакантными АО лиганда,упрочняя связь по дативному механизму. Таким образом, химическая связь в комплексных соединениях является обычной ковалентнойсвязью, достаточной прочной и энергетически выгодной.
С 34. Электронные пары, находящиеся на гибридных орбиталях комплексообразователя, стремятся занять в пространстве такое положение, при котором их взаимное отталкивание будет минимально. Это приводит к тому, что структура комплексных ионов и молекул оказывается в определенной зависимости от типа гибридизации.
Рассмотрим образование некоторых комплексов с позиций ТВС. Прежде всего отметим, что валентные орбитали атомов комплексообразователей близки по энергии:
E(n-1)d » Ens » Enp » End
| Тип гибридизации | КЧ | Геометрия комплекса | Примеры |
| sp | линейная | [Ag(CN)2]- [Cu(NH3)2]+ | |
| sp2 | треугольная | [HgI3]- | |
| sp3 | тетраэдр | [Be(OH)4]2- [MnCl4]2- [Zn(NH3)4]2+ | |
| dsp2 | квадрат | [Ni(CN)4]2- [PtCl4]2- [Pt(NH3)2Cl2]0 | |
| sp3d(z2) | тригональная бипирамида | [Fe(CO)5] | |
| sp3d(x2-y2) | квадратная пирамида | [MnCl5]3- [Ni(CN)5]3- | |
| sp3d2, d2sp3 | октаэдр | [Al(H2O)6]3+ [SnCl6]2- [Co(NH3)6]3+ [Fe(CN)6]3- | |
| sp3d3 | пентагональная бипирамида | [V(CN)7]4- [ZrF7]3- |
●С 34. Например, катион [Zn(NH3)4]2+ включает комплексообразователь цинк(II). Электронная оболочка ионаZn2+ имеет формулу [Ar] 3d10 4s0 4p0 и может быть условно изображена так:

Вакантные 4s- и 4p-орбитали атома цинка(II) образуют четыре sp3-гибридные орбитали, ориентированные к вершинам тетраэдра.
Каждая молекула аммиака имеет НЭП у атома азота. Орбитали атомов азота, содержащие НЭП, перекрываются с sp3-гибридными орбиталями цинка(II), образуя тетраэдрический комплексный катион тетраамминцинка(II) [Zn(NH3)4]2+:
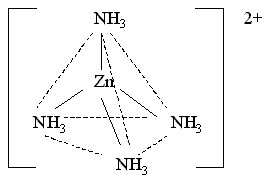
Поскольку в ионе [Zn(NH3)4]2+ нет неспаренных электронов, то он проявляет диамагнитные свойства.
●Тетрахлороманганат(II)-ион [MnCl4]2- содержит пять неспаренных электронов на 3d-орбиталях и вакантные 4s- и 4p-орбитали. Вакантные орбитали образуют sp3-гибридные орбитали, которые перекрываются с p-атомными орбиталями хлорид-ионов:

Полученный таким образом тетраэдрический ион [MnCl4]2- является парамагнитным, так как содержит пять неспаренных электронов.
| <== предыдущая страница | | | следующая страница ==> |
| Примеры образования и разрушения комплексов | | | Гибридизация орбиталей и структура комплексов |
Дата добавления: 2015-06-30; просмотров: 175; Нарушение авторских прав

Мы поможем в написании ваших работ!