
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Контрольная работа 1. 1. В каких случаях возможно самопроизвольное протекание химической реакции, если принять ½DH°½<< ½TDS°½?
Химическая термодинамика. Химическая кинетика и равновесие
Вариант 9
1. В каких случаях возможно самопроизвольное протекание химической реакции, если принять ½DH°½<< ½TDS°½?
2. Тепловой эффект реакции:
SO2 (г) + 2H2S (г) ® 3S (ромб) + 2Н2О (ж)
равен –234,50 кДж. Определите стандартную теплоту образования H2S.
3. Используя значения ΔfG˚298 соединений, участвующих в реакции:
C6H6 (ж) + NH3 (г) ® С6Н5NH2 (ж) + Н2 (г),
определите, возможна ли эта реакция, ΔfG˚298 (С6Н5NH2 ж) = 149,08 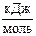 .
.
4. Выведите уравнение константы химического равновесия для реакции:
MgO (кр) + СО2 (г) « MgCO3 (кр); DrH° < 0.
Какими способами можно сместить химическое равновесие этой системы влево?
5. При 398 К реакция заканчивается за 18 мин. Через сколько времени эта реакция закончится при 453 К, если температурный коэффициент скорости реакции равен 3?
6. Равновесие реакции: H2 (г) + Cl2 (г) « 2НCl (г) установилось при следующих концентрациях участвующих в ней веществ: (  ): [Н2] = 0,25; [Cl2] = 0,05; [HCl] = 0,9. Определите исходные концентрации хлора и водорода.
): [Н2] = 0,25; [Cl2] = 0,05; [HCl] = 0,9. Определите исходные концентрации хлора и водорода.
| <== предыдущая страница | | | следующая страница ==> |
| Контрольная работа 1 | | | Контрольная работа 1. 1. Уменьшится или увеличится энтропия при переходе водяного пара в жидкость, кристаллического йода в парообразное состояние? |
Дата добавления: 2015-06-30; просмотров: 141; Нарушение авторских прав

Мы поможем в написании ваших работ!