
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Опыт 1. Определение устойчивости комплексного иона
В одну пробирку внесите 5-6 капель раствора хлорида железа (III) и добавьте 2-3 капли роданида калия. Напишите уравнения реакции в молекулярной и ионной формах, координационное число (к.ч.) комплексообразователя равно 2. Составьте выражение константы нестойкости, выпишите численное значение Кн из справочника.
Во вторую пробирку внесите 5-6 капель гексацианоферрата(III) калия (красная кровяная соль) и добавьте 2-3 капли роданида калия. Объясните, почему в этом случае не образуется комплекс кроваво-красного цвета, как в первой пробирке, для этого составьте выражение константы нестойкости комплексного иона гексацианоферрата(III) калия, выпишите численное значение Кн из справочника. Сравните Кн комплексов в двух пробирках.
Опыт 2. Получение амино-комплекса меди
В пробирку внесите 10 капель сульфата меди и 1-2 капли гидроксида аммония, образовавшийся голубой осадок растворите в избытке гидроксида аммония до образования комплексного соединения ярко- фиолетового цвета. Составьте уравнения реакций в молекулярном и ионном виде, учитывая, что лигандом являются молекулы аммиака NH3 . Назовите комплексное соединение.
Опыт 3. Образование гидроксокомплексов алюминия
С помощью обменной реакции получите осадок гидроксида алюминия, взяв 1мл соли алюминия. Разделите осадок на 2 пробирки. Исследуйте кислотно-основные свойства гидроксида алюминия, растворив осадок в первой пробирке в серной кислоте, а осадок во второй пробирке - в щелочи. Напишите уравнения реакций в молекулярном и ионном виде. Напишите названия полученных соединений. В полученном комплексном соединении к.ч. комплексообразователя равно 4.
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ
1. Какое выражение соответствует константе нестойкости комплексного иона в соединении Na3[Co(NO2)6]?
1) 
| 4) 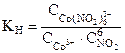
|
2) 
| 5) 
|
3) 
|
2. В каком соединении степень окисления комплексообразователя наименьшая?
| 1) [Cu(NH3)4]SO4 | 4) [Ag(NH3)2]Cl |
| 2) [Ni(NH3)6]Cl2 | 5) [Co(NH3)4]Cl2 |
| 3) [Hg(NH3)4](NO3)2 |
3. Чему равно координационное число комплексообразователя в соединении [Co(NH3)2(H2O)4]Cl3 ?
| 1) 9 | 2) 6 | 3) 2 | 4) 4 | 5) 7 |
4. Указать формулу гексацианоферрат (II) калия.
| 1) K3[Fe(CN)6] | 4) K2[Pt(CN)4] |
| 2) K4[Ni(CN)6] | 5) K4[Fe(CN)6] |
| 3) K3[Co(CN)6] |
5. Сравнив константы нестойкости, указать самый нестойкий ион.
1) 
| 4) 
|
2) 
| 5) 
|
3) 
|
Таблица
Константы нестойкости Кн некоторых комплексных ионов при температуре 298 К
| Ион | Кн | Ион | Кн |
| 1.Комплексы с аммиаком | 
| 1,55 · 10 – 12 | |

| 6,30 · 10 – 4 | 
| 2,04 · 10 – 22 |

| 9,31 · 10 – 8 | 
| 5,00 · 10 – 11 |

| 7,56 · 10 – 8 | 
| 2,50 · 10 – 5 |
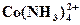
| 2,80 · 10 – 6 | 
| 5,00 · 10 – 13 |

| 7,75 · 10 – 6 | 
| 0,15 |

| 3,10 · 10 – 33 | 
| 4,00 · 10 – 5 |

| 2,14 · 10 – 13 | 
| 3,60 · 10 – 16 |

| 1,35 · 10 – 11 | 4.Йодидные комплексы | |

| 5,30 · 10 – 20 | 
| 1,80 · 10 – 14 |

| 10,90 | 
| 3,10 · 10 – 12 |

| 1,12 · 10 – 8 | 
| 8,00 · 10 – 7 |

| 1,86 · 10 – 9 | 
| 1,75 · 10 – 9 |

| 3,46 · 10 – 10 | 
| 1,48 · 10 – 30 |
| 2.Бромидные комплексы | 
| 1,42 · 10 – 4 | |

| 7,80 · 10 – 8 | 5.Роданидные комплексы | |

| 4,00 · 10 – 13 | 
| 2,70 · 10 – 8 |

| 1,50 · 10 – 8 | 
| 1,00 · 10 – 23 |
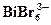
| 2,00 · 10 – 10 | 
| 1,00 · 10 – 42 |

| 2,00 · 10 – 4 | 
| 3,93 · 10 – 4 |

| 1,30 · 10 – 6 | 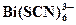
| 5,93 · 10 – 5 |

| 1,00 · 10 – 21 | 
| 1,67 · 10 – 2 |

| 1,00 · 10 – 3 | 
| 7,83 · 10 –13 |

| 3,00 · 10 – 21 | 
| 4,40 · 10 – 4 |
| 3.Гидроксокомплексы | 
| 5,90· 10 – 22 | |

| 1,38 · 10 – 9 | 
| 6,70 · 10 – 2 |

| 3,30 · 10 – 8 | 
| 2,40 · 10 – 2 |
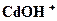
| 1,00 · 10 – 5 | 6.Сульфатные комплексы | |

| 4,00 · 10 – 5 | 
| 0,59 |

| 1,20 · 10 – 10 | 
| 0,59 |

| 3,40 · 10 – 7 | 
| 6,80 · 10 – 5 |

| 7,60 · 10 – 17 | 
| 1,05 · 10 – 3 |

| 1,30 · 10 – 4 | ||
| Ион | Кн | Ион | Кн |
| 7.Фторидные комплексы | 
| 1,00 · 10 – 16 | |

| 1,80 · 10 – 18 | 
| 4,00 · 10 – 19 |

| 1,44 · 10 – 20 | 9.Цианидные комплексы | |

| 5,00 · 10 – 10 | 
| 8,00 · 10 – 22 |

| 7,60 · 10 – 17 | 
| 2,10 · 10 – 21 |
| 8.Хлоридные комплексы | 
| 5,00 · 10 – 39 | |

| 1,76 · 10 – 5 | 
| 1,41 · 10 – 19 |

| 5,00 · 10 – 22 | 
| 1,00 · 10 – 24 |

| 1,70 · 10 – 4 | 
| 5,00 · 10 – 31 |

| 3,80 · 10 – 7 | 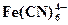
| 1,00 · 10 – 24 |

| 9,30 · 10 – 3 | 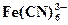
| 1,00 · 10 – 31 |

| 8,50 · 10 – 16 | 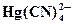
| 4,00 · 10 – 42 |

| 7,10 · 10 – 3 | 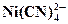
| 1,80 · 10 – 14 |

| 6,00 · 10 – 14 | 
| 1,30 · 10 – 17 |
| <== предыдущая страница | | | следующая страница ==> |
| ТЕОРЕТИЧЕСКАЯ ЧАСТЬ. Соединения сложного состава, в которых можно выделить центральный атом и непосредственно связанные с ним молекулы или ионы называются комплексными или | | | Общие понятия токсикокинетики |
Дата добавления: 2015-06-30; просмотров: 279; Нарушение авторских прав

Мы поможем в написании ваших работ!