
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Метод Фаянса. Метод основан на прямом титровании галогенидов стандартным раствором AgNO3 в присутствии адсорбционных индикаторов
Метод основан на прямом титровании галогенидов стандартным раствором AgNO3 в присутствии адсорбционных индикаторов.
Адсорбционными индикаторами называют соединения, которые при адсорбции на поверхности осадка изменяют свой цвет.
Например, при титровании хлорида натрия нитратом серебра
NaCl + AgNO3 = AgCl ¯ + NaNO3
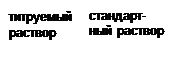
| До точки эквивалентности На осадке будут адсорбироваться ионы Cl-. Коллоидная частица заряжена отрицательно. Для нейтрализации отрицательного заряда к частицам осадка из раствора будут притягиваться положительно заряженные ионы Na+ из раствора. Адсорбция ионов Cl- наблюдается до тех пор, пока находятся свободные ионы Cl-. |
|
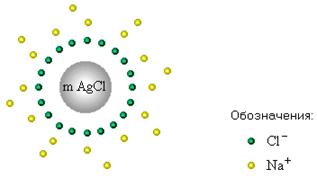
| Индикатор при избытке ионов Cl- не изменяет окраски, т.к. ионы Jnd2- отрицательно заряжены и, следовательно, не адсорбируются коллоидными частицами. | |
| Точка эквивалентности Коллоидная частица заряжена нейтрально. | 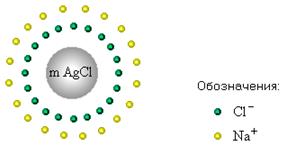
|
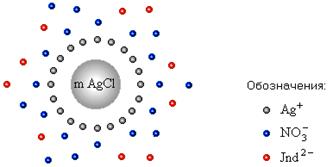
| Одна избыточная капля AgNO3 После точки эквивалентности от прибавления избытка одной капли AgNO3 на осадке будут адсорбироваться избыточные ионы Ag+, которые заряжают коллоидную частицу положительно. Для нейтрализации положительного заряда к частицам осадка из раствора будут притягиваться отрицательные ионы, в том числе и ионы индикатора. Анионы некоторых красителей, адсорбируясь, изменяют свой цвет. |
|
Адсорбционные индикаторы вызывают изменение окраски не в растворе, а на поверхности коллоидного осадка, несущего положительный заряд.
Титрование хлоридов с индикатором флуоресцеином проводят в нейтральной или слабощелочной среде при рН = 7 - 10, т.к. индикатор является слабой кислотой (Кg = 10-8), имеющей в растворе желто-зеленую окраску, а в точке эквивалентности окрашивает осадок в красный цвет.
Эозин является более сильной кислотой (Кg = 10-2). Успешно применяется для титрования бромидов, иодидов и роданидов при рН = 2. Ионы эозина имеют в растворе розовую окраску, а в точке эквивалентности окрашивают осадок в красно-фиолетовый цвет.
Адсорбция представляет собой обратимый процесс. При титровании концентрация определяемого иона в растворе постепенно понижается, равновесие нарушается и адсорбированные ионы переходят с поверхности осадка в раствор. Поэтому результат анализа окажется неточным.
Следовательно, титрование надо заканчивать очень медленно, энергично встряхивая содержимое колбы после прибавления каждой капли титруемого раствора, что способствует более быстрому установлению адсорбционного равновесия.
Адсорбционную ошибку можно уменьшить, если выдерживать осадок при нагревании в маточном растворе. При этом происходит уменьшение поверхности осадка, "старение" осадка. Адсорбция уменьшается настолько, что не влияет на результат анализа. Кроме этого, введение в раствор многозарядных ионов также препятствует адсорбции одноименных с осадком ионов и позволяет получить точные результаты анализа.
Титрование с адсорбционными индикаторами характеризуется высокой точностью и надежностью.
| <== предыдущая страница | | | следующая страница ==> |
| Условия титрования по методу Мора | | | Определение Ag в серебряном сплаве |
Дата добавления: 2015-07-26; просмотров: 203; Нарушение авторских прав

Мы поможем в написании ваших работ!