
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Опыт 8. Определение электрохимического эквивалента меди
Перед погружением в раствор сульфата меди медный электрод зачистите наждачной бумагой, погрузите на 2-3 с в концентрированную азотную кислоту, промойте водой, высушите и взвесьте с точностью до 0,01 г.
Подготовленный катод и медный анод опустите в электролизер и проведите электролиз при определенной силе тока и в течении нескольких минут (точное время и заданную силу тока указывает преподаватель).
По окончании опыта катод промойте водой, высушите и взвесьте. По результатам взвешивания определите массу осажденной меди:
m = m2 – m1,
где:
m – масса осажденной меди, г;
m2 – масса катода после электролиза;
m1 – масса катода до электролиза.
Вычисление электрохимического эквивалента меди проведите на основе 1 закона Фарадея:
 ,
,
где:
k – электрохимический эквивалент;
I - сила тока, А;
t - продолжительность электролиза, с.
Определите ошибку опыта:
kтеор. – kэкперим. = D - абсолютная ошибка опыта.
 - относительная ошибка опыта.
- относительная ошибка опыта.
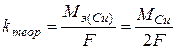 ,
,
Полученные результаты занесите в таблицу:
| Масса катода, г | Масса осажденной меди | kэксперим. | kтеор. | Абсол. ошибка | Относ. ошибка | |
| до электролиза | после электролиза | |||||
| <== предыдущая страница | | | следующая страница ==> |
| Опыт 1. Электролиз водного раствора хлорида натрия | | | Требования к отчету. Отчет должен быть оформлен аккуратно, грамотно и в срок |
Дата добавления: 2015-07-26; просмотров: 137; Нарушение авторских прав

Мы поможем в написании ваших работ!