
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Керамика на основе диоксида циркония
Особенностью диоксида циркония является его полиморфизм. Чистый ZrO2 при комнатной температуре находится в моноклинной фазе и при нагреве испытывает фазовые превращения (рис.4).
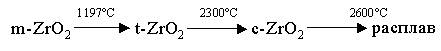
Рис.4. Схема фазовых переходов в чистом диоксиде циркония: m-, t-, c-ZrO2 – моноклинная, тетрагональная, кубическая модификации ZrO2, соответственно
Переход t-ZrO2↔c-ZrO2 имеет диффузионную природу и играет очень важную роль при производстве так называемого частично стабилизированного диоксида циркония. Превращение m-ZrO2↔t-ZrO2 протекает по мартенситному механизму и сопровождается объемными изменениями 5–9%. Такое значительное расширение материала при охлаждении, сопровождающееся растрескиванием, не позволяет получать компактные изделия из чистого ZrO2. По этой причине практическое значение имеют только твердые растворы различных оксидов на основе ZrO2 либо механические смеси с жесткой матрицей, способной стабилизировать высокотемпературные фазы ZrO2 при низкой температуре.
Установлено, что ZrO2 способен образовывать твердые растворы типа замещения со многими двух-, трех- и четырехвалентными оксидами. Общим и весьма важным для керамической технологии свойством этих растворов является отсутствие обратимых полиморфных превращений типа m-ZrO2↔t-ZrO2 - перехода в чистом ZrO2. Хотя образующиеся твердые растворы не являются термодинамически равновесными при низких температурах, практически они могут существовать при этих температурах, не подвергаясь распаду. К настоящему времени механизмы стабилизации ZrO2 путем образования твердых растворов изучены достаточно полно.
По Паулингу, предел устойчивости структуры типа флюорита CaF2, которая соответствует c-ZrO2, определяется соотношением радиусов катиона и аниона rк/ra=0,732. В решетке c-ZrO2 соотношение rк/ra=0,66, т.е ионы кислорода находятся в стесненном состоянии. Поэтому c-ZrO2 существует только при очень высоких температурах, когда значительны тепловые колебания кристаллической решетки. При снижении температуры происходит диффузионный переход c-ZrO2→t-ZrO2. Тетрагональный ZrO2 также имеет структуру типа флюорита. При дальнейшем снижении температуры, когда диффузия практически прекращается, а стесненность ионов кислорода увеличивается, происходит мартенситное превращение t-ZrO2→ m-ZrO2.
Расширение кислородной позиции, способствующее созданию устойчивой флюоритовой структуры в широком интервале температур, может быть достигнуто либо замещением части ионов Zr4+ на ионы большего радиуса (Ce4+, Th4+), либо созданием вакансий в анионной подрешетке путем замещения Zr4+ ионами меньшей валентности (Mg2+, Ca2+, Y3+, Sc3+). Малые размеры ионного радиуса, например 0,78Ǻ для Mg2+, менее благоприятны для устойчивости таких твердых растворов. При стабилизации ZrO2 оксидами магния и кальция ион Mg2+( Ca2+) занимает место Zr4+ в катионной подрешетке, неся в нее отрицательный заряд 2-. Одновременно в анионной подрешетке образуется кислородная вакансия, имеющая положительный заряд 2+. Примесный ион и вакансия притягиваются друг к другу, образуя достаточно устойчивый комплекс (Mg''ZrV''o). Если оксидом-стабилизатором является Y2O3, то для создания одной кислородной вакансии необходимо ввести два иона Y3+ в катионную подрешетку. В этом случае образуется сложный комплекс (Y'ZrV''oY'Zr), в котором два иона иттрия связаны с одной кислородной вакансией. Подобные комплексы при механическом нагружении материала могут вести к неупругой релаксации посредством диффузии в энергетически выгодные позиции и к дополнительной устойчивости флюоритовой структуры. Следует отметить, что не все вакансии в анионной подрешетке связаны с примесными ионами в подобные комплексы и также сами комплексы при повышенных температурах становятся неустойчивыми. Поэтому циркониевые керамики отличаются от других тугоплавких окислов хорошей ионной проводимостью, которая реализуется путем перескакивания ионов кислорода в несвязанные вакансии. При повышении температуры число несвязанных вакансий резко увеличивается и проводимость повышается. Этот факт нашел широкое практическое применение, в частности при изготовлении электронагревателей и твердых электролитов на основе ZrO2.
Таким образом, оптимальные условия стабилизации ZrO2 соответствуют сочетанию трехвалентности вводимого катиона и достаточной близости его радиуса с радиусом Zr4+(0,87Ǻ). Это положение оправдывается на примере стабилизации ZrO2 оксидом иттрия (Y3+, 1,06Ǻ) и оксидами РЗМ. Помимо достижения устойчивости флюоритовой структуры, добавки Y2O3 и CeO2 устойчивы к испарению и позволяют значительно расширить область гомогенности тетрагонального твердого раствора ZrO2, что делает возможным получение спеченной керамики, имеющей в своем составе более 90% t-ZrO2, которая является наиболее перспективной из всех циркониевых керамик.
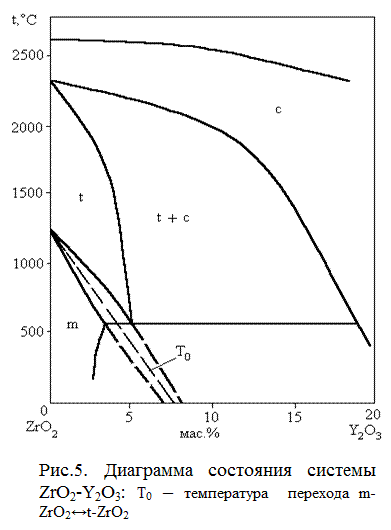 На рис.5 приведена равновесная диаграмма состояния системы ZrO2-Y2O3. Следует отметить, что практически соотношение фаз, соответствующее приведенной диаграмме, не реализуется вследствие очень низкой диффузии ионов Zr4+, Y3+, О2-. Высокотемпературные фазы при определенных добавках Y2O3 и режимах охлаждения могут существовать при низких температурах без распада. Линия Т0 представляет собой геометрическое место температур, при которых свободные энергии m-ZrO2 и t-ZrO2 одинаковы. Приведенные интервалы температур весьма условны и очень сильно зависят от скорости охлаждения твердого раствора и размера зерна.
На рис.5 приведена равновесная диаграмма состояния системы ZrO2-Y2O3. Следует отметить, что практически соотношение фаз, соответствующее приведенной диаграмме, не реализуется вследствие очень низкой диффузии ионов Zr4+, Y3+, О2-. Высокотемпературные фазы при определенных добавках Y2O3 и режимах охлаждения могут существовать при низких температурах без распада. Линия Т0 представляет собой геометрическое место температур, при которых свободные энергии m-ZrO2 и t-ZrO2 одинаковы. Приведенные интервалы температур весьма условны и очень сильно зависят от скорости охлаждения твердого раствора и размера зерна.
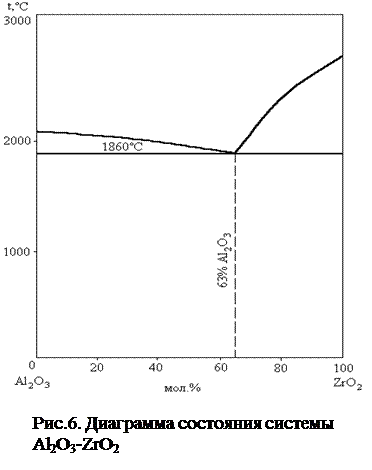
Помимо образования твердых растворов на основе ZrO2 в производстве высокопрочных керамик используется другой способ стабилизации высокотемпературной модификации t-ZrO2. После спекания механической смеси Al2O3-ZrO2 (рис.6.) с объемным содержанием ZrO2 менее 20% образуется жесткая корундовая матрица, удерживающая дисперсные включения t-ZrO2. Это обусловлено высоким модулем упругости корунда меньшим по сравнению с ZrO2 тепловым расширением, вследствие чего частицы t-ZrO2 находятся в поле сжимающих напряжений и остаются стабильными после охлаждения спеченного материала. Стабильность частиц t-ZrO2 зависит также от их размера: нелегированные зерна t-ZrO2 в корундовой матрице превращаются в m-ZrO2 при 20°С, если их размер превышает 0,6мкм. Более крупные зерна превращаются при повышенных температурах по сравнению с мелкими.
 Кроме корундовой матрицы возможно использование других материалов, например нитрида кремния, муллита, MgO, но максимальный прочностной эффект показывает система 85% Al2O3-15% ZrO2. Очень важным здесь является практически полное отсутствие взаимной растворимости компонентов, что исключает появление в материале промежуточных нежелательных фаз.
Кроме корундовой матрицы возможно использование других материалов, например нитрида кремния, муллита, MgO, но максимальный прочностной эффект показывает система 85% Al2O3-15% ZrO2. Очень важным здесь является практически полное отсутствие взаимной растворимости компонентов, что исключает появление в материале промежуточных нежелательных фаз.
Возможность получения высокопрочной циркониевой керамики связана с открытием так называемого эффекта трансформационного упрочнения за счет контролируемого фазового перехода t-ZrO2→m-ZrO2. Сущность этого эффекта вытекает из явления полиморфизма ZrO2, возможности стабилизации высокотемпературных t- и c-фаз и мартенситного характера t→m - перехода. Практически эффект трансформационного упрочнения реализуется в том случае, когда спеченный материал имеет в своем составе частицы t-ZrO2, способные превращаться в m-ZrO2. Возникающие при нагружении трещины распространяются в материале до тех пор, пока в их фронте не оказываются частицы t-ZrO2. Такая частица, находящаяся в сжатом (в корундовой матрице) или в когерентносвязанном с матрицей (при преобладании в составе материала c-ZrO2) состоянии устойчива к t→m - переходу даже при низких температурах. Попав в поле напряжений в вершине распространяющейся трещины, частица получает энергию, достаточную для превращения. Таким образом, энергия распространяющейся трещины переходит в энергию t→m - перехода и катастрофический рост трещины прекращается.
С открытием упрочняющего воздействия фазового t→m - перехода циркониевые керамики являются предметом многочисленных исследований. Циркониевые керамики из-за своей способности образовывать путем добавок различных оксидов и применяемых режимов выдержки при спекании и отжига часто обозначаются как «керамические стали». Ниже представлены основные классы циркониевых керамик, их прочностные характеристики и сферы практического применения.
1. Стабилизированный диоксид циркония CSZ (Cubic Stabilized Zirconia, рис.7,а): кубический твердый раствор на основе ZrO2. Для реализации этого материала количество добавки MgO, CaO должно быть более 15–20мол.%, Y2O3 – более 10мол.%. CSZ имеет низкие прочностные характеристики: σизг не более 250МПа и К1с до 3МПаּм0,5 и находит применение как огнеупорный материал, а также в технологии твердых электролитов.
2. Керамика, упрочненная диоксидом циркония ZTC (Zirconia Toughened Ceramic): дисперсные частицы t-ZrO2 распределены в керамической матрице и стабилизируются сжимающими напряжениями. Наибольшее техническое значение имеют композиции Al2O3-ZrO2 (ZTA: Zirconia Toughened Alumina, рис.7,б), которые используются, прежде всего, как инструментальные материалы. Оптимальные механические характеристики достигаются при содержании ZrO2 около 15об.%: σизг до 1000МПа и К1с до 7МПаּм0,5.
3. Частично стабилизированный диоксид циркония PSZ (Partialy Stabilized Zirconia, рис.7,в). Образуется при добавлении в ZrO2 оксидов Mg, Ca, Y и др. При спекании в области гомогенности кубической фазы образуются крупные зерна c-ZrO2 (60мкм). После отжига в двухфазной области появляются тетрагональные частицы, когерентно связанные с кубической фазой. В системах ZrO2-MgO(CaO) размер t-частиц должен быть менее 0,25мкм. В случае огрубления частиц когерентность нарушается и их упрочняющая способность резко падает. Объемное содержание t-фазы составляет около 40%. PSZ вследствие высокой вязкости (К1с до 10МПаּм0,5) и прочности (σизг до 1500МПа) находит очень широкое применение в машиностроении.
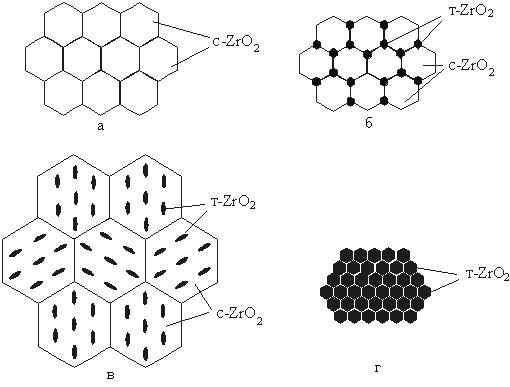
 Рис.7. Основные типы структур циркониевых керамик:
Рис.7. Основные типы структур циркониевых керамик:
а – CSZ, б – ZTA, в – PSZ, г – TZP
4. Тетрагональный диоксид циркония TZP (Tetragonal Zirconia Policrystals, рис.7,г). Данный материал реализуется в системах ZrO2– Y2O3(CeO) и состоит только из стабилизированных тетрагональных зерен. Спекание происходит в области гомогенности t-фазы, затем следует закалка. Диссипация энергии при упрочняющем фазовом превращении в TZP особенно высока и приводит, при оптимальной структуре, к экстремально высоким механическим характеристикам: σизг до 2400МПа при К1с около 15МПаּм0,5. При этом TZP обладает высокой ионной проводимостью. В развитых государствах TZP уже прошел испытания в различных областях машиностроения и применяется в производстве изделий конструкционного и инструментального назначения.
Конструкционную керамику на основе ZrO2, так же как и корундовую получают путем формования и спекания ультрадисперсных порошков (УДП). Сущность методов получения подобных порошков описана выше, здесь лишь следует отметить некоторые особенности применения этих методов для производства УДП ZrO2. При использовании метода совместного осаждения гидроксидов (СОГ) наблюдается негомогенность систем ZrO2-Y2O3 (MgO, CaO и др.). Это объясняется тем, что совместно осаждаемые соответствующие гидроксиды должны выпадать в осадок при различных показателях рН. Приливание раствора аммиака к смешанному раствору сульфатов (хлоридов и т.п.) приводит не к одновременному, а частично к последовательному осаждению гидроксидов. После их обезвоживания эта негомогенность переходит и твердые растворы на основе ZrO2. В этом отношении получение порошков методом плазмохимического синтеза является более предпочтительным. В то же время порошки, получаемые методом ПХС, как отмечалось, имеют сферическую форму, и, как следствие, низкие технологические характеристики. Поэтому перед формованием изделий из данных порошков требуется предварительный помол с целью раздробления микросфер. Формование порошков ZrO2 в заготовки проводят методом одноосного статического сухого прессования и прессованием в гидростатах при давлении 400–600МПа. Температура спекания стабилизированного ZrO2 лежит в интервале 1500–2000°С в зависимости от вида и количества оксида стабилизатора. Как отмечалось выше, в технологии некоторых видов циркониевой керамики применяется дополнительная термическая обработка. Так, в технологии керамики из частично стабилизированного диоксида циркония после спекания при температуре 1800–2000°С следует отжиг при 1400–1500°С с целью выделения упрочняющих дисперсных включений t-фазы. При изготовлении изделий из тетрагонального ZrO2 применяется закалка с температуры спекания 1600°С. Максимально высокие прочностные характеристики имеют изделия из ZrO2, получаемые методами ГП и ГИП.
Традиционно керамика на основе ZrO2 применялась в металлургической промышленности для изготовления тиглей для плавки металлов. Сегодня циркониевая керамика является одним из наиболее перспективных керамических материалов конструкционного и инструментального назначения и используется в технологии получения деталей газотурбинных и дизельных двигателей, узлов трения, уплотнительных колец насосов, элементов запорной арматуры, форсунок распылительных камер, фильер для протяжки проволоки, режущего инструмента. Также керамика на основе ZrO2 находит применение в медицине для изготовления имплантантов в костные ткани.
4.2.3. Керамика на основе MgO, CaO, BeO, ThO2, UO2
Керамика на основе MgO.Оксид магния существует только в одной модификации, называемой периклазом. с кристаллической решеткой типа каменной соли. МgО является основным оксидом, при взаимодействии с водой и с водяными парами образует гидроксид Мg(ОН)2. МgО устойчив к воздействию щелочей и разрушается под действием кислот.
MgO получают путем переработки магнийсодержащих минералов, главным образом магнезита. Одним из источников получения чистого оксида магния является морская вода. Чистый MgO может быть непосредственно получен термическим разложением гидрокарбоната магния и гидроксида магния при температурах 600–800°С, а также окислением металлического магния в парообразном состоянии в токе кислорода при температуре до 1200°С. Наиболее активные и мелкодисперсные (не более 0,5мкм) порошки оксида магния получают при разложении Мg(ОН)2.
Растворимость МgО в воде и в самых слабых кислотах исключает применение некоторых методов керамической технологии. Так, гидратация МgО ограничивает возможность тонкого помола порошков в воде. Растворимость МgО в кислотах исключает литье водных суспензий из кислых сред.
При изготовлении изделий из МgО преимущественное распространение имеет метод прессования. Используют также методы литья под давлением горячих шликеров, гидростатического прессования, литья из щелочных водных суспензий. Перед формованием оксид магния предварительно отжигают при температуре 1000–1300°С и тонко измельчают в вибромельницах сухим способом.
Температура спекания изделий из МgО составляет 1700–1750°С. Для достижения более высокой плотности при спекании часто используют добавки оксидов, которые образуют с MgО твердые растворы. Среди этих добавок наиболее эффективное действие оказывает ТiO2 и ZгО2. Например,при введении в чистый MgО 0,2% диоксида циркония теоретическая плотность достигается уже при 1320°С и выдержке 1,5ч.
Спеченная керамика на основе MgO имеет высокую температуру плавления – 2800°С, которая казалось бы позволяла применять этот широко распространенный в природе материал при самых высоких температурах. Гидратация и повышенная летучесть MgO ограничивают температуру его применения. Практически температура применения MgO в атмосферных условиях находится в пределах 2000–2200°С, а в восстановительной среде и вакууме – около 1700°С. Оксид магния обладает низкой термостойкостью из-за высокого коэффициента расширения и сравнительно небольшой теплопроводности. При равных условиях резкого охлаждения одинаковые по форме и размерам изделия из МgО выдерживают в 5–10 раз меньше теплосмен, чем изделия из А12О3, и в 50–100 раз меньше, чем из ВеО. При 2000°С испаряется до 40% веса MgO. Оксид магния является хорошим изолятором. Кристаллы обладают ионной проводимостью. Спеченная керамика на основе MgO имеет низкие прочностные характеристики: σизг не более100МПа при 20°С, К1с не выше 5МПаּм0,5.
Керамика из МgО применяется в производстве огнеупорных изделий, эксплуатируемых в щелочных средах и расплавах. В тиглях из МgО плавят железо, цинк, алюминий, олово, медь, а также тяжелые редкоземельные металлы. Изделия из MgO применяют для футеровки высокотемпературных печей и аппаратов, работающих при температуре до 2000°С на воздухе или в парах щелочных металлов.
Керамика на основе CaO.Оксид кальция является одним из самых распространенных в природе высокоогнеупорных окислов. Это единственное соединение кальция с кислородом. Оксид кальция имеет кристаллическую решетку кубической системы типа каменной соли, плотность 3,35г/см3, твердость по Моосу 4,5. Его температура плавления составляет 2570°С. CaO обладает резковыраженными основными свойствами, высокой термодинамической устойчивостью, хорошей устойчивостью против многих расплавленных металлов. Керамика на основе CaO используется в технике ограниченно вследствие повышенной гидратации CaO и испарения материала при высоких температурах (1800°С и выше).
При изготовлении изделий из СаО порошок сначала прессуют в брикеты, которые обжигают и размалывают. Это делается для снижения усадки во время окончательного спекания изделий. После помола обожженного брикета из зернистого порошка с неводной органической связкой прессуют тигли при давлении 50–70МПа.Температура спекания СаО составляет 1165–1700°С. Спеченную керамику из CaO покрывают защитными водонепроницаемыми пленками для предохранения от гидратации.
Так как CaO очень стоек к воздействию расплавов металлов, из него изготавливают тигли, применяемые для плавления цветных металлов, в частности для плавления платины и других металлов этой группы, а также для получения чистого урана.
Керамика на основе BeO.Оксид бериллия – единственное кислородное соединение бериллия. По своей химической природе BeO является слабоосновным оксидом, стойким к воздействию щелочей и щелочных расплавов. По отношению к кислым средам и расплавам ВеО неустойчив. Оксид бериллия кристаллизуется в гексагональной системе и имеет структуру типа вюрцита. Температура плавления чистого оксида бериллия 2570°С.
Оксид бериллия получают преимущественно из минерала берилла, химический состав которого соответствует формуле Ве3А12Si6О18. Оксид бериллия получают щелочным или кислотным способом. По способу щелочной переработки берилл с известью подвергают спеканию, в процессе которого образуются силикаты, алюминаты кальция и BeO. Продукт спекания разлагают серной кислотой. Раствор сульфата бериллия обрабатывают аммиаком, при этом выпадает Ве(ОН)2, который затем прокаливают до ВеО. При кислотном способе получения тонкоизмельченный берилл смешивают с NaF (1:2) с последующим прокаливанием при температуре 600–800°С. Образовавшийся при этом растворимый ВеF2 выщелачивают горячей водой и в кислый раствор добавляют едкий натр до нейтрализации. Образовавшийся при этом NaF возвращают обратно в процесс, а Ве(ОН)2 прокаливают до ВеО.
Изделия из BeO могут быть получены литьем из шликера, экструзией, прессованием и др. BeO предварительно обжигают при температуре 1300–1400°С, а затем измельчают в шаровой мельнице. Шликер для водной отливки изделий должен иметь рН=4,5-5,0, т.е. кислую среду. После сушки изделия спекают при температуре 1800°С. При формовании изделий из высокодисперсного порошка ВеО путем прессования его гранулируют с добавлением связующего, например водорастворимой синтетической смолы из этиленгликоля. Изделия прессуют при давлении до 150–200МПа. Высокоплотные изделия из ВеО могут быть изготовлены также литьем из термопластичных шликеров или прессованием ВеО, предварительно обожженного при 1700–1800°С с последующим измельчением до размера частиц не более 25мкм.При использовании такого порошка ВеО требуемая температура спекания повышается до 2000°С,одновременно линейная усадка изделий значительно снижается и составляет 8–9%. Для получения высокоплотных изделий из ВеО с мелкозернистым строением применяют горячее прессование в графитовых формах при температуре от 1400 до 1800°С и давлении до 15МПа.
Предел прочности при изгибе спеченной керамики из ВеО не превышает 300МПа при комнатной температуре. Теплопроводность BeO при низких температурах превосходит теплопроводность других керамических материалов в 7–10 раз. При нормальной температуре теплопроводность ВеО превышает также теплопроводность ряда металлов (стали, никеля, молибдена, свинца и др.). Большая теплопроводность окиси бериллия является одним из отличительных свойств этого материала.
По своим химическим свойствам керамика из ВеО является слабоосновным огнеупором и занимает промежуточное место между А12О3 и МgО. Она довольно чувствительна к воздействию различных шлаков и расплавов, особенно кислых растворов и стекол. Zг, Мg и Са, имеющих большое сродство к кислороду, восстанавливают ВеО до металла. С фтором и фторидами ВеО очень легко реагирует. При температурах выше 1800°С ВеО восстанавливается углеродом с образованием карбида бериллия ВеС. Оксид бериллия является чрезвычайно токсичным веществом, что значительно ограничивает возможность применения этого материала и усложняет технологию производства изделий.
Основная область применения керамики из ВеО – это ядерная энергетика. Это обусловлено тем, что ВеО обладает высоким коэффициентом замедления тепловых нейтронов. Из BeO изготавливают конструкционные элементы в ядерных реакторах. Тигли из ВеО применяются для плавки бериллия, платины, тория, титана, урана и др. Высокая термостойкость позволяет изготавливать из ВеО детали реактивных двигателей. Хорошие диэлектрические свойства ВеО и вакуумная плотность определили его применение в электро- и радиотехнике.
Керамика на основе ThO2.ТhO2 – единственное кислородное соединение тория, не имеющее модификационных форм. Он кристаллизуется в кубической системе типа флюорита. Диоксид тория ТhО2 имеет наиболее высокую среди оксидов температуру плавления – 3050°С.
Диоксид тория получают из из монацитовых песков, в состав которых входит до 15–18% ThO2. Исходный ThO2 обычно предварительно обжигают при температуре 1150°С, затем измельчают в стальных мельницах с последующей отмывкой соляной кислотой. Изделия формуют прессованием и литьем водных или парафиновых шликеров. ThO2 спекают при температурах 1800–2000°С, при этом изделия приобретают плотность 9,5–9,6г/см3.
Диоксид тория является одним из наиболее тяжелых высокоогнеупорных оксидов, его теоретическая плотность составляет 9,69г/см3.Термическая стойкость изделий из ТhO2 в связи с малой теплопроводностью, сравнительно большим коэффициентом термического расширения и малой прочностью на растяжение, является невысокой. ThO2 не взаимодействует с щелочами и щелочными расплавами, нерастворим в кислотах.
Высокая огнеупорность керамики из ThO2 позволяет использовать изделия из нее при температурах нагрева до 2700°С. В тиглях из ТЮ2 плавят осмий, платину, родий, иридий и другие тугоплавкие металлы. ThO2 используют также в ядерной энергетике. Так как ThO2 радиоактивен и токсичен, то необходимо при работе с ним соблюдать соответствующие правила техники безопасности.
Керамика на основе UO2.Диоксид урана имеет температуру плавления 2872°С. Другие оксиды урана разлагаются при сравнительно низких температурах. Плотность UO2 составляет 10,97г/см3. UO2 обладает гранецентрированной кубической решеткой типа флюорита. UO2 имеет основные свойства. Он нерастворим в соляной кислоте, хорошо растворяется в азотной кислоте, царской водке и смеси азотной и плавиковой кислот. С КаОН не реагирует, но реагирует с перекисью натрия, с Аl2О3, МgО, ВеО, не взаимодействует до температуры 1800°С. Диоксид урана устойчив вплоть до температуры плавления только в чистом водороде или вакууме. Поэтому использовать керамику из UO2 можно только в восстановительной или нейтральной среде. По этой же причине изделия из UO2 спекают в среде инертного газа или в вакууме.
Диоксид урана получают химической переработкой урановых руд, в первую очередь, минерала уранинита, содержание UO2 в котором достигает 50–60%.
Изделия из UO2 получают прессованием с органическими пластификаторами, шликерным литьем и протяжкой. Для прессования изделий необходимо давление около 70МПа. Стержни из UO2 изготавливают гидростатическим прессованием или протяжкой. Спекают изделия из UO2 в вакууме или в среде нейтрального газа при температуре 1750°С.
Прочностные характеристики спеченной керамики на основе UO2 находятся на уровне показателей прочности А12Оз. Термическая стойкость изделий из UO2 невелика, что связано с довольно большим коэффициентом термического расширения.
Диоксид урана получил широкое применение как реакторное топливо в виде тепловыделяющих элементов в реакторах различных типов. UO2 может быть использован либо в диспергированном виде в керамических или металлических матричных системах, либо в виде изделий – дисков, брусков, стержней, таблеток и др.
4.2.4. Керамика на основе TiO2, титанатов, цирконатов и других соединений с подобными свойствами
Керамика на основе TiO2.Диоксид титана обладает повышенным значением диэлектрической проницаемости и является основным материалом для изготовления так называемой конденсаторной керамики. TiO2 существует в трех модификационных формах: анатаз, брукит и рутил. Устойчивой является высокотемпературная форма – рутил, который имеет тетрагональную кристаллическую решетку.
Промышленность изготавливает два вида конденсаторов:
1. Низковольтные высокочастотные для радиотехники.
2. Высоковольтные для электротехники сильных токов.
Низковольтные высокочастотные конденсаторы выпускают в виде дисков трубок. Высоковольтные конденсаторы выпускают трех видов: трубчатые, горшковые и бочоночные. По размеру и весу они значительно массивнее, чем высокочастотные, вес которых равен нескольким граммам.
Компоненты шихты конденсаторной керамики являются непластичными материалами, поэтому во многих случаях в шихту вводят пластичную огнеупорную глину. В некоторые массы глину не вводят и изделия получают методами непластичной технологии с введением органических пластификаторов. Дисковые и бочоночные конденсаторы формуют методом прессования, трубчатые – методом протяжки, а горшковые – методом литья из водных суспензий.
Изделия из TiO2 следует спекать в слабоокислительной среде во избежание восстановления титана до низшей валентности. Соединения трехвалентного титана сильно ухудшают электрофизические свойства изделий, при этом резко увеличиваются диэлектрические потери, уменьшается удельное сопротивление и снижается электрическая прочность изделий. Обычно керамику из TiO2 спекают в электрических туннельных печах с карбидокремниевыми нагревателями. Температура спекания конденсаторной керамики находится в пределах 1250–1350°С. Конденсаторы металлизируют серебром, припаивают к ним выводы, после чего покрывают лаком соответствующего цвета.
Керамика на основе титанатов, цирконатов и других соединений с подобными свойствами. К настоящему времени синтезировано и детально изучено большое количество керамических материалов, являющихся сегнето- и пьезоэлектриками. К ним относятся титанаты, цирконаты, ниобаты, танталаты щелочно-земельных металлов и их комбинации, ниобаты, танталаты щелочных металлов, сегнетоэлектрики сложного состава.
Отличительной особенностью сегнетоэлектриков по сравнению с обычными диэлектриками является резко выраженная зависимость диэлектрической проницаемости ε от напряженности электрического поля.Значение ε сегнетоэлектриков велико и имеет максимум при определенной температуре. Другим важным свойством сегнетоэлектриков является наличие у них так называемого сегнетоэлектрического гистерезиса, т. е. явления отставания изменения величины поляризации от изменения напряженности поля. В некоторой определенной для каждого сегнетоэлектрика области температур происходит самопроизвольная ориентация его молекул – спонтанная поляризация, в результате которой образуется электрический момент.
В зависимости от направления поля знак спонтанной поляризации может быть изменен. Существование электрического момента связано с изменением структуры сегнетоэлектрика в точках фазового перехода. При температуре фазового перехода (точка Кюри) спонтанная поляризация сегнетоэлектрика появляется или исчезает. Диэлектрическая проницаемость в точке Кюри достигает наибольшего значения.
Сегнетокерамика, в отличие от солевых сегнетоэлектриков (сегнетова соль NaKC4H4O6ּ4H2O), не обладает пьезоэлектрическими свойствами. Они возникают после того, как керамика будет подвергнута воздействию сильного постоянного электрического поля, в результате чего произвольно направленные диполи ориентируются в одном определенном направлении.
Пьезоэффект заключается в том, что при приложении механической нагрузки изменяется поляризация пьезоэлектрика и на его поверхности появляются избыточные заряды, которые могут быть сняты и направлены в цепь. В этом случае имеет место прямой пьезоэффект. При помещении в электрическое поле в пъезоэлектрике возникнут механические напряжения, сопровождаемые изменением размера образца – происходит обратный пьезоэффект.
Считается, что при действии сжимающих усилий возникает положительный заряд, при действии растягивающих – отрицательный. Соответственно будет вести себя пьезоэлектрик в полях с разным знаком: увеличиваться в размере в положительно заряженном, сокращаться в отрицательно заряженном поле.
Пьезоэффект количественно определяется пьезомодулем
d = Q/F, (17)
где Q – заряд, возникающий на электродах образца, F – сила, приложенная к образцу.
В настоящее время для производства пьезокерамики широко применяют титанат бария BaTiO3. Титанат бария обладает сложным полиморфизмом: при температурах ниже –90°С он имеет ромбоэдрическую решетку, от –90 до 5°С – ромбическую, от 5 до 120°С – тетрагональную и выше 120°С – кубическую. Таким образом BaTiO3 имеет три точки Кюри и может находиться в четырех модификационных формах, три из которых сегнетоэлектрические (кроме кубической).
На первой стадии технологии керамики из титаната бария происходит его синтез из BaO и TiO2 в соотношении 1:1 путем обжига измельченных и спрессованных в брикеты компонентов при температуре 1300°С в слабоокислительной среде. Синтезированный BaTiO3 подвергают помолу. Изделия из BaTiO3 формуют прессованием и горячим литьем.
Температура спекания титаната бария составляет 1320–1360°С. После спекания на изделия наносят тонкослойное серебряное покрытие – электроды. Затем изделия подают на поляризацию. Поляризацию производят в трансформаторном масле при нагреве до 110–115°С и напряженности поля 6кв/см.Степень поляризации пьезоэлемента зависит от величины приложенного напряжения, длительности воздействия электрического поля и температуры, при которой происходит поляризация. Установлено, что в первые дни после поляризации наблюдается ухудшение пьезоэлектрических свойств, в первую очередь пьезомодуля. Однако после примерно 10 суток их значение стабилизируется.
Кроме BaTiO3 синтезирован целый ряд титанатов, у которых ион Ва2+ замещен ионом двухвалентного металла Ca, Рb, Сd и др. Эти титанаты используются чаще всего в виде твердых растворов, которые они образуют между собой, а также с титанатом бария. Из ряда титанатов наиболее высокой температурой Кюри (490°С) обладает титанат свинца РbTiO3. Его твердые растворы с другими титанатами и подобными соединениями в настоящее время его широко применяют в производстве пьезокерамики.
Пьезоэлектрические свойства были .обнаружены у ряда цирконатов, среди которых наибольшее практическое значение получил цирконат свинца РbZrО3. При температуре 230°С у РbZrО3 имеется фазовый переход из псевдомоноклинной структуры в кубическую, при котором резко выражен максимум диэлектрической проницаемости. Наиболее высокими значениями пьезоэлектрических свойств обладают твердые растворы цирконата – титаната свинца Рb(Zr,Ti)О3, так называемые материалы системы ЦТС. Пьезокерамика на основе твердых растворов Рb(Zr,Ti)О3 имеет значительные преимущества по сравнению с титанатом бария и твердыми растворами на его основе. ЦТС имеет более высокую температуру Кюри и, как следствие, повышенную температуру эксплуатации. Пьезосвойства материалов ЦТС более высокие и стабильные в широком температурном интервале. Благодаря этим качествам пьезокерамика на основе твердых растворов цирконата - титаната находит очень большое применение в технике и области ее применения постоянно расширяются.
Сравнительно невысокая температура Кюри у титаната бария и других известных сегнетокерамических материалов вызвала необходимость поиска новых материалов, способных работать при высоких температурах. Такими материалами оказались ниобаты и танталаты одно- и двухвалентных металлов как в виде отдельных соединений, так и в виде твердых растворов различных комбинаций этих соединений. Среди ниобатов наиболее высокой температурой Кюри обладает метаниобат свинца РbNb2О6 с точкой фазового перехода 570°С. Метаниобат свинца является основой пьезокерамических материалов в системе твердых растворов различных ниобатов. Для изготовления других видов сегнетокерамических материалов применяют танталаты калия и натрия (КTаО3 , NаТаО3 ), твердые растворы танталатов - ниобатов, станнаты, их твердые растворы и ряд других соединений.
| <== предыдущая страница | | | следующая страница ==> |
| Оксидная техническая керамика | | | Керамика на основе шпинелей |
Дата добавления: 2015-07-26; просмотров: 772; Нарушение авторских прав

Мы поможем в написании ваших работ!