
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Ошибки титрования
1.Пригодность того или иного индикатора для данного титрования можно количественно характеризовать индикаторной ошибкой титрования, возникающей из-за несовпадения рТ и рН в точке эквивалентности. При титровании сильной кислоты сильным основанием и наоборот ошибка может быть водородной или гидроксидной.Водородная, или Н+-ошибка, возникает, если рТ < 7, т. е. когда при титровании сильной кислоты щелочью в растворе после окончания титрования остается некоторое количество неоттитрованной кислоты. Для гидроксидной ошибки при титровании сильной кислоты характерно рТ > 7, что указывает на избыточное содержание в растворе сильного основания по сравнению с эквивалентным.
Водородную ошибку можно оценить следующим образом. Если титруется V (мл) раствора кислоты концентрации с,то по окончании титрования объем раствора увеличивается примерно до 2V (так как титрант имеет такую же концентрацию), концентрация ионов водорода становится равной 1,0 • 10-рТ и количество ионов Н+ в конечном растворе составит  моль. Процентное отношение этой величины к исходному количеству кислоты равно Н+-ошибке:
моль. Процентное отношение этой величины к исходному количеству кислоты равно Н+-ошибке:
 (1)
(1)
При неодинаковых концентрациях NaOH и НСl множитель 2 следует заменить на множитель  .
.
При титровании 0,1М НС1 с метиловым оранжевым водородная ошибка  . Для данного титрования метиловый оранжевый оказывается вполне удовлетворительным индикатором. При титровании 0,01М НС1 в присутствии метилового оранжевого Н+-ошибка составляет:
. Для данного титрования метиловый оранжевый оказывается вполне удовлетворительным индикатором. При титровании 0,01М НС1 в присутствии метилового оранжевого Н+-ошибка составляет:  . Это уже больше обычно допустимой ошибки, следовательно, для титрования разбавленных растворов НС1 метиловый оранжевый непригоден.
. Это уже больше обычно допустимой ошибки, следовательно, для титрования разбавленных растворов НС1 метиловый оранжевый непригоден.
Гидроксидная ошибка рассчитывается аналогично. Концентрация ионов водорода в растворе после окончания титрования 10-рТ, а концентрация гидроксид-ионов [ОН-] =  .
.
Следовательно, в растворе по окончании титрования содержится  моль щелочи (V – объем анализируемого раствора).
моль щелочи (V – объем анализируемого раствора).
В процентах к исходному количеству кислоты (или эквивалентному количеству щелочи) это составляет гидроксидную ошибку титрования:
 (2)
(2)
Если концентрации кислоты и щелочи неодинаковы, в формулу (2) вместо коэффициента 2 следует ввести множитель  .
.
Титрование V (мл) 0,1М НСl раствором NaOH такой же концентрации с фенолфталеином в качестве индикатора заканчивается при рТ 9,0. Гидроксидная ошибка этого титрования 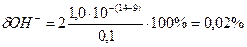 . Ошибка титрования 0,01 М НСl в тех же условиях составит 0,2%. Если в качестве индикатора взять не фенолфталеин, а, например, ализариновый желтый, у которого рТ 11,0, то в этом случае
. Ошибка титрования 0,01 М НСl в тех же условиях составит 0,2%. Если в качестве индикатора взять не фенолфталеин, а, например, ализариновый желтый, у которого рТ 11,0, то в этом случае  , а в 0,01 М НСl ошибка будет уже доходить до 20%. Такой индикатор для данного титрования явно не подходит.
, а в 0,01 М НСl ошибка будет уже доходить до 20%. Такой индикатор для данного титрования явно не подходит.
2. Известное значение имеет также ошибка титрования, вызываемая тем, что рН-индикаторы имеют кислотно-основную природу и переход индикатора из одной формы в другую требует расхода реагента. С уменьшением количества индикатора эта ошибка уменьшается, в связи с чем при титровании рекомендуется обходиться минимальным количеством индикатора.
3. Кроме концентрации индикатора, на изменение его окраски оказывает влияние ряд других факторов. Сюда относятся, как уже отмечалось, концентрация электролитов и других веществ в растворе, растворенный СО2, а также температура и так называемые спиртовая и белковая ошибки.
Солевая ошибка.Состояние равновесия в растворе индикатора контролируется зависимостью pKHInd от ионной силы. Эта ошибка относительно высока для индикаторов сульфофталеинов, имеющих высокий заряд щелочной формы, и невелика у азоиндикаторов. В общем следует сказать, что с ростом концентрации электролита у индикатора-кислоты интервал перехода смещается в область более низких значений рН, а у индикаторов-оснований – в сторону более высоких рН. Кроме того, присутствие в растворе электролита обычно вызывает уменьшение интенсивности окраски индикатора.
4.Влияние СО2 связано с растворимостью диоксида в воде, которая возрастает в щелочных растворах. Поэтому все индикаторы, имеющие интервал перехода в нейтральной или щелочной области (например, фенолфталеин), чувствительны к СО2, в связи с чем при титровании щелочных растворов не рекомендуется интенсивное перемешивание особенно при приближении к точке эквивалентности. Эффективным оказывается также кипячение раствора для удаления СО2.
5.Температура влияет на величину pKHInd так же, как и на величину любой другой константы равновесия и, следовательно, влияет на интервал перехода индикатора и интенсивность его окраски. Однако титрование кислот и оснований обычно проводят при температурах, близких к комнатной, а небольшие колебания температуры не оказывают существенного влияния на интервал перехода индикатора и его показатель титрования рТ.
6.Спиртовая ошибка вызывается тем, что растворы индикаторов обычно готовятся на спирте и, таким образом, в анализируемый раствор вместе с индикатором вносится некоторое количество спирта. Его количество невелико, поэтому спиртовая ошибка незначительна. В неводных и смешанных растворителях свойства индикаторов (интервал перехода и рТ) меняются существенно.
7.Белковая ошибка.Присутствие в водном растворе белковых веществ и макромолекул может существенно изменить интервал перехода индикатора. Она уменьшается, когда при титровании положительно заряженных коллоидов применяют индикатор-основание, а в случае отрицательно заряженных – индикатор-кислоту.
| <== предыдущая страница | | | следующая страница ==> |
| Кислотно-основные индикаторы. Индикатор Область перехода рН рКа (I=0) Изменение окраски Метиловый фиолетовый 0—1,8 — Желтая — фиолетовая | | | Кривая титрования слабой кислоты сильным основанием |
Дата добавления: 2015-07-26; просмотров: 314; Нарушение авторских прав

Мы поможем в написании ваших работ!