
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Кривая титрования слабой кислоты сильным основанием
В начале титрования в растворе находится только слабая кислота (другими источниками ионов водорода можно пренебречь). В растворе кислоты при степени ее диссоциации менее 5%
[Н+] = 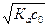 и рН =
и рН = 
До ТЭпри титровании получается сопряженное основание, и раствор представляет собой буферную смесь, поэтому рН вычисляют по формуле:
[Н+] =  ,
,
рН = 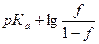
где f – степень оттитрованности, т.е. отношение количества оттитрованного в данный момент вещества nт к исходному количеству n0.
В ТЭвся кислота оттитрована, и рН раствора определяется наличием сопряженного основания (другими источниками ОН--ионов можно пренебречь). В растворе слабого основания
[ОН-] = 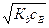 ; [Н+] = Кw /
; [Н+] = Кw / 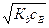 и рН = 14 – 1/2рКb – 1/2рсв
и рН = 14 – 1/2рКb – 1/2рсв
Поскольку при титрования количество получившегося основания равно исходному количеству кислоты, пренебрегая изменением объема, можно считать, что св = с0.
После ТЭосновным источником ОН--ионов будет добавленное сильное основание.
Кривая титрования 100,0 мл 0,1М СН3СООН 0,1М раствором NaOH выглядит следующим образом:

рН раствора до точки эквивалентности изменяется плавно, хотя и с более высоким угловым коэффициентом, чем при титровании сильной кислоты. Линия нейтральности пересекается с кривой титрования еще до точки эквивалентности. В области точки эквивалентности (±0,1%) наблюдается скачок титрования от рН 7,76 до рН 10,00, а точка эквивалентности находится при рН 8,88.
Характерной особенностью кривых титрования слабых одноосновных кислот является несовпадение точки эквивалентности с точкой нейтральности и расположение точки эквивалентности в щелочной области, так как в точке эквивалентности образуется основание, сопряженное с титруемой кислотой С уменьшением концентрации кислоты и увеличением температуры скачок уменьшается. Он уменьшается также с уменьшением константы диссоциации кислоты.
Индикаторы и индикаторные ошибки при титровании слабой кислоты
Интервалы перехода бромтимолового синего и метилового оранжевого не перекрываются скачком титрования уксусной кислоты и, следовательно, для данного титрования оба индикатора непригодны. Наиболее подходящим индикатором для титрования уксусной кислоты является фенолфталеин, окрашивающий раствор в точке эквивалентности в красный (пурпурный) цвет.
Выбор индикатора или оценку его пригодности можно сделать также на основании индикаторных ошибок титрования. При титровании слабой кислоты может возникнуть гидроксидная и кислотная индикаторные ошибки. Гидроксидная ошибка рассчитывается по формуле (2). Если при титровании 0,1 М уксусной кислоты в качестве индикатора взять фенолфталеин с рТ 9,0, гидроксидная ошибка 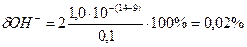 , что подтверждает пригодность фенолфталеина для данного титрования.
, что подтверждает пригодность фенолфталеина для данного титрования.
Кислотная, или НА-ошибка, обусловлена наличием в растворе неоттитрованной слабой кислотой. Эта ошибка определяется отношением:


Следовательно, для титрования слабой кислоты, имеющей константу диссоциации К,будут пригодны только те индикаторы, у которых рТ на 3 единицы или больше превышает рК.Например, для титрования уксусной кислоты могут быть использованы индикаторы, у которых рТ > 4,76 + 3 = 7,76, и, следовательно, метиловый оранжевый будет явно не подходящим, как это уже было установлено. Условию (7.4) для титрования уксусной кислоты удовлетворяет фенолфталеин (рТ 9,0). Могут быть использованы и многие другие индикаторы, удовлетворяющие условию (7.4), если гидроксидная ошибка не будет превышать заданного предела.
Ализариновый желтый Р имеет рТ 11,0 и с точки зрения условия (7.4) его можно использовать для титрования уксусной кислоты. Однако гидроксидная ошибка в этом случае составляет  , что примерно на порядок превышает обычную погрешность титриметрических определений, и, следовательно, для данного титрования этот индикатор применять не следует.
, что примерно на порядок превышает обычную погрешность титриметрических определений, и, следовательно, для данного титрования этот индикатор применять не следует.
| <== предыдущая страница | | | следующая страница ==> |
| Ошибки титрования | | | Кривая титрования слабого основания сильной кислотой |
Дата добавления: 2015-07-26; просмотров: 345; Нарушение авторских прав

Мы поможем в написании ваших работ!