
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Химические свойства. 1.Галогенирование. Осуществляется с помощью хлористого сульфурила, брома в спиртовом растворе и триодид-иона (йод в растворе иодида калия)
1.Галогенирование. Осуществляется с помощью хлористого сульфурила, брома в спиртовом растворе и триодид-иона (йод в растворе иодида калия), причем в результате иодирования образуется тетраиодпиррол-иодол, являющийся хорошим антисептиком:
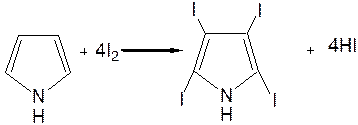
2. Сульфирование. Пиррол осмоляются при действии минеральных кислот (проявляют ацидофобные свойства), т.е. в кислой среде протон связывает неподеленную пару электронов кислорода или азота, образуется оксониевый или аммониевый ион, обладающий свойствами диена с сопряженными двойными связями, который легко полимеризуется и осмоляется:
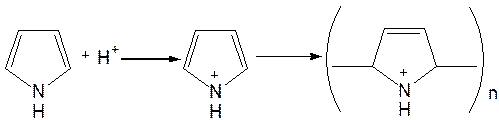
Поэтому сульфируют пиррол с помощью пиридинсульфотриоксида – комплекс пиридина с оксидом серы (VI) C6H5N×SO3:
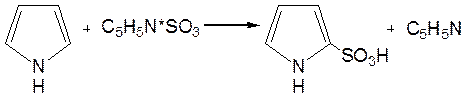
3. Реакция электрофильного замещения (механизм и ориентация замещения):

Пирролидин(тетрагидропиррол, тетраметиленимин) – бесцветная жидкость с резким аммиачным запахом, Ткип. = 86,6 °С. Он дымит на воздухе, хорошо растворим в воде и многих органических растворителях. Пирролидин является сильным основанием (рКа = 11,27), поэтому легко образует соли с сильными минеральными и органическими кислотами. Это соединение обладает всеми химическими свойствами вторичных аминов. Пирролидин возбуждающе действует на ЦНС, при длительном воздействии снижает уровень гемоглобина в крови, усиливает диурез. ПДКвозд 0,1 мг/м3.
Кольцо пирролидина является структурным элементом многих биологически активных соединений, например никотина, алкалоидов группы тропана, алкалоида гигрина. В небольших количествах пирролидин содержится в листьях табака и опии.
Тетрапирролыпредставляют собой соединения, структурными элементами которых являются четыре пиррольных кольца. Многие из этих соединений содержат в молекуле особую группировку их четырех пиррольных ядер, соединенных между собой с помощью четырех метиновых (=СН–) мостиков в 16-членное кольцо – ядро порфина. В молекуле порфина (и порфиринов) имеется непрерывное сопряжение p-связей (многоконтурная сопряженная p-система), при этом максимальное p-электронное взаимодействие охватывает 16-членный (С12N4) цикл, в котором порядок связей С=С и С=N достигает 1,5, а в ряде случаев и превышает его. Таким образом, 16-членный макроцикл (порфина) является ароматическим с повышенной термической устойчивостью, способным к реакциям электрофильного замещения. Сам порфин, как таковой, в природе не встречается и получен лишь синтетически. Он представляет собой высокоплавкое кристаллическое вещество темно-красного цвета:

При замещении атомов водорода в b-положении пиррольных колец порфина на радикалы образуются порфирины. Многие важные природные соединения являются металлическими производными порфиринов. Следует отметить, что атомы азота в ядре порфина и в порфиринах неравноценны – два из них являются пиррольными (имеют кислотный характер), а два – пирролиновыми (имеют основной характер). Такое строение является исключительно благоприятным для образования комплексов с металлами (для «хелатизации»), что существенно для проявления этими соединениями физиологической активности. Биологическое значение этих природных соединений определяется природой ионов металлов и заместителями в ядре порфина. Если комплекс образован с помощью иона железа (Fe3+), то при определенных заместителях в порфине мы получаем гемин – красное вещество крови (основная часть гемоглобина).
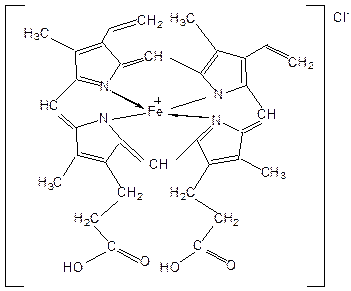
Порфин является устойчивой ароматической системой. Величина энергии сопряжения порфина (840 кДж/моль) также свидетельствует о его высокой стабильности.
| <== предыдущая страница | | | следующая страница ==> |
| Основные способы получения | | | Применение пиррола и его производных |
Дата добавления: 2015-07-26; просмотров: 359; Нарушение авторских прав

Мы поможем в написании ваших работ!