
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
Среди гетероциклических соединений наиболее многочисленна и разнообразна группа пятичленных гетероциклов, содержащих более одного гетероатома. Большинство этих циклических систем можно формально получить из фурана, пиррола и тиофена заменой одной или более групп — СН на гетероатом азота. Возможность варьирования числа и расположения атомов азота в кольце приводит к структурному многообразию гетероциклов.
Имидазол – более сильное основание, чем пиразол, что проявляется в образовании межмолекулярных водородных связей, а, следовательно, и в более высокой температуре его кипения по сравнению с пиразолом:

Оба атома азота в имидазоле (как и в пиразоле), эквивалентны и атом водорода легко мигрирует между ними. Имидазол образует соли как с сильными кислотами, так и со щелочными и щелочноземельными металлами. Водородные связи имидазола:

Ароматическая p-электронная система имидазола (как и пиразола), образована за счет трех электронов атомов углерода и трех электронов атомов азота. Однако следует отметить, что в 6 p-электронном сопряжении атомы азота участвуют неодинаково: один из атомов азота отдает в p-электронную систему электрон (пиридиновый азот), а другой атом азота – два электрона (пиррольный азот).
Реакции электрофильного замещения в ряду имидазола могут протекать либо по атомам азота (алкилирование и ацилирование), либо по атомам углерода в положения 4 и 5 по месту наибольшей электронной плотности: нитрование, сульфирование, галогенирование. Механизм и ориентация реакции электрофильного замещения:

Замещенный 4,5-диметилимидазол не вступает в реакцию нитрования:
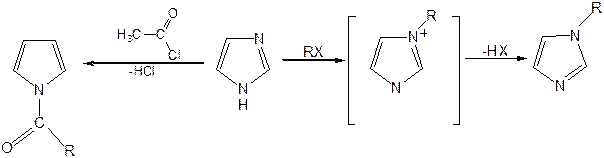
Ацилирование имидазола имеет большое биологическое значение: с помощью N-ацилимидазолов осуществляются реакции ферментативного переацилирования.
Пиразол.Введение второго атома азота в пиррол сильно стабилизирует молекулу, понижая электронную плотность в цикле, поэтому пиразол вступает в реакции электрофильного замещения намного труднее, чем пиррол:

Ароматическая природа пиразола связана с наличием сопряженной 6 p-электронной системы, в которую входят три электрона от атомов углерода и три электрона от атомов азота и имеют равную принадлежность протона каждому из этих атомов.
Расположенные рядом два атома азота в силу своей электро-отрицательности являются источником сильного –I эффекта. Соседние с атомами азота углеродные атомы вследствие этого несут некоторый избыток положительного заряда. Поэтому реакции электрофильного замещения в пиразоле идут в положении 4, как наиболее удаленном от атомов азота:

Пиразол является слабым основанием и слабой кислотой. Атом водорода при азоте довольно легко замещается на щелочные металлы, магний, серебро. Ряд производных пиразола применяются как лекарственные препараты, красители, люминесцентные вещества и др. Среди фармацевтических препаратов это - антипирин, пирамидон, анальгин:
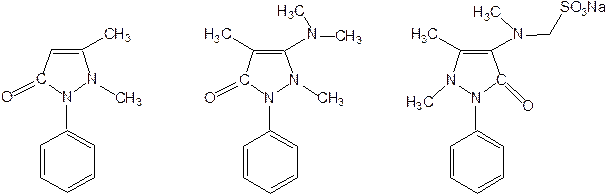
| <== предыдущая страница | | | следующая страница ==> |
| Триптофан | | | Оксазол |
Дата добавления: 2015-07-26; просмотров: 269; Нарушение авторских прав

Мы поможем в написании ваших работ!