
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Химические свойства
1. Восстановление водородом. При восстановлении водородом в момент выделения (действуя натрием на спиртовой раствор пиридина А.Н. Вешнеградский) или над катализатором пиридин превращается в пиперидин:

Гофмановская деструкция азотистых гетероциклов состоит в серии последовательных метилирований йодистым метилом до стадии образования четвертичной аммониевой соли, замены аниона иода на гидроксил и пиролиза аммониевого основания. При этом отщепляется вода и образуется непредельный амин, а на последней стадии – триметиламин и диеновый или полиеновый углеводород, имеющий ту же последовательность связей углеродных атомов, что и в исходном гетероцикле (последняя фаза – превращение 1,4-пентадиена в 1,3-пентадиен вызвана большей устойчивостью системы с сопряженными π-связями). Метод и применяется для установления последовательности С-С-связей в гетероцикле. В данном случае это – неразветвленная цепь из пяти углеродных атомов. Подобным образом может быть установлено строение и гомологов пиридина.
Переходя в пиперидин (гексагидропиридин), пиридин присоединяет шесть водородных атомов, следовательно, он имеет три двойные связи. Ароматические свойства пиридина доказывают бензоидность этих связей.
2. Взаимодействие пиридина с эфиром хлорсульфоновой кислоты и затем со щелочью: в результатеобразуется натриевый енолят глутаконового альдегида:

3. Нуклеофильные замещения в пиридине.А.Е. Чичибабин и О.А. Зейде нашли, что при нагревании пиридина примерно до 130° С в растворе ксилола с амидом натрия образуется с хорошим выходом α-аминопиридин. Реакция представляет собой типичную нуклеофильную атаку на ароматическое ядро:
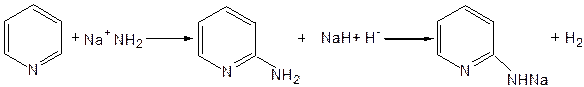
При значительно более высокой температуре (400 оС) подобная реакция происходит и между пиридином и твердым едким кали:
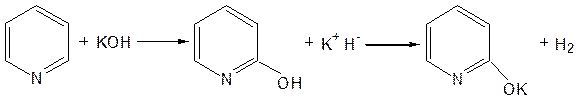
Аналогично, но в мягких условиях, на пиридин действуют такие еще более сильные нуклеофилы, как металлорганические соединения щелочных металлов:

При взаимодействии с галоидным альдегидом и вслед за этим – с анилином получается енольная форма дианила глутаконового альдегида:
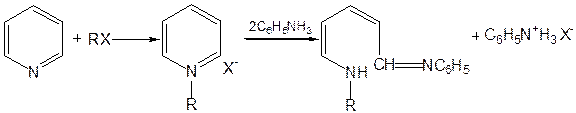
Такого рода размыкания пиридинового цикла применяются в синтезе открытых систем с сопряженными двойными связями. Таким образом, этот синтез дает смесь изомеров, подлежащую разделению.
4. Меркурирование. Пиридин и многие его производные легко подвергаются меркурированию при взаимодействии с ацетатом ртути, давая 3-пиридилмеркурацетат и его производные. При добавлении ацетата ртути к пиридинупри комнатной температуре образуется продукт присоединения, растворимый в избытке пиридина. Если продукт присоединения нагревать при 155 °С в сухом виде в присутствии воды, то происходит замещение в ядре и образуется 3-пиридилмеркурацетат с выходом 35–50 %.

5. Алкил- и арипиридиниевые соединения. Соли пиридиния. Среди продуктов присоединения пиридинового ряда наиболее важными являются четвертичные алкил- и арилпиридиниевые соли. При добавлении йодистого метила к пиридину реакция идет настолько энергично, что необходимо охлаждение. Обычно эту реакцию проводят в инертном растворителе, например в бензоле, из которого йодистый N-метилпиридиний (часто называемый иодметилатом пиридина) выделяется в виде бесцветных кристаллов с выходом, близким к количественному:
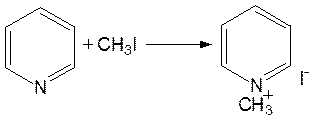
6. Восстановительное расщепление. Частично или полностью восстановленные производные пиридина теряют устойчивость цикла, присущую самому пиридину, и вследствие этого восстановление их в некоторых условиях приводит к разрыву шестичленного кольца. Конечно, и продукт восстановления самого пиридина – пиперидин может быть подвергнут специальным реакциям расщепления, например исчерпывающему метилированию или расщеплению его N-бензоильного производного по методу Брауна. Известно, например, что каталитическое гидрирование пиридина над никелевыми катализаторами, особенно при высокой температуре, дает π-амил-амин, π-пентан и аммиак .Вероятно, они образуются при гидрогенолизе первоначального продукта восстановления - пиперидина.
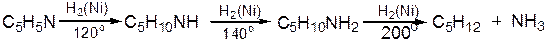
Пиперидин.Химия пиридина обусловлена ароматическим характером последнего в то время как химия пиперидина обусловлена прежде всего свойствами пиперидина как вторичного амина. Так как шестичленное пиперидиновое кольцо насыщено, то здесь существуют все те возможности оптической и геометрической изомерии, которые установлены в ряду циклогексана. Вследствие неполной симметричности пиперидинового цикла важную роль в определении числа таких изомеров играют положения групп в цикле.
Дегидрирование пиперидинов. Хорошо известно, что пиперидины могут быть дегидрированы до пиридинов. Однако практическое значение этого метода невелико. При дегидрировании производных пиперидина имеет место иногда аномальный ход реакции:
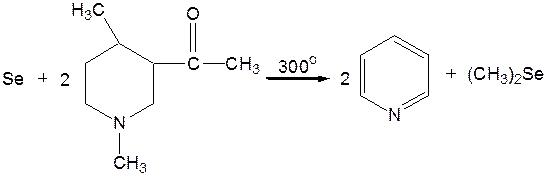
Производные пиридина и пиперидина, их биологическая активность. Многие производные пиридина обладают ярко выраженной биологической активностью. Ядро пиридина содержится в молекуле витамина РР, являющегося амидом никотиновой (b-пиридинкарбоновой) кислоты:

Витамин РР применяется для лечения пеллагры и других заболеваний, а также входит в состав никотинамидадениндинуклеотида (НАД+) и никотинамидадениндинуклеотидфосфата (НАДФ+), являющихся коферментами большого числа ферментов оксидоредуктаз, катализирую-щих ОВР, лежащие в основе биологического окисления.
Пиридиновый цикл является также основным структурным элементом молекул многих алкалоидов.
Алкалоиды – это группа азотистых соединений, обладающих основными свойствами и встречающихся в основном в растениях. Очень часто алкалоиды обладают сильным физиологическим или фармакологическим действием. Ряд известных алкалоидов содержит ядро пиридина и пиперидина. К ним относятся никотин, анабазин, кониин и др.
Никотинв виде солей лимонной и яблочной кислот (является сильным основанием) в большом количестве (до 3 %) содержится в листьях и корнях табака. Это один из наиболее ядовитых алкалоидов, 40 мг никотина является смертельной дозой для человека. В небольших дозах он возбуждает центральную и периферическую нервные системы, повышает кровяное давление.
Структурные формулы никотинамидадениндинуклеотид (НАД+) и никотинамидадениндинуклеотидфосфат:

Анабазин– изомер никотина, содержится в листьях табака:

Являясь сильным ядом для насекомых, анабазин вместе с никотином применяется в сельском хозяйстве в качестве инсектицида.
Кониин– сильный яд, содержащийся в соке болиголова, вызывающий паралич двигательных центров, а в больших дозах – паралич дыхательного центра.

Витамин В6представляет собой смесь трех веществ – пиридоксаля I, пиродоксола II и пиродоксамина III, которые являются производными 3-гидроксипиридина и отличаются друг от друга природой замещающей группы в положении 4 пиридинового кольца:
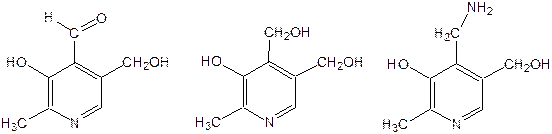
Эти витамины входят в структуру ферментов, регулирующих белковый обмен и катализирующих, в частности, реакции переаминирования и декарбоксилирования аминокислот. Оказалось, что коферментные функции выполняют только фосфорилированные производные пиродоксаля и пиридоксамина:
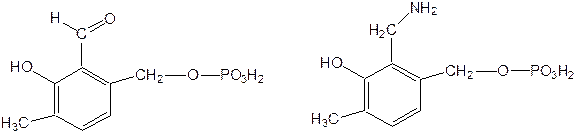
Доказано, что пиридоксальфосфат является простетической группой ферментов аминотрансфераз, катализирующих обратимый перенос аминогруппы от аминокислот на a-кетокислоту, и декарбоксилаз аминокислот, осуществляющих необратимое отщепление СО2 от карбоксильной группы аминокислот с образованием биогенных аминов.
Хинолин содержит бензольное и пиридиновое кольца, соединенные, как показано в формуле:

В целом свойства хинолина вполне соответствуют тому, что можно было ожидать на основании свойств уже изученных пиридина и нафталина.
Хинолин и его гомологи содержатся в каменноугольной смоле, а также в некоторых нефтях, откуда их и получают. Кроме этого, разработаны синтетические методы получения этих соединений. Из них наиболее широко используется синтез Скраупа, который заключается в нагревании анилина с глицерином и концентрированной серной кислотой в присутствии нитробензола в качестве окислителя. В результате дегидратации серной кислотой глицерин превращается в акролеин, который конденсируется с анилином в дигидрохинолин, окисляющийся в хинолин нитробензолом:
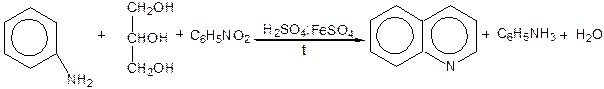
Этот синтез включает следующие стадии:
1. Дегидратация глицерина действием горячей серной кислоты, дающую непредельный альдегид – акролеин:

2. Нуклеофильное присоединение анилина к акролеину, приводящее к β-пропионовому альдегиду:

Хинолин подобен пиридину как по физическим свойствам, так и по химическим превращениям. Основные свойства у хинолина менее выражены, что является результатом влияния бензольного кольца, в сторону которого и смещена электронная плотность. Но как и пиридин, хинолин образует соли хинолиния с кислотами: соляной, серной, азотной; легко окисляется в N-окись:
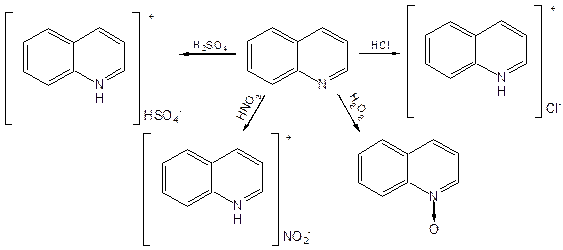
Являясь ароматической системой, содержащей децет p-электронов, хинолин вступает в реакции электрофильного и нуклеофильного замещения.
Электрофильные реагенты атакуют бензольную половину молекулы хинолина в положения 5 и 8, причем реакции протекают легче, чем для пиридина:
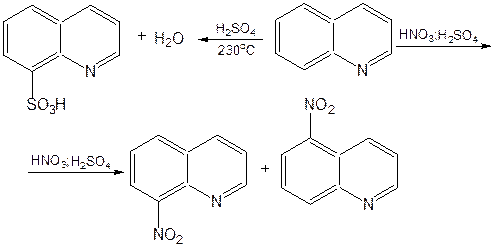
Реакции нуклеофильного замещения протекают по пиридиновому кольцу в положения 2 и 4, причем для 2- и 4-оксихинолинов возможна окси-оксо-таутомерия (оксо-форма более устойчива):
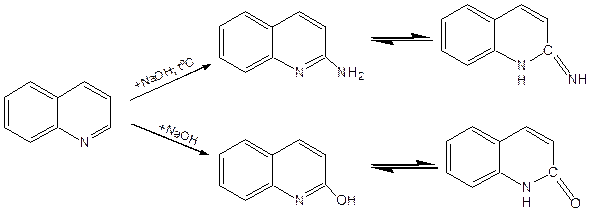
При окислении хинолина образуется 2,3-пиридиндикарбоновая (хинолиновая) кислота, т. е. окисляется бензольное кольцо. Восстановлению, наоборот, поддается пиридиновый цикл:

Ряд замещенных хинолина используется в синтезе лекарственных препаратов и красителей. 8-оксихинолин (оксин) широко применяется в качестве реагента в аналитической химии. В природе хинолиновое и изохинолиновое ядра встречаются в молекулах алкалоидов (хинин, папаверин), наркотиков (морфин, кодеин, героин и т.д.).
| <== предыдущая страница | | | следующая страница ==> |
| Пиридин | | | ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ |
Дата добавления: 2015-07-26; просмотров: 848; Нарушение авторских прав

Мы поможем в написании ваших работ!