
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
II. Пространственная изомерия
1. Конфигурационная изомерия.
1.1. Геометрическая изомерия. Характерна для соединений, имеющих в составе молекулы двойную связь или цикл и около них одинаковые атомы или группы атомов. Примеры:
1) СН3–СН=СН–СН3 бутен-2. Для этого вещества характерны два геометрических изомера:
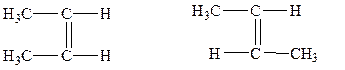
цис-бутен-2 транс-бутен-2
2) Для циклопропандикарбоновой кислоты также характерны два геометрических изомера:
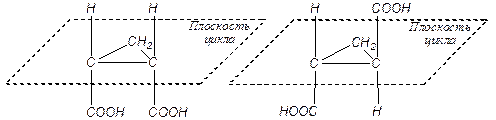
цис-циклопропандикарбоновая транс-циклопропандикарбоновая
кислота кислота
1.2. Оптическая изомерия. Характерна для соединений, имеющих в составе молекулы асимметричный атом углерода (С*), т.е. атом, у которого все 4 валентности заняты разными атомами или группами атомов. Такие молекулы способны вращать поляризованный свет. Если вещество отклоняет плоскость поляризации влево, то оно называется левовращающим (L) изомером, если вправо – правовращающим (D) изомером. Молекулы D- и L-изомеров являются зеркальным отражением друг друга. Например:

2. Конформационная изомерия. Электронная плотность s-связи между двумя sp3-гибридизованными атомами углерода распределена равномерно относительно оси связи, т.е. s-связь обладает осевой симметрией. Из этого следует, что вокруг одинарной С–С-связи возможно вращение атомов углерода. Это хорошо видно на шаростержневой модели этана. Поворот одной метильной группы относительно другой в этане происходит без нарушения химического строения молекулы, не меняются порядок связывания атомов, межатомные расстояния, величины углов между связями. Изменяется лишь взаимное расположение в пространстве атомов водорода. В случае других соединений можно говорить об изменении взаимного расположения заместителей, не связанных друг с другом ковалентными связями. Молекула может принимать при этом различные геометрические формы.
Различные геометрические формы молекулы, переходящие друг в друга путем вращения вокруг s-связей, называются конформациями.
В результате вращения вокруг s-связи между атомами углерода из множества возможных конформаций молекула этана стремится принять наиболее выгодную конформацию, обладающую наименьшей внутренней энергией. Рассмотрим из всех возможных две конформации этана. В одной из этих конформаций:

расстояние между атомами водорода двух метильных групп наименьшее, поэтому находящиеся друг против друга связи С–Н отталкиваются. Это приводит к увеличению потенциальной энергии молекулы, а следовательно, к меньшей устойчивости этой конформации. Такая конформация называется заслоненной.
В другой конформации:

атомы водорода двух метильных групп удалены на максимально возможное расстояние друг от друга. При этом электронное взаимодействие связей С–Н наименьшее и потенциальная энергия этой конформации также наименьшая. Такая конформация называется заторможенной. Она более устойчива. Разница в энергиях заслоненной и заторможенной конформаций этана составляет 10–12 кДж/моль. При обычных условиях конформации этана легко переходят друг в друга и составляют равновесную смесь. Выделить этан в виде какой-либо отдельной конформации невозможно. Существование конформаций этана обнаруживается только с помощью физико-химических методов.
Однако в случае более сложных соединений появляется реальная возможность выделения в индивидуальном состоянии отдельных, наиболее устойчивых конформаций, которые принято называть конформерами.
III. Таутомерия – вид изомерии, при которой одно и то же вещество существует в виде нескольких форм, находящихся в состоянии динамического равновесия. Примеры:
1). Кольчато-цепная таутомерия глюкозы:

a-глюкоза открытая, альдегидная b-глюкоза
форма глюкозы
2). Кето-енольная таутомерия (енолы – это соединения, содержащие в молекулах гидроксильную группу и двойную связь):
 ⇄
⇄ 
виниловый спирт уксусный альдегид
(енольная форма) (кетоформа);
 ⇄
⇄ 
кетоформа енольная форма
пептидной связи.
| <== предыдущая страница | | | следующая страница ==> |
| I. Структурная изомерия | | | Типы органических соединений по строению углеродного скелета |
Дата добавления: 2015-07-26; просмотров: 360; Нарушение авторских прав

Мы поможем в написании ваших работ!