
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Легирование сталей, как способ повышения коррозионной стойкости
Для придания сталям определенных механических свойств или коррозионной стойкости в их состав вводят легирующие элементы. Легирующие элементы образуют с железом твердые растворы, а взаимодействуя друг с другом или с примесными элементами — неметаллические включения или избыточные фазы.
Химический состав сталей соответствует стандартам, обозначаемым для различных стран-производителей следующим образом: ГОСТ — Россия (или СССР); AISI — США; B.S. — Великобритания; A.F.N.O.R. — Франция; DIN — Германия (ФРГ); SIS — Швеция, MSZ — Венгрия; CSN — Чехия (Чехословакия).
Для обозначения химического (марочного) состава сталей согласно отечественной классификации используется цифровое и буквенное обозначение. Каждому из легирующих элементов присвоена определенная буква русского алфавита: X — Сг; Η — Ni; Μ — Mo; Γ — Μn; Ю — Αl; Φ — W; С — Si; Τ — Ti; Д — Сu; Б — Nb; A — N. За буквой, обозначающей химический элемент, следует одно- или двузначное целое число, соответствующее концентрации легирующего элемента в массовых %. Первая цифра аббревиатуры, обозначающей марку стали, соответствует концентрации углерода в сотых долях масс. %.
Согласно стандартам, содержание легирующих и примесных элементов в стали каждой определенной марки колеблется в некоторых допустимых пределах.
Низколегированные стали содержат в своем составе легирующие элементы в количестве нескольких процентов, вводимых, в основном, для придания сталям определенных механических или технологических свойств.
В особую группу следует выделить коррозионностойкие стали, в состав которых обязательно входит хром в количестве 12 и более (до 30) масс.%. Стали указанной группы разработаны специально для эксплуатации в особо агрессивных условиях, что характерно для химической промышленности, где углеродистые и низколегированные стали нестойки. Классификация, номенклатура и химический состав отечественных коррозионностойких сталей представлены ГОСТ 5632-72.
Хром обладает высокой склонностью к пассивации в средах различной кислотности и анионного состава. Он устойчив также к питтинговой коррозии. Поляризационная кривая растворения хрома в серной кислоте приведена на рис. 7.2 (кривая 2). Область пассивации наступает при более отрицательном потенциале, чем у железа, а 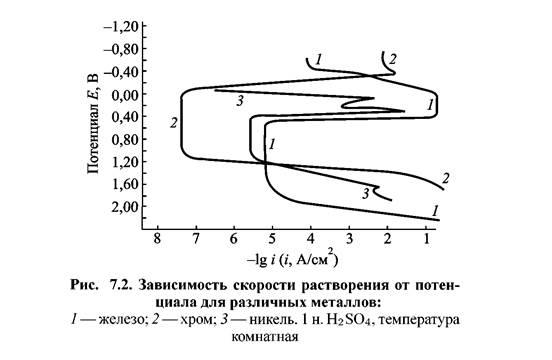
критический ток пассивации примерно на два порядка меньше. Это означает, что хром обладает более высокой склонностью к пассивности, чем железо.
Пассивность хрома обеспечивается образованием на его поверхности слоя оксида Cr2О3.
Железо и хром имеют одинаковый тип кристаллической решетки — ОЦК, с близкими параметрами решетки и дают непрерывный ряд твердых растворов (рис. 7.3). Преобладающей твердой фазой является α-фаза (феррит). При содержании менее 11,5-12% Сr при температурах не выше 865-1400 °С существует γ~фаза (аустенит). При концентрации Сг 20-75 % при температурах не выше 800-850 °С образуется σ-фаза, которая является интерметаллическим соединением Fe-Cr (рис. 7.3).
В системе Fe-Cr реализуется правило Таммана. Согласно этому правилу скачкообразное повышение устойчивости сплава происходит при доле благородных или коррозионноустойчивых атомов в сплаве, равной n/8, где n — целое число (1, 2, 3, 4, 6).
Сплавы железо-хром, содержащие 11,8 масс.% Сг, имеют в решетке твердого раствора 1/8 долю атомов Сг. При этом появляется первая граница устойчивости, характеризующаяся стойкостью сплава к холодной разбавленной ΗΝΟ3. При содержании 23,7 маc. % Сг, что соответствует 2/8 атомным долям хрома в сплаве, появляется вторая граница устойчивости, характеризующаяся стойкостью сплава в горячей разбавленной ΗΝΟ3.
Около 35,8 масс.% Сr, т.е. приблизительно при 3/8 атомных долях хрома в сплавах, появляется граница устойчивости к таким активным средам, как царская водка.
Введение хрома в железо способствует улучшению пассивируемости и увеличению устойчивости пассивного состояния сплавов Fe-Cr.
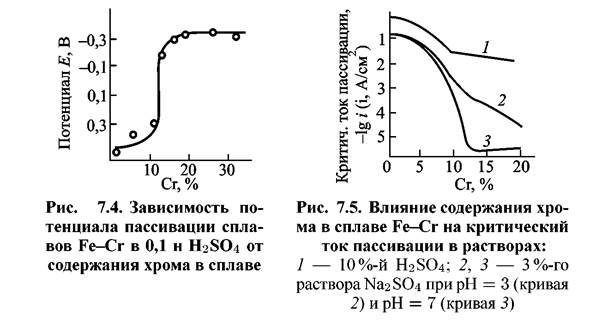
 При достижении концентрации хрома, равной 12 %, происходит смещение критического потенциала пассивации сплавов в отрицательную сторону до значения, равного Екр чистого хрома (рис. 7.4). При указанном содержании хрома происходит и резкое скачкообразное снижение критического тока пассивации, т.е. уменьшения скорости растворения металла (рис. 7.5).
При достижении концентрации хрома, равной 12 %, происходит смещение критического потенциала пассивации сплавов в отрицательную сторону до значения, равного Екр чистого хрома (рис. 7.4). При указанном содержании хрома происходит и резкое скачкообразное снижение критического тока пассивации, т.е. уменьшения скорости растворения металла (рис. 7.5).
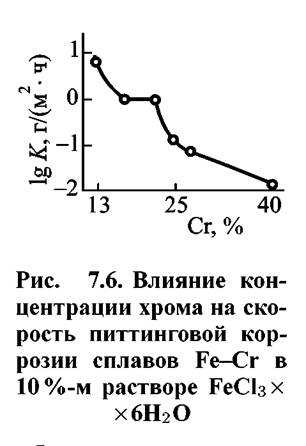
Характеристики питтингостойкости сплавов Fe-Cr также претерпевают существенное улучшение при достижении 12 % Сr (рис. 7.6).
При концентрации в сплавах 17% Сr происходит второе резкое улучшение питтингостойкости. Сплавы, содержащие более 40 % Сг, как и чистый хром, в водных средах вообще не подвергаются питтинговой коррозии.
Скачкообразное увеличение коррозионной стойкости сплавов Fe-Cr при достижении 12% Сr обусловлено происходящими при этой концентрации изменениями состава и свойств пассивирующей пленки. Так, пассивирующие слои сплавов с низким содержанием хрома состоят из оксидов желе за. Они близки по своему составу к оксидам, образующимся на поверхности чистого железа. В сплавах, содержащих более 12% Сr, внешние (контактирующие с раствором) слои пассивирующей пленки обогащены хромом, входящим в состав оксида Сг2О3.
 |
Основным недостатком хромистых сталей является их высокая склонность к хрупкому разрушению. Для преодоления этого недостатка коррозионностойкие стали легируют никелем. Благодаря высокой прочности, пластичности и коррозионной стойкости никель используют и как основу для изготовления коррозионностойких конструкционных материалов.
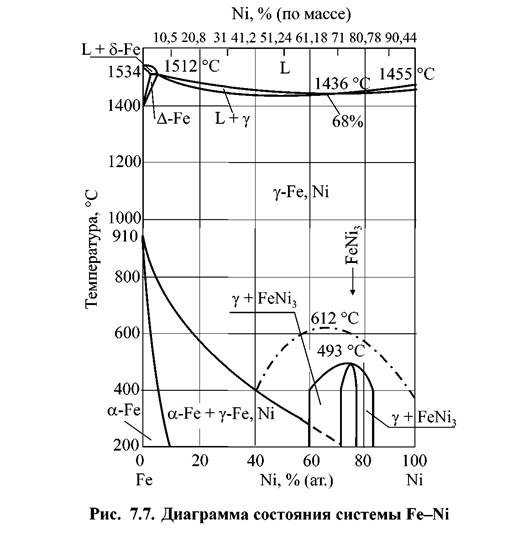
Так же, как и хром, при температурах, близких к температуре плавления, никель образует с железом непрерывный ряд твердых растворов, имеющих, однако, ГЦК решетку (рис. 7.7). При снижении температуры γ~твердый раствор распадается на а + 7· Равновесная концентрация Ni в α-твердом растворе достигает ~ 7,5% . При концентрации в сплаве ~ 74 % никеля происходит образование интерметаллического соединения FeNi3. Никель снижает скорость диффузии углерода в кристаллической решетке сплавов на основе железа, тем самым препятствуя выделению карбидной фазы.
Электрохимическое поведение никеля в активном состоянии во многом сходно с рассмотренным ранее поведением железа. Пассивность обеспечивается образованием на поверхности защитного слоя, состоящего из NiO (подслой толщиной ~ 4 Аo, прилегающий к металлу) и Ni(OH)2 (подслой толщиной ~ 6 А, контактирующий с электролитом).
Введение в сталь никеля способствует не только улучшению механических свойств вследствие аустенизации структуры, но и облегчает пассивацию и повышает устойчивость пассивного состояния, в том числе в средах, провоцирующих развитие таких локальных коррозионных процессов как питтинговая и щелевая коррозия. Повышение коррозионной стойкости сталей вследствие легирования их никелем не связано с изменением состава и свойств пассивирующей пленки — никель в составе пассивирующих пленок не обнаружен.
Недостатком хромоникелевых аустенитных сталей является их низкая стойкость портив коррозионного растрескивания, минимум которой приходится на наиболее широко распространенные стали типа 18Cr-8Ni.
Более 70 % всех производимых нержавеющих сталей являются сталями аустенитного класса, содержащими 17% хрома и свыше 10 % никеля.
Для большего повышения коррозионной стойкости в состав хромоникелевых нержавеющих сталей вводят молибден. Молибден улучшает пассивируемость сталей в неокислительных средах, сужая область активного растворения, и способствует существенному снижению их склонности к питтинговой и щелевой коррозии за счет затруднения питтингообразования, облегчения репассивации, снижения скорости растворения металла в очагах локальной коррозии и увеличения индукционного периода.
Молибден и вольфрам имеют ОЦК кристаллическую решетку и обладают ограниченной растворимостью в железе.
Увеличение устойчивости пассивного состояния хромоникельмолибденовых сталей объясняется вхождением молибдена в состав пассивирующих слоев. Предполагается, что при потенциалах пассивной области сталей, где молибден подвергается перепассивации, то есть растворяется с образованием молибдат-ионов, происходит образование смешанных оксидов хрома и молибдена, обладающих более высокими защитными свойствами, чем оксид хрома.
Основным недостатком хромоникельмолибденовых сталей является их низкая стойкость в окислительных средах. Для придания хромистым и хромоникелевым сталям высоких прочностных характеристик их дополнительно легируют вольфрамом. Кроме улучшения механических свойств вольфрам, подобно молибдену, увеличивает коррозионную стойкость сталей, однако его действие оказывается не столь эффективным.
Углерод является необходимым легирующим элементом в сталях мартенситного класса (стали 30X13, 40X13, 95X18 и др.), где он обеспечивает высокие прочностные характеристики. В сталях других структурных типов углерод является вредной примесью. Так, он образует карбиды хрома (типа Сr23С6), что снижает содержание хрома в сплаве.
Марганец в концентрациях 6-9 % в комбинации с никелем обеспечивает по сравнению с хромоникелевыми сплавами более высокий предел растворимости углерода и азота, повышенную стабильность аустенита.
Азот является сильным аустенитообразующим элементом. Он очень полезен в аустенитных и аустенито-ферритных сталях. Азот упрочняет твердый раствор сильнее, чем углерод, повышает стойкость против питтинговой коррозии, замедляет выделение карбидных и интерметаллидных фаз. Однако, присутствие азота в сталях ферритного класса нежелательно, так как он отрицательно влияет на их механические свойства.
Медь, введенная в стали, повышает их стойкость в минеральных кислотах.
Титан и ниобий образуют карбиды TiC и NbC и тем самым удаляют углерод из твердого раствора. При их введении в сталь повышается стойкость сталей против локальных видов коррозии.
Элементы S, Pb, Se вводят в сплавы для повышения механической обрабатываемости. А1 и Si повышают жаростойкость, микродобавки редких металлов (бор и цирконий) улучшают механические свойства.
Таким образом, важнейшим направлением повышения коррозионной стойкости конструкционных материалов является противокоррозионное легирование.
Регулирование фазового состава сталей. Реальные стали являются гетерогенными системами, содержащими в твердом растворе — металлической матрице — посторонние фазы (так называемые избыточные фазы и неметаллические включения). Избыточные фазы (к ним относят карбиды, нитриды, силициды, бориды) и неметаллические включения (оксиды и сульфиды) образуются в результате взаимодействия примесных и легирующих элементов сталей и отличаются от металлической матрицы химическим составом, кристаллической структурой и электрохимическими характеристиками. Несмотря на относительно небольшое количество (от сотых до десятитысячных долей масс.%) посторонние фазы вносят свой вклад в интегральную скорость анодного и катодного процессов и характер растворения металла.
| <== предыдущая страница | | | следующая страница ==> |
| Стали и чугуны | | | Жаростойкие сплавы на основе железа |
Дата добавления: 2015-07-26; просмотров: 473; Нарушение авторских прав

Мы поможем в написании ваших работ!