
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
ХАРАКТЕРИСТИКА РАСТВОРОВ
РАСТВОРЫ
Растворы широко распространены в природе и имеют важное значение в химической технологии. С молекулярно-кинетической точки зрения раствор - гомогенная смесь, состоящая из нескольких веществ, находящихся в стадии молекулярного раздробления. С точки зрения правила фаз раствором называется двух или многокомпонентная гомогенная часть системы, состав которой может произвольно меняться в границах, определяемой растворимостью веществ. В этих определениях подчеркивается два основных признака раствора - его гомогенность и переменность состава.
Растворы отличаются от химических соединений также характером и величинами энергии связи между частицами. Химическое соединение образуется за счет мощных валентных связей (130 – 630 (кдж/моль), а раствор, главным образом, за счет гораздо более слабого межмолекулярного взаимодействия (2 - 40 кдж/моль).
В зависимости от агрегатного состояния различают следующие типы истинных растворов:
1. Г + Г (воздух)
2. Г + Ж (р-р кислорода в воде)
3. Г + Т (р-р водорода в платине)
4. Ж + Ж (р-р глицерина в воде)
5. Ж + Т (р-р канифоли в спирте)
6. Т + Т (металлические сплавы)
Важнейшей характеристикой раствора является его концентрация.
1.Массовая доля , %
gi = 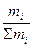 i 100
i 100
2. Объемная доля, %
ji = 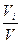 100
100
3.Молярность, моль/л - количество молей i - того компонента на 1 литр раствора.
ci = 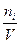 =
= 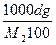
4.Моляльность , количество молей i- того компонента в 1000 г. растворителя.
mi = 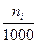 =
= 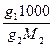
5.Нормальность, г-экв/л , количество г-эквивалентов на 1 литр раствора.
CN = 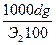
6. Мольная доля - отношение числа молей данного компонента к общему числу молей всех компонентов в растворе.
Ni = 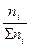 =
= 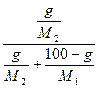
| <== предыдущая страница | | | следующая страница ==> |
| ТРЕХКОМПОНЕНТНЫЕ СИСТЕМЫ | | | ЗАКОН РАУЛЯ |
Дата добавления: 2014-03-11; просмотров: 423; Нарушение авторских прав

Мы поможем в написании ваших работ!