
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Многоатомные спирты
|
Читайте также: |
Атомность спиртов определяется количеством гидроксильных групп. Двухатомные спирты содержат две гидроксильные группы и носят общее название диолы или гликоли. Трехатомные спирты называют триолами или глицеринами. Простейшие и наиболее важные представители диолов и триолов – этиленгликоль и глицерин.
Этиленгликоль (этандиол-1,2).
Этиленгликоль получают из этилена по следующим схемам:
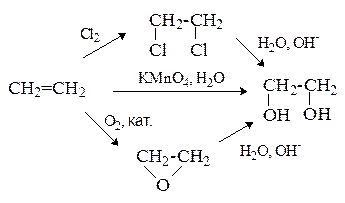
Химические свойства этиленгликоля аналогичны свойствам одноатомных спиртов. Однако есть ряд специфических свойств, обусловленных присутствием двух гидроксильных групп.
Этиленгликоль (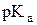 =15,1) является более сильной кислотой, чем одноатомные спирты и образует в водных растворах комплексные алкоголяты с ионами тяжелых металлов.
=15,1) является более сильной кислотой, чем одноатомные спирты и образует в водных растворах комплексные алкоголяты с ионами тяжелых металлов.
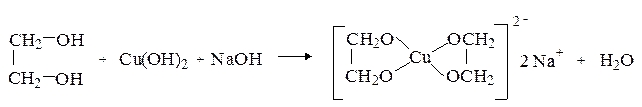
Появляющееся при этом ярко-синее окрашивание позволяет использовать реакцию как качественную на виц-диольный фрагмент.
При дегидратации этиленгликоля в зависимости от условий реакции образуются разные продукты. При нагревании в присутствии серной кислоты происходит межмолекулярная дегидратация с образованием циклического простого эфира – диоксана. Нагревание с хлоридом цинка дает продукт внутримолекулярной дегидратации – ацетальдегид.
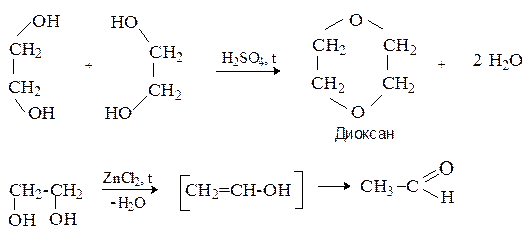
Этиленгликоль легко окисляется. В зависимости от природы окислителя могут образоваться гликолевый альдегид, глиоксаль, глиоксиловая кислота, щавелевая кислота.
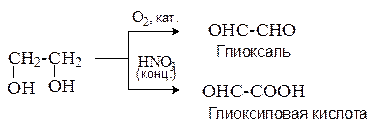
Этиленгликоль используется для приготовления антифризов; для получения растворителей (простые эфиры этиленгликоля, диоксан) и полимеров (полиэфиров).
Глицерин (1,2,3- пропантриол).
Глицерин ранее получали гидролизом жиров, но в настоящее время его получают синтетическим путем из пропилена.
Глицерин дает все реакции, известные для спиртов. Наличие трех гидроксильных групп обусловливает некоторые специфические свойства.
Глицерин (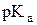 =14) является более сильной кислотой, чем одноатомные спирты и, подобно этиленгликолю, образует хелатные комплексы с ионами металлов.
=14) является более сильной кислотой, чем одноатомные спирты и, подобно этиленгликолю, образует хелатные комплексы с ионами металлов.
При дегидратации глицерина образуется ненасыщенный альдегид акролеин.
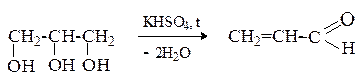
Мягкое окисление глицерина дает смесь глицеринового альдегида и дигидроксиацетона.
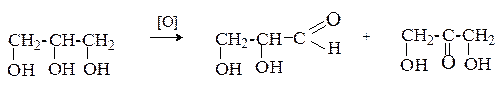
Важное значение имеют сложные эфиры глицерина. При действии на глицерин азотной кислоты в присутствии серной кислоты образуется тринитрат глицерина (нитроглицерин).
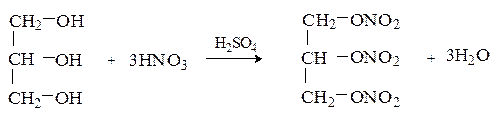
Нитроглицерин используется в производстве взрывчатых веществ. В малых концентрациях нитроглицерин применяется как сосудорасширяющее средство.
При действии на глицерин фосфорной кислоты образуется смесь a- и b-глицерофосфатов.
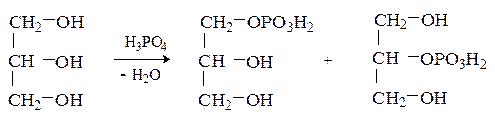
Глицерофосфаты являются структурными компонентами фосфолипидов (см.18.1.3) .
Сложные эфиры глицерина и высших жирных кислот – основная составная часть природных жиров и масел (см. 18.1.2).
Примерами многоатомных спиртов, содержащих четыре, пять и шесть гидроксильных групп, могут служить соответственно эритриты, пентиты и гекситы, которые образуются при восстановлении моносахаридов(см.17.1.5).
| <== предыдущая страница | | | следующая страница ==> |
| Химические свойства. Реакции спиртов определяются присутствием группы ОН и протекают по следующим основным направлениям | | | Фенолы. Классификация и номенклатура |
Дата добавления: 2014-04-24; просмотров: 1068; Нарушение авторских прав

Мы поможем в написании ваших работ!