
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
АТОМНО-КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ И СПЛАВОВ. ДИАГРАММЫ СОСТОЯНИЙ
В твердом состоянии атомы металлов и сплавов образуют правильную пространственную кристаллическую решетку. Наибольшее распространение имеют кубическая объемно центрированная, кубическая гранецентри-рованная и гексагональная решетки (рисунок 18.1).
Пространственные кристаллические решетки образуются при переходе металла из жидкого состояния в твердое, т. е. кристаллизации. Каждый металл кристаллизуется при строго индивидуальной температуре.
Некоторые металлы в затвердевшем состоянии при разной температуре обладают способностью изменять кристаллическую структуру. Это явление называется аллотропическим превращением. Оно сопровождается выделением или поглощением теплоты. Железо имеет четыре аллотропические формы: α-Fe, β-Fe, γ-Fe, δ-Fe. Практическое значение имеют α-Fe и β -Fe Отличие δ -Fe и β -Fe от α -Fe состоит в величине межатомного расстояния и в β -Fe отсутствуют магнитные свойства.

|
| Рисунок 18.1 – Основные виды элементарных ячеек кристаллических решеток металлов: а– объемно центрированная кубическая; б– гранецентрированная кубическая; в – гексагональная |
Кривая охлаждения чистого железа (рисунок 18.2) показывает, что при температуре 1539 °С железо переходит из жидкого состояния в твердое, кристаллизуясь в виде δ-Fe с решеткой объемно центрированного куба. Дальнейшие кристаллические превращения будут происходить в твердом состоянии. При температуре 1401 °С происходит превращение железа в 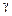 -Fe с кубической гранецентрированной решеткой, которая при 898 °С переходит в α-Fe с кубической объемно центрированной решеткой. Далее при температуре 768 °С α-Fe приобретает магнитные свойства.
-Fe с кубической гранецентрированной решеткой, которая при 898 °С переходит в α-Fe с кубической объемно центрированной решеткой. Далее при температуре 768 °С α-Fe приобретает магнитные свойства.
При совместной кристаллизации нескольких элементов образуются сплавы в виде механических смесей, твердых растворов, химических соединений.
 Механические смеси получаются при раздельной кристаллизации составляющих. Каждый компонент сохраняет свои свойства. Свойство сплава будет средним между элементами, входящими в его состав.
Механические смеси получаются при раздельной кристаллизации составляющих. Каждый компонент сохраняет свои свойства. Свойство сплава будет средним между элементами, входящими в его состав.
 Твердые растворы бывают растворами замещения и внедрения. В твердом растворе замещения атомы одного компонента частично замещаются атомами другого в узлах его кристаллической решетки. Они образуются при совместной кристаллизации металлов. В твердом растворе внедрения атомы одного из компонентов размещаются в междоузлиях (пустотах) кристаллической решетки другого. Они образуются при совместной кристаллизации металла и неметалла.
Твердые растворы бывают растворами замещения и внедрения. В твердом растворе замещения атомы одного компонента частично замещаются атомами другого в узлах его кристаллической решетки. Они образуются при совместной кристаллизации металлов. В твердом растворе внедрения атомы одного из компонентов размещаются в междоузлиях (пустотах) кристаллической решетки другого. Они образуются при совместной кристаллизации металла и неметалла.
Химические соединения образуются при химическом взаимодействии компонентов. Например, в сплавах железа с углеродом получается карбид железа (цементит) 3Fe + С = Fe3C.
Зависимость между строением сплава, его составом и температурой описывается диаграммами состояния. Они строятся экспериментально по критическим точкам на кривых охлаждения сплавов. По диаграммам можно определить механические, физические и химические свойства сплавов, что позволяет назначать режимы термической обработки, сварки, обработки давлением.
Имеются основные типы диаграмм состояний (рисунки 18.3–18.5). Диаграммы состояний I типа относятся к сплавам, когда их компоненты А и В неограниченно растворяются друг в друге в жидком состоянии и не растворяются в твердом.
Такой является диаграмма состояний сплава свинец-сурьма (см. рисунок 18.3).
 |
Рисунок 18.3 – Кривые охлаждения и диаграмма состояния сплавов свинца и сурьмы
На кривых охлаждения чистых металлов имеется по одной критической точке, соответствующей переходу металлов из жидкого состояния в твер-
дое. Для свинца – 327 °С (точка А) и для сурьмы – 631 °С (точка В). Ниже этих точек свинец и сурьма находятся в твердом состоянии. На кривых охлаждения сплавов Pb–Sb имеется две критические точки – начала и конца их затвердевания (точка С – конец затвердевания свинца и сурьмы). Чистые металлы состоят из однородных зерен. Кривые охлаждения сплавов отличаются от кривых затвердевания чистых металлов. Вначале из расплавленной массы выделяется один из компонентов, а затем, после достижения определенной концентрации, происходит окончательное затвердевание металла.
|

Затвердевание сплавов Pb-Sb при количестве Sb менее 13 % начинается при температурах, соответствующих верхним критическим точкам с выпадением кристаллов свинца. С понижением температуры их содержание увеличивается, а оставшийся расплав обогащается сурьмой. При 245 °С (нижние критические точки) содержание сурьмы достигает 13 % и при последующем охлаждении происходит одновременная кристаллизация свинца и сурьмы. Образуется эвтектика – механическая равномерно распределенная смесь кристаллов свинца и сурьмы. Если сурьмы содержится больше 13 %, затвердевание сплавов начинается с образования кристаллов сурьмы, при достижении ее концентрации 13 % затвердевание происходит с образованием эвтектик.
При построении диаграммы состояний сплавов верхние и нижние критические точки переносят на координатные оси температура – состав сплава. Линия АСВ, соединяющая критические точки начала затвердевания, называется ликвидусом. Линия DCE, соединяющая точки конца затвердевания, называется солидусом. В точке С линии ликвидуса и солидуса пересекутся. Сплав, отвечающий этой точке, будет самым легкоплавким из всех возможных сплавов РЬ и Sb. Он называется эвтектическим.
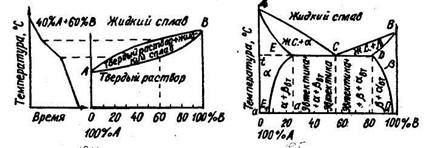
По диаграмме состояний II типа (см. рисунок 18.4) затвердевают сплавы с неограниченной растворимостью как в жидком, так и в твердом состоянии.
По диаграмме состояний III типа (см. рисунок18.5) затвердевают сплавы с неограниченной растворимостью в жидком виде и ограниченной – в твердом. Они не образуют химических соединений.
На рисунке 18.6 приведена диаграмма состояний сплавов железо-цементит.

|
Углерода в цементите – 6,67 %. При большем его количестве сплавы приобретают повышенную хрупкость и практического применения не имеют.
По диаграмме судят о структуре медленноохлажденных сплавов и их эксплуатационных свойствах. Изменяя режимы нагрева и охлаждения, получают различные структуры железоуглеродистых сплавов, отличающихся по механическим свойствам.
Феррит – твердый раствор углерода в α-Fe. Он содержит при 723 °С примерно 0,02 % и при 20 °С примерно 0,006 % углерода. Пластичен; твердость 60–80 НВ; по свойствам близок к чистому железу.
Цементит (карбид железа Fe3C) – химическое соединение с содержанием углерода 6,67 %. Температура его плавления 1600 °С, твердость около 800 НВ. Очень хрупок, при нагреве распадается.
Аустенит – твердый раствор внедрения углерода в γ-Fe. При 1147 °С может содержать углерода до 2,14 %, при 727 °С – 0,8 %. Твердость 170–200 НВ.
Перлит – эвтектоидная смесь феррита и цементита, содержащая 0,83 % углерода. Она образовалась в результате распада аустенита при 723 °С.
Ледебурит – эвтектическая смесь аустенита и цементита с содержанием углерода 4,3 %. Образовалась при 1130 °С. При охлаждении аустенит, входящий в состав ледебурита, распадается на вторичный цементит и перлит. Имеет высокую твердость 700 НВ, хрупкий.
Графит – разновидность углерода. Мягкий, хрупкий. Встречается в серых и ковких чугунах.
Железоуглеродистые сплавы со строением, приведенным на диаграмме, подразделяются на стали и белые чугуны. Стали содержат углерода до 2,14 %, чугуны – более 2,14 %.
При содержании углерода до 0,83 % стали называются доэвтектоидны-ми, при – 0,83 % – эвтектоидными, при 0,83–2,14 % – заэвтектоидными. Чугуны при содержании углерода от 2,14 до 4,3 % называются доэвтектиче-скими, при 4,3–6,7 % – заэвтектическими.
Стали затвердевают при температурах, ограниченных линиями ликвидуса АС и солидуса АЕ. Из жидкого сплава кристаллизуется аустенит.
Чугун с содержанием углерода 4,3 % затвердевает при температуре немного ниже 1147 °С. При этом образуется эвтектика, состоящая из максимально насыщенного углеродом аустенита (2,14 %) и цементита и называемая ледебуритом.
Затвердевание заэвтектических чугунов с содержанием углерода от 4,3 до 6,67 % начинается по линии ликвидуса CD. Вначале из жидкого сплава выделяются тонкие пластинчатые кристаллы первичного цементита. При этом, с понижением температуры по линии ликвидуса CD, в жидкости уменьшается количество углерода. При 1147 °С концентрация углерода становится 4,3 % и сплав затвердевает с образованием ледебурита.
Дальше линии солидуса AECF превращения происходят в твердом состоянии из-за полиморфизма железа и разной растворимости углерода в нем при понижении температуры.
При 910 °С γ-модификация железа должна переходить в α-модифи-кацию. В кристаллической решетке γ-Fe содержится углерод, поэтому при медленном охлаждении при 727 °С в сплаве еще остается аустенит с содержанием углерода 0,83 %. При дальнейшем понижении температуры при распаде аустенита образуются феррит и цементит.
Линия GS на диаграмме состояний сплавов представляет собой критические точки начала образования феррита. При большем содержании углерода перекристаллизация γ-Fe в α-Fe происходит при более низкой температуре. При температуре ниже 727 °С аустенит распадается с образованием перлита. Линия РК называется линией перлитовых превращений. Ниже этой линии доэвтектоидные стали состоят из феррита и перлита.
При охлаждении заэвтектоидных сталей по линии ES из твердого раствора (аустенита) выделяется цементит. Его называют вторичным аустени-том в отличие от первичного аустенита, образующегося из жидкого раствора при содержании в сплаве более 4,3 % углерода. На линии перлитовых превращений в аустените содержится 0,8 % углерода, который при последующем охлаждении распадается с образованием перлита.
|

|
| |||
|
По линии GPQ происходит изменение растворимости углерода в α-Fe при снижении температуры. Из феррита выделяется углерод, химически взаимодействующий с железом, который называется третичным. Растворимость его при 0 °С – 0,006 %.
Вышеприведенная диаграмма сплавов Fe–Fe3C получена при их медленном охлаждении. При быстром же охлаждении феррит или цементит не успевают полностью выделиться из аустенита к моменту образования перлита. Аустенит распадается частично, а при особых условиях вообще не распадается, в остывшей стали можно получить структуру аустенита.
Структурами распада аустенита являются мартенсит, троостит и сорбит.
Мартенсит представляет собой твердый раствор углерода в α-Fe с искаженной решеткой. Образуется при очень быстром охлаждении. Имеет игольчатую структуру, твердость 600–700 НВ. Мартенситовая структура характерна для закаленных сталей.
Троостит – дисперсная смесь частиц цементита и феррита и представляет следующую стадию распада аустенита. Встречается в виде неправильных участков игольчатого строения и сопровождается образованием мартенсита и сорбита. Образуется путем умеренной закалки стали на мартенсит. Твердость 350–500 НВ.
Сорбит представляет собой переходную структуру между трооститом и перлитом. Она получается более ускоренным, по сравнению с перлитом, охлаждением стали или отпуском закаленной стали при 500–600 °С. Его твердость 250–350 НВ.
| <== предыдущая страница | | | следующая страница ==> |
| Металлические материалы и изделия | | | МЕХАНИЧЕСКИЕ СВОЙСТВА И ИСПЫТАНИЯ МЕТАЛЛОВ |
Дата добавления: 2014-09-29; просмотров: 900; Нарушение авторских прав

Мы поможем в написании ваших работ!