
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Титранты и стандартные вещества
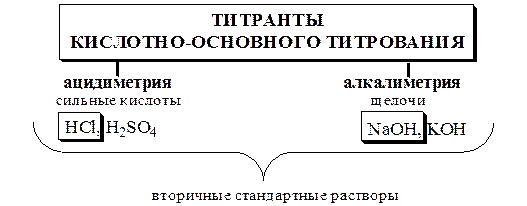

Стандартизацию растворов титрантов можно проводить также с помощью вторичных стандартных веществ. Cтандартные растворы можно готовить из фиксаналов.
Стандартные растворы HCl и H2SO4 устойчивы при хранении. Их хранят при обычных условиях в закрытой посуде. Растворы щелочей поглощают CO2 из воздуха, поэтому их следует хранить в плотно укупоренной таре. Для предотвращения взаимодействия щёлочи и CO2 растворы защищают с помощью трубки, заполненной оксидом кальция или натронной известью. Исходный образец щёлочи, например, NaOH может содержать некоторое количество карбоната в качестве примеси. Для того чтобы получить раствор, свободный от этой примеси, поступают следующим образом: в свежепрокипячённой воде растворяют определённую навеску NaOH, так чтобы получился концентрированный раствор этого вещества. Полученный раствор оставляют на некоторое время в плотно укупоренной посуде. Карбонат натрия плохо растворим в концентрированном растворе NaOH и выпадает в виде осадка. Через некоторое время прозрачный раствор сливают с осадка и разбавляют до необходимой концентрации свежепрокипячённой водой.
Растворы щелочей, особенно концентрированные, не рекомендуется хранить в стеклянной посуде.
13.2. Обнаружение конечной точки титрования. Кислотно-основные индикаторы
Индикатором (лат. indicator - указатель) называется вещество, видимо изменяющее свои свойства (окраску, люминесценцию, растворимость) при изменении концентрации какого-либо компонента в растворе. У правильно выбранного индикатора изменение окраски должно происходить в точке эквивалентности или вблизи неё.
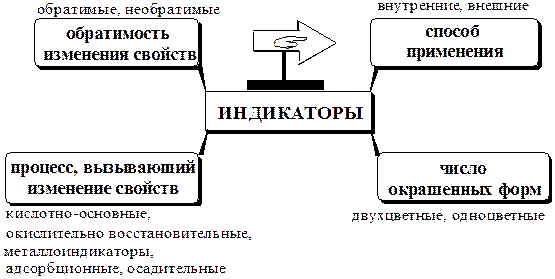
Кислотно-основные индикаторы - слабые органические кислоты или основания, кислотная (протонированная) и основная формы которых отличаются по окраске или флуоресценции, т.е. вещества, окраска или флуоресценция которых зависят от рН.
В качестве кислотно-основных индикаторов при титровании в водных растворах наиболее широко используются:

Метиловый оранжевый представляет собой двухцветный индикатор. Его основная форма окрашена в жёлтый цвет, а кислотная (протонированная) - в красный.
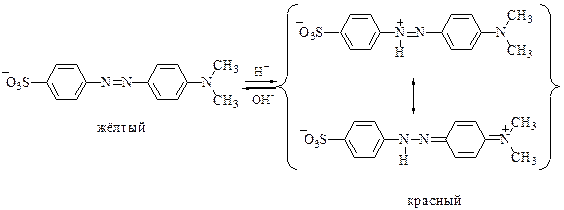
У протонированной формы степень делокализации электронной плотности выше и поэтому меньше разность энергий основного и возбуждённого состояния. Вследствие этого кислотная форма поглощает электромагнитное излучение видимого диапазона с большей длиной волны (меньшей энергией), чем основная.
Изменение окраски метилового оранжевого и любых других кислотно-основных индикаторов происходит в определённом интервале рН, называемом интервалом перехода окраски индикатора.
HInd+ + H2O › Ind + H3O+
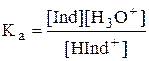
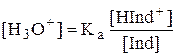
В среднем, человеческий глаз замечает изменение окраски, когда концентрация одной окрашенной формы становится в 10 раз больше, чем другой.
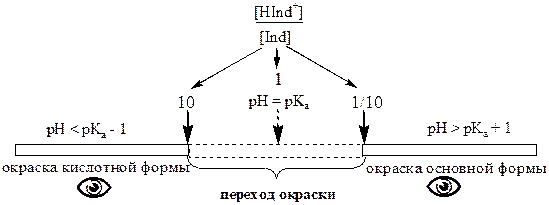
pHперехода = pKa ± 1
Границы интервала pKa ± 1 соблюдаются лишь в том случае, если интенсивность окраски обеих форм одинакова. В действительности это обычно не так. У метилового оранжевого pKa = 3,36, а интервал перехода окраски - 3,1-4,6. Это объясняется тем, что протонированная форма имеет больший молярный коэффициент светопоглощения и для того, чтобы окраска раствора индикатора соответствовала окраске кислотной формы, достаточно, чтобы её концентрация не в 10, а всего лишь в ~ 2 раза превышала концентрацию основной формы.
Значение рН, при котором заканчивают титрование с данным индикатором, называется показателем титрования (для данного индикатора) - рТ.
Величина показателя титрования находится примерно в середине интервала перехода окраски индикатора, например, у метилового оранжевого рТ » 4.
Интервал перехода окраски индикаторов зависит от:
· температуры;
· ионной силы;
· присутствия в растворе посторонних веществ (например, этанола), влияющих на кислотно-основные свойства индикатора.
У метилового оранжевого и других двухцветных индикаторов интервал перехода не зависит от концентрации индикатора в растворе.
| <== предыдущая страница | | | следующая страница ==> |
| ГЛАВА 13 | | | Метиловый красный |
Дата добавления: 2014-10-10; просмотров: 355; Нарушение авторских прав

Мы поможем в написании ваших работ!