
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Церулоплазмин (ЦП)
ЦП — медьсодержащий гликопротеид, относящийся к α2-глобулиновой фракции плазмы крови млекопитающих животных и человека. Выполняет в организме ряд важных биологических функций: повышает стабильность клеточных мембран; участвует в иммунологических реакциях; ионном обмене; оказывает антиоксидантное действие; тормозит перекисное окисление липидов; стимулирует гемопоэз.
Роль церулоплазмина в транспорте самой меди не очень значительна, поскольку оборот меди в нем медленный (основную роль в транспорте меди играют альбумин и транскупреин). Основной физиологической функцией ЦП является его способность окислять различные биологические субстраты по оксидазному механизму. ЦП эффективно окисляет ионы двухвалентного железа, аскорбиновую кислоту, фенол, амины, катехолы, проявляя при этом одновременно феррооксидазную, аскорбатоксидазную и аминоксидазную активность.
ЦП усиливает связывание ионов железа с трансферрином, а в случае их высокой концентрации в плазме крови - и с ферритином. В крови церулоплазмин совместно с трансферрином образует главную антиоксидантную систему, контролирующую процессы ПОЛ, индуцированные ионами двухвалентного железа. Действуя как ферроксидаза, церулоплазмин выполняет важнейшую роль в регуляции ионного состояния железа - окислении Fe2+ в Fe3+. Это делает возможным включение железа в трансферрин без образования токсических продуктов железа. Поддержание нормального транспорта и метаболизма железа – жизненно важная функция церулоплазмина.
Окисляя Fe2+ до Fe3+, ЦП может препятствовать образованию OH* радикалов при взаимодействии Fe2+ c H2O2, в реакции Фентона:
Fe2+ + H2O2 Fe3+ + OH- + OH*
Способствуя встраиванию в ферритин окисленного Fe3+, ЦП ингибирует супероксидное и ферритин-зависимое перекисное окисление липидов (ПОЛ). Описанные выше свойства ЦП послужили основой для объяснения его противовоспалительной активности, что вместе с быстрым возрастанием концентрации ЦП (в 2-3 раза) в русле крови уже в начале воспалительной реакции позволяет причислить его к белкам “острой фазы”. Показано, что ЦП может выступать как фактор роста, вследствие антиоксидантных свойств.
Церулоплазмин является наиболее сильным ингибитором образования гипогалоидов в системе миелопреоксидаза-перекись водорода-ионы хлора. Ионы хлора выступают в роли естественных регуляторов каталитической активности церулоплазмина, многократно повышая ее при нейтральных значениях рН и существенно снижая при рН< 6. В физиологических условиях церулоплазмин на порядок более эффективно захватывает OCl- , чем трансферрин, альбумин, СОД.
ЦП применяется в медицинской практике в качестве медицинского препарата, он используется как основной антиоксидант крови, стимулятор гемопоэза, уменьшающий интоксикацию и иммунодепрессию.
Металлотионеины (МТ) – еще один класс соединений, обеспечивающих эффективное ингибирование свободнорадикальных процессов. Металлотионеины представляют собой низкомолекулярные белки, содержащие до 30% цистеина и способные связывать ионы тяжелых металлов. Синтез металлотеининов индуцируется под влиянием различных химических и физических факторов. Функции металлотеининов до конца не выяснены, хотя доказана их роль в снижении токсичности тяжелых металлов и в регуляции уровней цинка и меди в организме. Весьма вероятно также участие этих белков в защите биологических объектов от окислительного стресса.
«Ловушки» гидроксильных радикалов. Маннит, ксилит, сорбит, сахароза и другие многоатомные спирты, бензойная кислота, мочевая кислота, диметилсульфоксид ингибируют ПОЛ, связывая гидроксильные радикалы. Содержание мочевой кислоты в крови человека довольно значительное, поэтому некоторые авторы полагают, что на ее долю приходится не менее половины эффекта защиты липопротеидов крови от свободнорадикального окисления и не менее 10-15% ингибирования гидроксильных радикалов. Реакция мочевой кислоты с гидроксильными радикалами приводит либо к отрыву атома водорода и образованию гидроперекиси, либо, если ОН-радикал присоединяется к мочевой кислоте, к конформационной перестройке ее молекулы с образованием аллантоина, который подвергается дальнейшему окислению.
Гормоны – антиоксиданты. Некоторые гормоны, в частности, эстрогены и мелатонин, кроме своей основной функции способны влиять на интенсивность свободнорадикальных окислительных процессов как в условиях физиологической нормы, так и при развитии патологии.
Многочисленными исследованиями показано, что у женщин различных возрастных групп, активность процессов свободнорадикального окисления и содержание в сыворотке крови продуктов ПОЛ, ниже чем, у мужчин соответствующего возраста.
Некоторые авторы связывают меньший риск развития атеросклероза и большую продолжительность жизни женщин по сравнению с мужчинами с выраженными антиоксидантными свойствами женских половых гормонов – эстрогенов. Полагают, что антиокислительная активность эстрогенов обусловлена наличием в их структуре фенольной гидроксильной группы.
Мелатонин – синтезируется в эпифизе на основе серотонина. Мелатонин эффетивно нейтрализует гидроксильный радикал, супероксидный анион-радикал, пероксинитрит, гидроперекисные радикалы, синглетный кислород. Было показано, что мелатонин активно защищает от свободнорадикального повреждения липиды и нуклеиновые кислоты, обладает антиканцерогенным и радиопротекторным действием, предотвращает развитие аллоксан-индуцированного диабета и возрастных патологий. На различных моделях ишемии/реперфузии, острого и хронического воспаления у животных, а также в клинических условиях мелатонин проявлял выраженный защитный и противовоспалительный эффекты. Вероятно, антирадикальная активность обусловлена нейтрализацией гидроксильного радикала благодаря наличию в его структуре метокси-группы (рис.13).
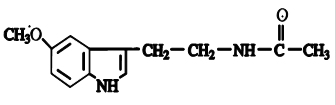
Рис.8. Строение мелатонина
Установлена также способность мелатонина повышать активность антиоксидантных глутатион-зависимых ферментов, глюкозо-6-фосфатдегидрогеназы и супероксиддисмутазы.
| <== предыдущая страница | | | следующая страница ==> |
| АНТИОКСИДАНТЫ НЕФЕРМЕНТАТИВНОЙ ПРИРОДЫ | | | Ферментные системы антиоксидантной защиты |
Дата добавления: 2014-10-17; просмотров: 508; Нарушение авторских прав

Мы поможем в написании ваших работ!