
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Задача 6
1. В условиях промышленного производства и в аптеках готовят лекарственные средства с лекарственным веществом следующей структуры:

При оценке качества лекарственного вещества в образцах одной серии показатель «Прозрачность и цветность раствора» не отвечал требованиям НД. Дайте обоснование причинам изменения его качества по данному показателю в соответствии со свойствами. Предложите испытания для характеристики его качества.
• Приведите русское, латинское и рациональное название препарата. Охарактеризуйте физико-химические свойства (внешний вид, растворимость, спектральные характеристики) и их использование для оценки качества.
• В соответствии с химическими свойствами предложите реакции идентификации и методы количественного определения. Напишите уравнения реакций.
2. Проведите сравнительную характеристику каллусных и суспензионных культур при использовании их в качестве субстрата для получения БАВ биотехнологическими методами.
3. Обоснуйте требования к глазным лекарственным формам и условиям их промышленного производства. Укажите критерии выбора вспомогательных веществ, входящих в состав глазных капель, объясните их назначение, приведите примеры.
• Обоснуйте последовательность и содержание технологических стадий получения глазных капель.
• Как обеспечивается одно из основных требований - стерильность (методы стерилизации и принцип работы стерилизующего оборудования)? Как контролируется этот показатель в соответствии с требованиями ГФ XI и другими нормативными документами ОЭР (принципы анализа)?
4. В каком помещении аптеки осуществляют процесс изготовления глазных капель? Какие другие лекарственные формы требуют аналогичных условий изготовления? Ответ обоснуйте.
5. Процесс изготовления стерильных лекарственных форм связан с использованием дистилляционно-стерилизационного оборудования - источника повышенной опасности.
• Кто в фармацевтических организациях отвечает за охрану труда?
• Каков порядок проведения и документального оформления инструктажа по технике безопасности?
• К какой группе имущества и почему относится в аптеке санитарная спецодежда? Каков порядок документального учета ее выдачи персоналу и последующего списания?
6. В аптеках ЛПУ готовят настой шалфея листьев.
• Приведите латинские названия сырья, растения, семейства.
• Какие группы действующих веществ шалфея обуславливают его активность? Приведите формулы основных действующих веществ. Объясните выбор методики количественного определения действующих веществ в листьях шалфея в соответствии с физико-химическими свойствами веществ.
• В каких условиях должно храниться сырьё и почему? Как применяют в медицине листья шалфея (фармакологическая группа, препараты)?
Ответ
Сульфацил-натрий
Sulfacilum natrium

Сульфацетамид натрия
n-аминобензолсульфонилацетамид-натрий моногидрат
Относится к группе сульфаниламидных препаратов, это производное n-аминобензолсульфамида.
Фармакологическое действие сульфаниламидов обусловлено наличием в молекуле лекарственного вещества амида сульфаниловой кислоты. Сульфацил-натрий обладает, как и все сульфаниламиды, химиотерапевтической активностью при инфекциях, вызванных грамположительными и грамотрицательными бактериями.
Хорошая растворимость в воде позволяет использовать сульфацил-натрий для инъекций при пневмониях, гнойных трахеобронхитах, инфекциях мочеполовых путей. Назначают в глазной практике в виде 20-30% растворов и мазей.
Сульфацил-натрий – белый кристаллический порошок без запаха. Как и другие натриевые соли, легко растворим в в оде и метаноле, и практически нерастворим в органических растворителях (этаноле, эфире, хлороформе, ацетоне).
Сульфацил-натрий можно идентифицировать по характеру УФ-спектров.
2. Для идентификации используют общие и частные реакции, обусловленные физико-химическими свойствами, растворимостью и наличием функциональных групп в молекуле: первичной ароматической аминогруппы, ароматического цикла, сульфамидной группы, ацетильной группы.
Общие реакции:
Реакция образования азокрасителя (на первичную ароматическую аминогруппу) основана на образовании хлорида диазония при действии раствором нитрита натрия и разведенной хлороводородной кислотой. Последующее сочетание хлорида диазония с фенолами в щелочной среде приводит к образованию азокрасителя:

вишнево-красное окрашивание
или осадок оранжево-красного цвета
Лигниновая проба. Это своеобразная разновидность реакции образования шиффовых оснований. Она выполняется на древесине или газетной бумаге, при нанесении на которую сульфацила-натрия и капли разведенной соляной кислоты появляется оранжево-желтое окрашивание. Сущность происходящего химического процесса в том, что образуются ароматические альдегиды. Альдегиды взаимодействуют с первичными ароматическими аминами, образуя шиффовы основания:
 |
Реакция галогенирования (на ароматический цикл). Эта реакция основана на наличии донорной группы в ароматическом ядре молекулы сульфацила-натрия (заместитель первого рода):
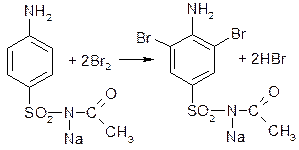
Реакция обнаружения серы (в сульфамидной группе). Наличие серы в молекуле сульфацила-натрия можно установить после окисления органической части молекулы концентрированной азотной кислотой или сплавления с 10-кратным количеством нитрата калия до сульфат-иона. Последний затем обнаруживают с помощью раствора хлорида бария:
SO42- + BaCl2 → BaSO4↓ + 2Cl-
белый
Гидролиз. При термическом разложении сульфацила-натрия в сухой пробирке образуется плав и ощущается запах уксусной кислоты.
Реакция с растворами солей тяжелых металлов. Ионы меди, замещая подвижный атом водорода сульфамидной группы, образуют с сульфацилом-натрия внутрикомплексное соединение голубовато-зеленоватого цвета, не изменяющегося при стоянии:
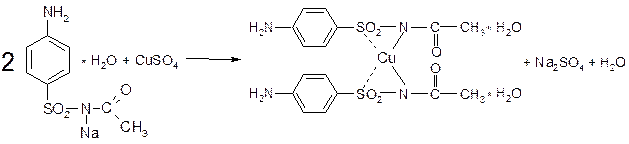
Реакция с нитропруссидом натрия. Раствор сульфацила-натрия в присутствии едкой щелочи образует окрашеный в красный цвет раствор.
Частная реакция на сульфацил-нария:
Сульфацил-натрий при действии уксусной кислотой выделяет белый осадок сульфацила, который после высушивания должен иметь температуру плавления около 183ºС:

При растворении осадка в этаноле и добавлении концентрированной серной кислоты образуется этилацетат, имеющий характерный запах:
 |
Катион натрия можно обнаружить по окраске бесцветного пламени в желтый цвет.
Количественное определение сульфацила-натрия можно провести с помощью физико-химических методов анализа.
Используют УФ- и ИК-спектроскопию, фотоколориметрию.
ИК-спектр сульфацила-натрия в таблетке калия бромида снимают в области от 400 до 4000 см-1.
УФ-спектр сульфацила-натрия имеет максимум светопоглощения при 256 нм. Содержание рассчитывают по раствору стандартного образца.
Фотоколориметрический метод основан на измерении оптической плотности окрашенных продуктов реакции (с нитропруссидом натрия, реакции образования азокрасителя).
Широко используют для количественного определения сульфацила-натрия нитритометрию. Титрант – 0,1 М раствор нитрита натрия. Определение ведут в кислой среде при температуре + 4ºС в присутствии бромида калия. Точку эквивалентности устанавливают по внутреннему индикатору – нейтральному красному, по внешнему индикатору – иодкрахмальной бумаге или потенциометрически.

Внешний индикатор при нитритометрическом титровании используют в тех случаях, когда образуется окрашенная соль диазония, маскирующая переход окраски внутреннего индикатора. Титрование с иодкрахмальной бумагой ведут до тех пор, пока капля титруемого раствора, взятая через 1 минуту после прибавления титранта, не вызовет тотчас же посинение бумаги:
2KI + 2NaNO2 + 4HCl → I2 + 2NO↑ + 2NaCl + 2KCl + 2H2O
Натриевые соли сульфаниламидных препаратов титруют кислотой в спирто-ацетоновой среде (индикатор – метиловый оранжевый):

Метод броматометрического определения основан на галогенировании сульфаниламидов. Титруют раствором бромата калия в кислой среде в присутствии калия бромида. Конец титрования устанавливают по обесцвечиванию индикатора метилового оранжевого выделяющимся бромом, или иодометрически:
KBrO3 + 5KBr + 6HCl → 3Br2 + 6KCl + 3H2O
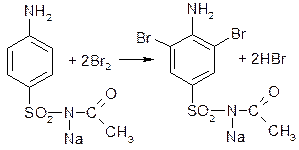
Br2 + 2KI → I2 + 2KBr
I2 + 2Na2S2O3 → 2NaI + Na2S4O6
3. Сульфацил-натрий при неправильном хранении постепенно теряет воду, что может привести к изменению его физических свойств. Под действием света, кислорода воздуха и воды в процессе хранения его происходит разложение. Чаще всего оно сопровождается реакцией гидролиза с образованием сульфаниловой кислоты и других веществ, которые затем окисляются. Поэтому некоторые сульфаниламиды темнеют, а их растворы желтеют.
 |
| <== предыдущая страница | | | следующая страница ==> |
| Задача 5 | | | Задача 7 |
Дата добавления: 2015-06-30; просмотров: 558; Нарушение авторских прав

Мы поможем в написании ваших работ!