
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
Образование сложных эфиров (этерификация)
Карбоксильная группа аминокислоты легко этерифицируется обычными методами. Например, метиловые эфиры получают, пропуская сухой газообразный хлористый водород через раствор аминокислоты в метаноле.

Если спирт не является жидкостью, реакцию можно проводить в инертном растворителе. Воду, которая при этом образуется, отгоняют. Одним из широко применяемых кислотных катализаторов является n-толуолсульфокислота (сильная органическая кислота). В качестве примера ниже показано получение бензилового эфира глицина.
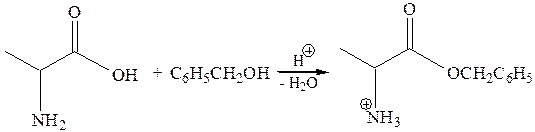
Реакции по аминогруппе:
Они аналогичны превращениям аминов, легко образуют с минеральными кислотами, легко ацилируются и алкилируются.
1. Ацилирование (образование амидов по аминогруппе). При нагревании с карбоновыми кислотами, их ангидридами и хлорангидридами аминокислоты ацилируются с образованием N-замещенных аминокислот:

Ангидриды и хлорангидриды, как сильные ацилирующие реагенты, вступают в реакцию с аминокислотами при комнатной температуре. Реакции с кабоновыми кислотами протекают в более жестких условиях (при нагревании).
2. Алкилирование. Подобно аминам, α-аминокислоты можно алкилировать алкилгалогенидами. В этой реакции образуются смеси с различной степенью алкилирования, а также триалкильные производные, которые обладают четвертичным атомом азота и называются бетаинами.

У животных и растений аминокислоты могут подвергаться полному метилированию с образованием бетаинов, которые обладают значительным запасом энергии и являются донорами метильных групп в метаболических процессах, не требующих дополнительного источника энергии. В настоящее время выделены бетаины глицина, триптофана, пролина, y-масляной кислоты.
3. Взаимодействие с альдегидами. Аминокислоты, подобно певичным аминам, реагируют с альдегидами с образованием оснований Шиффа (азометинов):

Эта реакция лежит в основе титрования аминокислот. Вследствие амфотерности аминокислоты не могут быть оттитрованы щелочью, но после обработки формальдегидом у них остается свободной только СООН-группа, которая может быть количественно оттитрована.
4. Дезаминирование (диазотирование): Реакция, при которой аминокислота теряет свою аминогруппу.
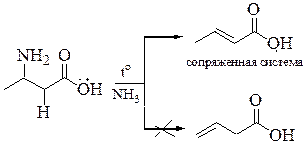
Удаление аминогруппы из молекулы амнокислоты может осуществляться под действием азотистой кислоты, воды, при нагревании, а также ферментативно.
Под действием азотистой кислоты через неустойчивые соли диазония образуются оксикарбоновые кислоты и выделяется молекулярный азот:
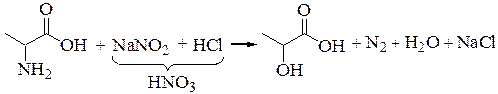
Возможно гидролитическое дезаминирование аминокислот:
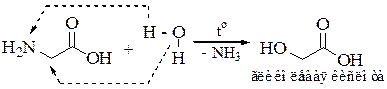
При нагревании некоторые аминокислоты могут отщеплять аммиак с образованием непредельных карбоновых кислот:

В живых организмах дезаминирование осуществляется под действием ферментов несколькими путями: восстановлением (а), окислением (б) и гидролизом.

Восстановительное дезаминирование. Реакция характерна для некоторых микроорганизмов. В качестве примера можно назвать превращение аспарагиновой кислоты в фумаровую кислоту и аммиак под действием фермента аспартазы.

Окислительное дезаминирование – наиболее распространенный (встречается в основном у бактерий и грибов) в природе процесс:

Для того чтобы полностью прошла реакция окислительного дезаминирования, например превращение аланина в пировиноградную кислоту, фермент, катализирующий эту реакцию, нуждается в окислительном (дегидрирующем) агенте. Обычным акцептором водорода в таких системах служит ФАД (флавинадениндинуклеотид), который переходит в восстановленную форму, сокращенно обозначаемую ФАД-Н2. Окислительное дезаминирование осуществляется через образование промежуточного имина. Ниже приведены два уравнения, описывающие дезаминирование аланина до пировиноградной кислоты: первое из них написано химиком-органиком, второе — биохимиком.
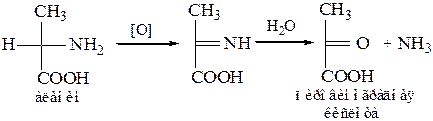

Реакции дезаминирования позволяют организму удалять избыток аминокислот, однако концентрация нежелательных азотистых веществ в системе при этом повышается. Высокие концентрации аммиака токсичны для организма, который стремится поэтому освободиться от аммиака или его производных. Организмы, обитающие в воде, выделяют аммиак непосредственно в окружающую среду. Поскольку наземные организмы лишены такой возможности, они выделяют лишний азот в виде твердых веществ — мочевины или мочевой кислоты.
5. Взаимодействие с кислотами. В результате получаем солянокислый глицин (соль).
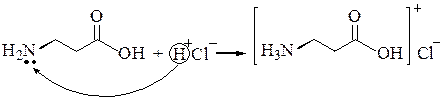
6. Переаминирование аминокислот с участием пиридоксальфосфата и аминотрансфераз, в результате чего аспарагиновая кислота превращается в щавелевоуксусную кислоту, а пиридоксальфосфат – в пиридоксаминофосфат. Последний участвует в аминировании α-кетокислот, например, при биосинтезе глутаминовой кислоты из D-глюкозы.
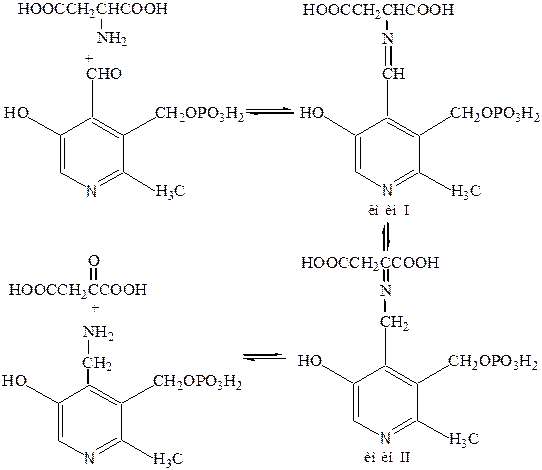
Реакции с одновременным участием карбоксильной и аминогруппы:
1. Межмолекулярная дегидратация (отношение к нагреванию). В зависимости от положения аминогруппы аминокислоты при нагревании ведут себя по-разному.
· α-аминокислоты образуют циклические амиды с устойчивым шестичленным циклом – дикетопиперазины (при этом аминогруппа одной молекулы аминокислоты взаимодействует с карбоксильной группой другой молекулы и наоборот), нециклические – пептиды, линейные амиды и полиамиды:
1,1-амидные группы

глицин дикетопиперазин
Дикетопиперазины способны гидролизоваться до исходных α-аминокислот.Дикетопиперазины можно рассматривать как замещенные амиды, содержащие две амидные группировки. Название дикетопиперазины связано с названием шестичленного гетероцикла пиразина.
· β-аминокислоты отщепляют аминогруппу и атом водорода у α-углеродного атома с образованием α,β-непредельной кислоты:

Причиной такой реакции является высокая подвижность атомов водорода, находящихся рядом с карбоксильной группой (влияние σ, π-сопряжения).
Способность β-аминокислот вступать в реакции элиминирования обусловлена тем, что за счет –I-эффекта двух электроноакцепторных групп у α-атома углерода возникает СН-кислотный центр и атом водорода становится способным отщепляться в виде протона.
В специальных условиях β-аминокислоты образуют β-лактамы:
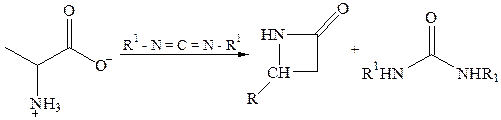
· y,δ-аминокислоты образуют внутренние (циклические) амиды – лактамы, которые самопроизвольно могут переходить в таутомерную y-лактимную форму:
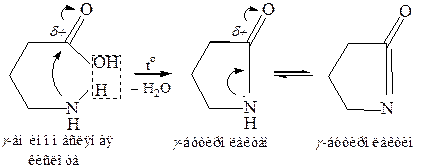
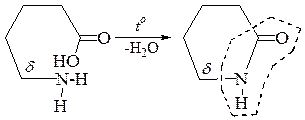
δ-валеролактам
Получение лактамов объясняется пространственным сближением амино- и карбоксильной групп (за счет свободного вращения вокруг С–С- и С–N-связей и образования клешневидной конформации), а также устойчивостью 5- и 6-членных циклов, образующихся в этих реакциях.
у-Аминокислоты, подобно y-гидроксикислотам, могут принимать клешневидную конформацию. В клешневидной конформации оказываются сближенными в пространстве карбоксильная группа и аминогруппа, поэтому взаимодействие между ними протекает внутримолекулярно. Лактамы способны гидролизоваться до исходной аминокислоты.
· ε-аминокислоты и аминокислоты, у которых амино- и карбоксильная группы разделены шестью и более атомами углерода, превращаются в полиамид и лишь частично в лактам. При образовании полиамида молекулы аминокислот вступают в реакцию поликонденсации по типу «голова-хвост»:

Для получения пептидов с определенной последовательностью аминокислот пользуются специальными методами «защиты» и «активации» функциональных групп.
Один из способов предотвращения полимеризации аминокислоты состоит в блокировании ее аминогруппы с тем, чтобы в реакцию могла вступать только аминогруппа амина. С этой целью используют карбобензоксихлорид (известный также под названием карбобензилоксихлорида или бензилхлор-формиат ), который реагирует с аминогруппами аминокислот и других соединений, давая карбамат:
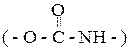
2. Взаимодействие с реактивом Сэнгера (2, 4-динитрофторбензол). Эта реакция идёт по механизму нуклеофильного ароматического замещения в слабощелочном растворе с образованием замещенного динитроанилина.

3. Нингидриновая реакцияприменяется для качественного и количественного анализа (обнаружения) в аминокислотных анализаторахдля спектрофотометрического определения α-аминокислот. Нингидрин разлагает α-аминокислоты на альдегиды, оксид углерода (IV) и аммиак. Аммиак конденсируется с избытком нингидрина и с продуктами его восстановления. Продукты конденсации окрашены в розово-фиолетовый цвет. Различные α-аминокислоты образуют окрашенные соединения, отличающиеся оттенком.

Продукт конденсации с нингидрином даёт краситель:

- Действие окислителей.

5. Ионнообменная хромотография – анализаторы аминокислот. Нерастворимые полимеры или смолы, содержащие свободные сульфогруппы, при обработке едким натром, становятся анионами, которыми заполняют колонку и пропускают через нее водный раствор смеси аминокислот. Различные цвиттер-ионы дают соли с основными группами смолы и связываются с ней.

Если вводить в колонку смесь аминокислот в виде раствора катионных солей, они будут еще прочнее связываться со смолой из-за отсутствия карбоксилат-анионов:
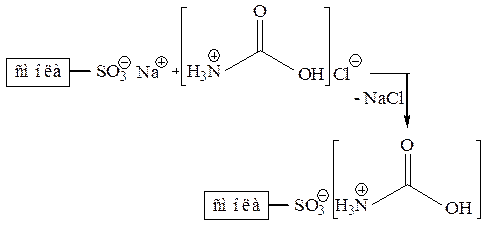
Чтобы разделить смесь аминокислот, колонку со смолой, содержащей катионы аминокислот H3NCHRCO2H, медленно промывают (элюируют) буферами, постепенно повышая их рH. При этом различные аминокислоты переходят в анионную форму и вымываются из колонки.
| <== предыдущая страница | | | следующая страница ==> |
| Комплексные соли с ионами меди | | | Качественные реакции аминокислот |
Дата добавления: 2015-07-26; просмотров: 290; Нарушение авторских прав

Мы поможем в написании ваших работ!