
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
ВОЛНОВЫЕ СВОЙСТВА ЭЛЕКТРОНОВ
СТРОЕНИЕ АТОМА
Уже в XIX веке было признано, что свет обладает волновыми свойствами, проявляющимися в дифракции от решетки. Однако, согласно данной впоследствии интерпретации фотоэлектрического эффекта, свету были приписаны также и корпускулярные свойства, так что излучение обладает двойственным корпускулярно-волновым характером. Следующие уравнения связывают количественно массу и частоту излучения n с его энергией Е, описывая этот дуализм:
E==hv==mc2
Здесь h—постоянная Планка, hv—энергия фотона с массой, эквивалентной т,а с—скорость света. Частота связана с длиной волны l уравнением
n=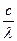
Из уравнений следует
l=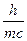 .
.
В 1924 г. де Бройль высказал предположение, что частицы, которые считались корпускулярными, также обладают волновыми свойствами. Уравнение де Бройля связывает длины волн таких частиц с их массой т и скоростью J:
l= 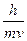
Подставляя в уравнение значения h, т и J, можно найти длины волн различных частиц, движущихся с определенными скоростями
Согласно этим вычислениям, для объектов с массой 1 г или больше, движущихся с обычными скоростями, длины волн настолько малы, что их
нельзя измерить. Однако из таблицы легко видеть, что электроны с соответствующими скоростями имеют длины волн, сравнимые с межатомными
расстояниями в молекулах и кристаллах.
Длины волн, вычисленные для различных частиц
| Частица | Масса m, г | Скорость, см/с | Длина волны, см |
| Медленный электрон | 9×10-28 | 7×10-2 | |
| Быстрый электрон | 9×10-28 | 5,9×108 | 1×10-8 |
| a-частица | 6,6×10-24 | 1,5×109 | 6×10-13 |
| Масса 1 г. | 6×10-27 | ||
| Теннисный мяч | 6×10-32 | ||
| Бейсбольный мяч | 2×10-32 |
Принцип неопределенности Гейзенберга утверждает, что нельзя одновременно определить точно импульс и положение электрона. Это утверждение можно проиллюстрировать следующим образом. При любом измерении положения электрона излучение, используемое для наблюдения электрона, должно претерпевать изменения. Измеряемая величина—это изменение, происходящее с фотоном при его контакте с электроном. Поэтому нельзя точно обнаружить объект, размеры которого меньше длины волны используемого излучения. Следовательно, чтобы обнаружить такую маленькую частицу, как электрон, необходимо использовать излучение с очень малой длиной волны l и соответственно с очень большой энергией E=hc/l. Однако, поскольку электрон чрезвычайно мал, столкновение с фотоном, обладающим большой энергией, должно изменять его импульс. В результате, чем точнее измеряется положение электрона (при использовании малых длин волн, т. е. фотонов с большой энергией), тем менее точно можно измерить одновременно его импульс (и обратно).
Модель атома Бора находится в противоречии с принципом неопределенности, так как она описывает одновременно и положение и импульс электрона. Вместо этого правильная теория может только предсказать вероятность нахождения электрона в определенном положении при данной энергии. После гипотезы де Бройля Шрёдингер интуитивно использовал волновое уравнение в качестве модели для описания поведения электрона в атоме. Эта модель учитывает требования, входящие в принцип неопределенности.
| <== предыдущая страница | | | следующая страница ==> |
| ЭКСТРАКЦИЯ | | | МАТЕМАТИЧЕСКОЕ ОПИСАНИЕ ВОЛНОВОГО ДВИЖЕНИЯ |
Дата добавления: 2014-03-11; просмотров: 501; Нарушение авторских прав

Мы поможем в написании ваших работ!