
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
В организме пировиноградная кислота восстанавливается в молочную. Напишите схему реакции
Метиловый спирт при попадании в организм вызывает тяжелое отравление, сопровождаемое потерей зрения. Полагают, что потеря зрения вызвана взаимодействием промежуточного продукта окисления метанола с белками сетчатки глаза. Напишите схему реакции окисления.
ТЕМА 9. Поли- и гетерофункциональные соединения,
участвующие в процессах жизнедеятельности
Подавляющее большинство органических веществ, участвующих в процессах метаболизма, представляют собой соединения с двумя и более функциональными группами. Такие соединения принято классифицировать следующим образом:
 1) полифункциональные, содержащие одинаковые функциональные группы, например: этиленгликоль СН2ОН – СН2ОН, гидрохинон НО– –ОН, щавелевая кислота НООС–СООН;
1) полифункциональные, содержащие одинаковые функциональные группы, например: этиленгликоль СН2ОН – СН2ОН, гидрохинон НО– –ОН, щавелевая кислота НООС–СООН;
 2) гетерофункциональные, содержащие различные функциональные группы, например: коламин СН2ОН–CH2NH2, п-аминобензойная кислота H2N– –СООН, пировиноградная кислота СН3–С(О) –СООН;
2) гетерофункциональные, содержащие различные функциональные группы, например: коламин СН2ОН–CH2NH2, п-аминобензойная кислота H2N– –СООН, пировиноградная кислота СН3–С(О) –СООН;
3) гетерополифункциональные, например: различные моносахариды, яблочная кислота
НООС–СН(ОН) –СН2-СООН.
Наличие нескольких функциональных групп в молекуле оказывает значительное влияние на химические свойства соединения, приводя, с одной стороны, к усилению или ослаблениию реакционной способности соединений, а с другой – к появлению нехарактерных для монофункциональных соединений специфических свойств. Последние являются наиболее важными для обеспечения биологических функций, выполняемых этими веществами в организме.
Кислотно-основные свойства. Выполняется общая закономерность: наличие в молекуле групп ОН, SH, СООН приводит к усилению ее кислотных свойств, а аминогрупп NH2, NH – к усилению основных свойств. Кроме того, наличие дополнительной электроноакцепторной группы вблизи кислотного центра влечет за собой повышение кислотности соединения. Так, этиленгликоль СН2ОН–СН2ОН проявляет более сильные кислотные свойства по сравнению с этанолом СН3–СН2ОН; щавелевая кислота НООС–СООН является более сильной кислотой, чем уксусная СН3–СООН, а молочная кислота СН3–СН(ОН) –СООН – более сильной, чем пропановая СН3–СН2–СООН.
Во всех перечисленных случаях отрицательный индуктивный эффект заместителей (-I-эффект) вблизи групп ОН и СООН обусловливает значительную поляризацию связи О–Н и легкость отщепления протона, т. е. усиление кислотных свойств. Аналогично, замена метильной группы СН3 в ацетамиде на аминогруппу в карбамиде (мочевине):
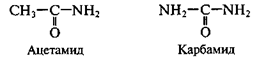
приводит к усилению основных свойств, что можно проиллюстрировать реакцией с соляной кислотой (образуется соль – гидрохлорид мочевины):

Еще более сильные по сравнению с карбамидом основные свойства проявляет гуанидин:
 NH
NH
NH2–C–NH2
Наконец, наличие в молекуле различных по кислотно-основным свойствам функциональных групп обусловливает амфотерные свойства соединений. Предельным случаем является полный перенос протона от кислотного центра к основному, например в a-аминокислотах, которые в кристаллическом состоянии, а так же в нейтральном водном растворе существуют в форме цвиттер-иона (биполярного иона, внутренней соли): H3N+–CH(R) –COO–.
Нуклеофильно-электрофильные свойства. Выполняется общая закономерность, а именно: наличие электроноакцепторного заместителя (-I-эффект) облегчает протекание нуклеофильных реакций и затрудняет протекание электрофильных реакций. Так, в присутствии карбоксильной группы атом галогена, например в a- галогенкарбоновых кислотах, легко замещается не только на гидроксильную группу (при взаимодействии со щелочами), но и на аминогруппу (при взаимодействии с аммиаком):
 R-CH-COOH + 3NH3 ® R-CH-COONH4 + NH4C1
R-CH-COOH + 3NH3 ® R-CH-COONH4 + NH4C1
Cl NH2
Приведенная реакция протекает по механизму SN, давая соли a-аминокислот.
В a,b-ненасыщенных карбоновых кислотах близость электроноакцептора (карбоксильной группы) приводит к протеканию реакций присоединения по двойной С-С связи по нуклеофильному (AN) механизму; реакции же электрофильного присоединения затруднены.
Реакции циклизации. Относятся к специфическим реакциям гетерофункциональных соединений и могут протекать как внутримолекулярно, так и межмолекулярно в зависимости от удаленности функциональных групп друг от друга.
Внутримолекулярная циклизация. Выполняется общая закономерность: реакции характерны для гетерофункциональных соединений с g- и d-положением функциональных групп. Нуклеофильный и электрофильный реакционные центры находятся внутри одной молекулы и оказываются сближенными в пространстве за счет существования молекулы в «свернутой» (клешневидной) конформации.
В результате реакций внутримолекулярной циклизации могут образоваться циклические полуацетали из альдегидоспиртов по механизму AN:
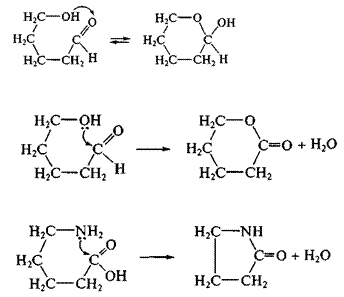 |
циклические эфиры – лактоны – из гидроксикислот по механизму SN с участием sр2-гибридизованного атома углерода
циклические амиды – лактамы – из аминокислот по механизму SN с участием sр2-гибридизованного атома углерода:
Реакции идут самопроизвольно уже при незначительном наггревании. Образующиеся циклические продукты подвергаются гидролизу в кислой и щелочной среде с образованием соответствующих солей.
Межмолекулярная циклизация. Выполняется общая закономерность: реакции характерны для замещенных кислот, проходят по механизму межмолекулярного элиминирования и сопровождаются образованием устойчивых шестичленных циклов – циклических диэфиров – лактидов из a-гидроксикислот; например, образование лактида молочной кислоты или циклических диамидов – дикетопиперазидов из a-аминокислот:

Реакции комплексообразования. Выполняется общая закономерность: поли- и гетерофункциональные соединения с a-положением функциональной группы выступают в роли бидентатных или полидентатных лигандов при взаимодействии с ионами переходных металлов с образованием внутрикомплексных соединений – хелатов.
Реакции хелатообразования являются специфическим свойством поли- и гетерофункциональных соединений; чрезвычайно широко распространены и играют существенную роль в процессах метаболизма. Один из примеров – образование внутрикомплексной соли – глицината меди – при взаимодействии в растворе амино-уксусной кислоты с солями меди(П):

Хелаты представляют собой устойчивые циклические комплексные соединения. Большинство ионов биометаллов в организме находятся в виде хелатных комплексов с органическими биолигандами. Одним из примеров таких соединений является гемовая структура (гем), представленная на рисунке.
Многоатомные спирты.
В соответствии с числом гидроксильных групп, входящих в их состав, различают одноатомные, двухатомные и т. д. спирты. Двухатомные спирты, т. е. спирты, содержащие две гидроксильные группы, носят общее название диолы, или гликоли. Трехатомные спирты называют триолами, или глицеринами; спирты с большим числом гидроксильных групп носят общее название полиолы.
Простейшие и наиболее важные представители диолов и триолов – этиленгликоль и глицерин соответственно.
Многоатомные спирты обладают большей кислотностью по сравнению с одноатомными, что является следствием - I- эффекта одной гидроксильной группы по отношению к другой. Многоатомные спирты по свойствам в значительной степени напоминают одноатомные. Гидроксильные группы в них могут первичными, вторичными и третичными, причем в реакции может вступать одна или несколько гидроксильных групп. Многоатомные спирты с гидроксидами некоторых тяжелых металлов в щелочной среде образуют внутрикомплексные (хелатные) соединения, имеющие характерное окрашивание. В частности, при взаимодействии с гидроксидом меди(II) возникает интенсивное синее окрашивание.
Дегидратация этиленгликоля в специальных условиях приводит к макроциклическим полиэфирам, так называемым к р а у н - э ф и р а м. Краун-эфиры весьма перспективные комплексообразователи, своеобразные ловушки катионов. В определенной степени они моделируют действие некоторых веществ (например, антибиотика пептидной природы валиномицина), облегчающих транспорт ионов через клеточные мембраны. Примером может служить полиэфир 18-краун-6, образующий прочный комплекс с ионом калия.
Примерами многоатомных спиртов высшей атомности служат пентиты и гекситы – соответственно пяти- и шестиатомные спирты с открытой цепью. Накопление гидроксильных групп в молекуле ведет к появлению сладкого вкуса.
 Представители пентитов и гекситов – ксилит и сорбит – заменители сахара для больных диабетом. Инозиты – шестиатомные спирты циклогексанового ряда. В связи с наличием асимметрических атомов углерода у инозита существует несколько стереоизомеров.
Представители пентитов и гекситов – ксилит и сорбит – заменители сахара для больных диабетом. Инозиты – шестиатомные спирты циклогексанового ряда. В связи с наличием асимметрических атомов углерода у инозита существует несколько стереоизомеров.
Справа приведена кресловидная информация мезоинозита (в которой пять из шести гидроксильных групп находятся в экваториальном положении).
Мезоинозит относится к витаминоподобным соединениям (витамины группы В) и является структурным компонентом сложных липидов. В растениях широко распространена фитиновая кислота, представляющая собой гексафосфат мезоинозита. Ее кальциевая или смешанная кальций магниевая соль, называемая фитином, стимулирует кроветворение, улучшает нервную деятельность при заболеваниях, связанных с недостатком фосфора в организме.
Двухатомные фенолы
Двухатомные фенолы – пирокатехин, резорцин, гидрохинон – входят в состав многих природных соединений. Все они дают характерное окрашивание с хлоридом железа. Пирокатехин (о-дигидроксибензол, катехол) является структурным элементом многих биологически активных веществ в частности катехоламинов. Его монометиловый эфир гваякол, применяется как лекарственное средство при катаре верхних дыхательных путей.
Резорцин (м-дигидроксибензол) используется при лечении кожных заболеваний в составе примочек или мазей.
Гидрохинон (п-дигидроксибензол) применяется как проявитель в фотографии. В организме восстановительная способность замещенного гидрохинонового фрагмента делает его участником важного процесса транспорта электронов от окисляемого субстрата к кислороду. Сама гидрохиноновая группировка окисляется при этом в хиноидную.
Простейшим диамином является этилендиамин. Он образуется при аммонолизе 1,2-дихлорэтана или этиленимина.
Тетраметилендиамин (путресцин) и пентаметилендиамин (кадаверин) длительное время считали трупными ядами, т. е. соединениями, образующимися при декарбоксилировании диаминокислот и обусловливающими ядовитость гниющих белков.
H2NCH2CH2CH2CH2NH2 Н2NСН2СН2СН2СН2СН2МН2
Путресцин Кадаверин
В настоящее время выяснено, что ядовитые свойства белкам при гниении придают другие вещества.
Дикарбоновые и ненасыщенные карбоновые кислоты.
Карбоновые кислоты, содержащие в своем составе одну карбоксильную группу, называют одноосновными, две — двухосновными т. д.
Дикарбоновые кислоты – белые кристаллические вещества, обладающие более кислым характером, чем монокарбоновые ты. Дикарбоновые кислоты образуют два ряда функциональных производных – по одной и двум карбоксильным группам; получить их можно общими для карбоновых кислот методами.
Щавелевая кислота НООС–СООН – простейшая двухосновная кислота. Ее соли называют оксалатами. Некоторые из них трудно растворимы и часто образуют камни в почках и мочевом пузыре (оксалатные камни). К таким солям относится оксалат кальция. При нагревании с серной кислотой щавелевая кислота разлагается с образованием СО.
Малоновая кислота НООС–СН2–СООН и ее производные по метиленовой группе легко декарбоксилируются при нагревании выше 100 °С. Эта реакция лежит в основе общего способа получения замещенных производных уксусной кислоты
Янтарная кислота в заметном количестве находится в янтаре – отсюда она и получила свое название. Некоторые ее производные, например имид (сукцинимид) и соли (сукцинаты), называют с учетом латинского названия янтаря.
Окисление (дегидрирование) янтарной кислоты в фумаровую, катализируемое ферментом сукцинатдегидрогеназой, осуществляется с участием кофермента ФАД. Реакция протекает стереоспецифично с отщеплением атомов водорода и образованием фумаровой кислоты.
Аминоспиртами называют соединения, содержащие в молекуле одновременно амино- и гидроксигруппы.
У одного атома углерода эти группы удерживаются непрочно (происходит отщепление аммиака с образованием карбонильного соединения или воды с образованием имина). Поэтому простейшим представителем аминоспиртов является 2-аминоэтанол, соединение, в котором две функциональные группы расположены у соседних атомов углерода.
Аминоспирты
2-Аминоэтанол (этаноламин, коламин) – структурный компонент сложных липидов, образуется путем размыкания напряженных трехчленных циклов этиленоксида и этиленимина аммиаком или водой соответственно (реакции нуклеофильного замещения).
Холин (триметил-2-гидроксиэтиламмоний) — структурный элемент сложных липидов. Имеет большое значение как витаминоподобное вещество, регулирующее жировой обмен.
В организме холин может образоваться из аминокислоты серина. При этом сначала в результате декарбоксилирования серина получается 2-аминоэтанол (коламин), который затем подвергается исчерпывающему метилированию при участии S-аденозилметионина (SAM).
В результате окисления свободного холина in vivo образуется биполярный ион бетаин, который может служить источником метильных групп в реакциях трансметилирования.
Биологическая роль сложных эфиров холина. Замещенные фосфаты холина являются структурной основой фосфолипидов — важнейшего строительного материала клеточных мембран.
Сложный эфир холина и уксусной кислоты — ацетилхолин — наиболее распространенный посредник при передаче нервного возбуждения в нервных тканях (нейромедиатор). Он образуется в организме при ацетилировании холина с помощью ацетил кофермента А.
При ингибировании ацетилхолинэстеразы ацетилхолин накапливается в организме, что приводит к непрерывной передаче нервных импульсов и соответственно непрерывному сокращению мышечной ткани. На этом основано действие инсектицидов (химических средств уничтожения насекомых) и нервно паралитических ядов — зарина, табуна — фосфорорганических соединений, которые, реагируя с остатком серина, содержащимся в активном центре ацетилхолинэстеразы, ингибируют действие этого фермента.
В медицинской практике используется ряд производных холина.
Ацетилхолин хлорид применяется в качестве сосудорасширяющего средства. Карбамоилхолинхлорид (карбахолин) — холинуретан, сложный эфир холина и карбаминовой кислоты, не гидролизуется холинэстеразой и поэтому активнее холина и обладает более продолжительным действием. Сукцинил-холиниодйд (дитилин) — сложный эфир холина и янтарной кислоты, оказывает мышечно-расслабляющий эффект.
Важную роль в организме играют аминоспирты, содержащие в качестве структурного фрагмента остаток пирокатехина. Они носят общее название катехоламинов.
Катехоламины — представители биогенных аминов, образующихся в организме в результате процессов метаболизма. К катехоламинам относятся дофамин, норадреналин и адреналин, выполняющие, как и ацетилхолин, роль нейромедиаторов. Адреналин является гормоном мозгового вещества надпочечников. Адреналин участвует в регуляции сердечной деятельности. При физиологических стрессах он выделяется в кровь («гормон страха»). Активность адреналина связана с конфигурацией хирального центра, определяющей взаимодействие с рецептором.
Подобно 1,2-дигидроксибензолу, катехоламины с раствором хлорида железа (III) дают изумрудно-зеленое окрашивание, переходящее в вишнево-красное при добавлении раствора амиака, что может служить качественной реакцией на эти соединения.
Структурно близки катехоламинам некоторые природные и синтетические биологически активные вещества, применяемые в производстве лекарственных средств. Примерами служат алкалоид иофедрин, оказывающий сосудорасширяющее действие, и синтетический препарат мезатон, повышающий, подобно норадреналину, артериальное давление. Оба вещества применяются в виде гидрохлоридов.
Гидрокси- и аминокислоты.
Гидроксикислоты содержат в молекуле одновременно гидроксильную и карбоксильную группы, аминокислоты — карбоксильную и аминогруппу.
В зависимости от расположения гидрокси- или аминогруппы по отношению к карбоксилу различают a-, b-, g- и т. д. гидроксикислоты или аминокислоты.
a-Гидрокси и а-аминокислоты. При нагревании эти соединения претерпевают межмолекулярную дегидратацию с образованием шестичленных кислород- и азотсодержащих гетероциклов — лактидов и дикетопиперазинов соответственно.
a-Гидроксикислоты способны разлагаться при нагревании в присутствии минеральных кислот с образованием карбонильных соединений и муравьиной кислоты.
Гликолевая кислота НОСН2СООН — простейший представитель гидроксикислот. Встречается во многих растениях, например свекле и винограде.
Молочная кислота СН3СН(ОН)СООН — одна из важнейших гидроксикислот. Широко распространена в природе как продукт молочнокислого брожения лактозы, содержащейся в молоке, и других углеводов, входящих в состав овощей и плодов. Кислое молоко, кефир, кислая капуста, моченые яблоки и т. д. содержат в значительном количестве молочную кислоту, образующуюся в результате жизнедеятельности молочнокислых бактерий. Соли называют лактаты.
Молочная кислота содержит асимметрический атом углерода, поэтому может существовать в виде двух энантиомерных форм. В организме L-(+)-молочная кислота, называемая также мясомолочной кислотой, является одним из продуктов превращения глюкозы (гликолиза). Она накапливается в мышцах при интенсивной работе, вследствие чего в них возникает характерная боль. Причина накопления молочной кислоты – недостаток кислорода, что вызывает восстановление пировиноградной кислоты в молочную с участием кофермента НАДН.
Оксокислоты
Оксокислоты — соединения, содержащие одновременно карбоксильную и альдегидную (или кетонную) группы. В соответствии с этим различают альдегидокислоты и кетокислоты.
Простейшей альдегидокислотой является глиоксиловая кислота НООС—СНО.
Она содержится в недозрелых фруктах, но по мере созревания ее количество уменьшается. Глиоксиловая кислота обычно существует в виде гидрата НООС—СН(ОН)2. Электроноакцепторная карбоксильная группа в глиоксиловой кислоте, подобно трихлорметильной группе хлораля, создает значительный дефицит электронной плотности и соседнем атоме углерода, в результате чего две гидроксильные группы при нем удерживаются достаточно прочно. Важную роль в биохимических процессах играют следующие кетонокислоты.
Пировиноградная, щавелевоуксусная и a-оксоглутаровая кислоты участвуют в цикле трикарбоновых кислот. Ацетоуксусная кислота относится к b-кетонокислотам. При переаминировании a-кетонокислоты образуют соответствующие a-аминокислоты.
Пировиноградная кислота СН3С(О)СООН (т. пл. 14 °С, т. кип. 165 °С) — одно из центральных соединений в цикле трикарбоновых кислот. Она является также одним из промежуточных продуктов при молочнокислом и спиртовом брожении углеводов. Может быть получена при взаимодействии ацетилхлорида с цианидом калия с последующим гидролизом образующегося кетононитрила или путем окисления молочной кислоты.
Своим названием пировиноградная кислота обязана тому, что впервые была выделена при пиролизе виноградной кислоты. Ее соли называют пируватами. Пировиноградная кислота легко декарбоксилируется при нагревании с разбавленной и декарбонилируется — с концентрированной серной кислотой. При окислении пировиноградная кислота превращается в уксусную кислоту и оксид углерода (IV).
Декарбоксилирование пировиноградной кислоты in vivo протекает в присутствии фермента декарбоксилазы и соответствующего кофермента. Получающийся при этом ацетальдегид, не теряя связи с коферментом («активный ацетальдегид»), может присоединяться к a- кетонокислотам, образуя a-ацето-a-гидроксикислоты. Пировиноградная кислота сильнее уксусной и способна к енолизации. Важное её производное – фосфоенолпировиноградная кислота (фосфат енольной формы пировиноградной кислоты). В организме анион этой кислоты – фосфоенолпируват – образуется в процессе гликолиза и служит предшественником пирувата.
Ацетоуксусная кислота СН3С(О)СН2СООН — пример b-кетонокислоты. В свободном состоянии представляет сиропообразную жидкость, уже при комнатной температуре медленно выделяющую диоксид углерода. Получающийся при этом ацетон образуется первоначально в енольной форме. Подобное декарбоксилирование – общее свойство b-кетонокислот.
Ацетоуксусная кислота образуется in vivo в процессе метаболизма высших жирных кислот и как продукт окисления b-гидроксимасляной кислоты наряду с продуктами ее превращений накапливается в организме у больных сахарным диабетом (так называемые «ацетоновые» или «кетоновые» тела).
Большое теоретическое значение в связи с вопросами таутомерии и двойственной реакционной способности имеет этиловый эфир ацетоуксусной кислоты СН3С(О)СН2СООС2Н5, так называемый ацетоуксусный эфир.
Ацетоуксусный эфир — бесцветная жидкость (т. кип. 181 °С) с приятным фруктовым запахом. Впервые синтезирован более 100 лет назад, его строение долгое время было предметом острых дискуссий. Основная трудность заключалась в том, что в результате его химических превращений получались два ряда производных – ацетоуксусной и b- гидроксикротоновой кислот, т.е. ацетоуксусный эфир оказался веществом, проявляющим двойственную реакционную способность.
 В соответствии со строением ацетоуксусного эфира (вещества, имеющего кетонную группу) протекают реакции присоединения циановодородной кислоты и восстановления. Однако под действием натрия, гидроксида натрия или при ацилировании в определенных условиях образуются производные b-гидроксикротоновой кислоты, т. е. соединения с енольной группой. Исследования показали, что ацетоуксусный эфир представляет смесь двух изомеров – кетона (95 %) и енола (5 %), находящихся в таутомерном равновесии. Это еще один пример кето-енольной таутомерии.
В соответствии со строением ацетоуксусного эфира (вещества, имеющего кетонную группу) протекают реакции присоединения циановодородной кислоты и восстановления. Однако под действием натрия, гидроксида натрия или при ацилировании в определенных условиях образуются производные b-гидроксикротоновой кислоты, т. е. соединения с енольной группой. Исследования показали, что ацетоуксусный эфир представляет смесь двух изомеров – кетона (95 %) и енола (5 %), находящихся в таутомерном равновесии. Это еще один пример кето-енольной таутомерии.
При действии на ацетоуксусный эфир какого-либо реагента в реакцию вступает один из таутомеров. Поскольку второй таутомер за счет равновесия восполняет убыль реагирующего таутомера, то таутомерная смесь реагирует в данном направлении
Скорость установления таутомерного равновесия может быть оценена на основании изучения взаимодействия ацетоуксусного эфира с бромом в присутствии хлорида железа(III). Ацетоуксусный эфир как енол образует с хлоридом железа характерное фиолетовое окрашивание. Если к этому окрашенному раствору прибавлять по каплям бром то енольный таутомер, присоединяя бром по двойной связи, переходит в бромпроизводное и окраска исчезает. Однако чернз некоторое время окраска вновь появляется, так как нарушенное равновесие восстанавливается и кетонный мономер частично переходит в енольную форму. Опыт можно вторить несколько раз, пока все взятое количество ацетоуксусного эфира не прореагирует с бромом.
Ацетоуксусный эфир широко применяется в органическом синтезе как исходное вещество для получения кетонов, карбоновых кислот, гетерофункциональных соединений, в том числе производных гетероциклов, представляющих интерес в качестве лекарственных средств.
Гетерофункциональные производные бензола как лекарственные средства.
Последние десятилетия характеризуются появлением множества новых лекарственных средств и препаратов. Вместе с тем большое значение продолжают сохранять некоторые группы известных ранее лекарственных средств, в частности таких, структурную основу которых составляет бензольное ядро.
Сам бензол может быть причиной острых и хронических отравлений. Он оказывает раздражающее действие на кожу, пары его в большой концентрации вызывают возбуждение, расстройство дыхания. Монофункциональные производные бензола в большинстве случаев также обладают выраженными токсическими свойствами. Фенол, анилин, галогенопроизводные ароматического ряда служат исходными или промежуточными продуктами крупнотоннажной химической промышленности. В связи с этим необходимо учитывать их токсическое действие.
Среди монофункциональных производных бензола особое место занимает производное с карбоксильной группой — бензойная кислота, применяемая в медицине в виде натриевой соли (натрия бензоат) как отхаркивающее средство.
Бензойная кислота в свободном виде встречается в некоторых смолах и бальзамах, а также клюкве, бруснике, но чаще содержится в связанном виде, например, в виде N-бензоильного производного аминоуксусной кислоты C6H5CONHCH2COOH, называемого гиппуровой кислотой. Гиппуровая кислота образуется в печени из бензойной и аминоуксусной кислот и выводится с мочой. В клинической практике по количеству гиппуровой кислоты в моче больных (после приема бензоата натрия) судят об эффективности обезвреживающей функции печени.
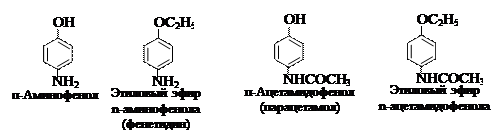
Как гетерофункциональное соединение п- аминофенол образует производные по каждой функциональной группе в отдельности и одновременно по двум функциональным группам. п-Аминофенол ядовит. Интерес для медицины представляют его производные – парацетамол, фенацетин, оказывающие анальгетическое (обезболивающее) и жаропонижающее действие.
Парацетамол является N-ацетильным производным п-аминофенола. Фенацетин получается при ацетилировании этилового эфира п-аминофенола, называемого фенетидином.
 |
п-Аминобензойная кислота (ПАБК) и ее производные.
Эфиры ароматических аминокислот обладают общим свойством – способностью в той или иной степени вызывать местную анестезию, т.е. потерю чувствительности. Особенно заметно это свойство выражено у пара- производных. В медицине используют анестезин (этиловый эфир ПАБК) и новокаин (b-диэтиламиноэтиловый эфир ПАБК). Новокаин применяют в виде соли (гидрохлорида), что связано с необходимостью повышения его растворимости в воде.
 |
Анестезин и новокаин несколько уступают по силе анестезирующего действия кокаину, широко употреблявшемуся ранее в медицинской практике. Однако замена кокаина на новокаин имела важное значение в связи с выведением из практики вещества, при хроническом применении которого развивается лекарственная зависимость (кокаинизм). Новокаин в основе своей структуры имеет те же фрагменты, что и кокаин.
п-Аминобензойная кислота является фактором роста микроорганизмов и участвует в синтезе фолиевой кислоты, при недостатке или отсутствии которой микроорганизмы погибают. Название кислоты связано с выделением ее из листьев шпината (от лат. folium – лист). Фолиевая кислота играет важную роль в метаболизме нуклеиновых кислот и белков; в организме человека не синтезируется.
Фолиевая кислота (витамин В) включает три структурных фрагмента — ядро птеридина, п-аминобензойную и L-глутаминовую кислоты. Обе функциональные группы п- аминобензойной кислоты участвуют в образовании связей с двумя другими компонентами.
Сульфаниловая кислота (п-аминобензолсульфокислота) легко получается при сульфировании анилина, существует в виде диполярного иона. Амид сульфаниловой кислоты (сульфаниламид), известный под названием стрептоцид, является родоначальником группы лекарственных средств, обладающих антибактериальной активностью и называемых сульфаниламидами (сульфамидами).
Антибактериальное действие сульфаниламидов основано на том, что они являются антиметаболитами по отношению к п-аминобензойной кислоте, участвующей в биосинтезе фолиевой кислоты в микроорганизмах. Амид сульфаниловой кислоты имеет структурное сходство с п-аминобензойной кислотой. При наличии в бактериальной среде сульфаниламидов, они конкурируют с аминобензойной кислотой на стадии образования птероевой кислоты и связываются с птеридиновым фрагментом. Наличие сульфамидной группы препятствует дальнейшему взаимодействию с глутаминовой кислотой, и биосинтез фолиевой кислоты прекращается, что ведет к гибели бактерий. Избирательность бактериального действия сульфаниламидов основана на том, что фолиевая кислота в человеческом организме не синтезируется. Таким образом, сульфаниламиды блокируют метаболические реакции, существенные для определенных бактерий (пневмококки, стрептококки и др.), и в то же время не влияют на организм человека.
Салициловая кислота относится к группе гидроксибензойных кислот. Как о-гидроксибензойная кислота она легко декарбоксилируется при нагревании с образованием фенола.
Салициловая кислота растворима в воде, дает интенсивное окрашивание с хлоридом железа(III) (качественное обнаружение фенольной гидроксильной группы). Она оказывает антиспазматическое, жаропонижающее и антигрибковое действие, но как сильная кислота (рКа 2,98) вызывает раздражение пищеварительного тракта и поэтому применяется только наружно. Внутрь применяют ее производные – соли или эфиры. Салициловая кислота способна образовывать производные по любой функциональной группе. Практическое значение имеют салицилат натрия, сложные эфиры по СООН-группе (метилсалицилат, фенилсалицилат (салол)) и ОН-группе – ацетилсалициловая кислота (аспирин). Перечисленные производные (кроме салола) оказывают анальгетическое, жаропонижающее и противовоспалительное действие. Метилсалицилат из-за раздражающего действия используется наружно в составе мазей. Салол применяется как дезинфицирующее средство при кишечных заболеваниях и примечателен тем, что в кислой среде желудка не гидролизуется, а распадается только в кишечнике, поэтому используется также в качестве материала для защитных оболочек некоторых лекарственных средств, которые не стабильны в кислой среде желудка.
Салициловая кислота впервые была получена путем окисления салицилового альдегида, содержащегося в растении таволге (род Spireae). Отсюда и ее первоначальное название — спировая кислота, с которым связано название аспирин (начальная буква «а» обозначает ацетил). Ацетилсалициловая кислота в природе не найдена.
Из других производных салициловой кислоты большое значение имеет п- аминосалициловая кислота (ПАСК) как противотуберкулезное средство. ПАСК является антагонистом п-аминобензойной кислоты, необходимой для нормальной жизнедеятельности микроорганизмов. Другие изомеры таким действием не обладают. м-Аминосалициловая кислота является высокотоксичным веществом.
Контрольные задания
1. a-Гидроксикислоты получают при действии водным раствором щелочи на a- галогенокарбоновые кислоты. Синтезируйте молочную (2-гидроксипропановую) кислоту из соответствующей галогенкарбоновой кислоты. Каков механизм реакции? Является ли молочная кислота оптически активным соединением? Если да, изобразите оба энантиомера.
2. В метаболизме некоторых a-аминокислот участвует гомосерин (2-амино-4- гидроксибутановая кислота) и его лактон. Напишите уравнение образования лактона гомосерина.
3. Яблочная кислота НООС-СНОН-СН2СООН при нагревании отщепляет воду. Напишите схему реакции дегидратации яблочной кислоты и объясните механизм. Чем объясняется легкость дегидратации яблочной кислоты?
4. Какое вещество можно распознать при помощи свежеосажденного гидроксида меди (II): а) глицерин; б) 1,3- бутадиен; в) этиловый спирт; г) бромбутан? К какому классу органических соединений относится выбранное Вами вещество? Обладает ли оно кислотными свойствами?
5. Наличие какой функциональной группы (групп) в молекуле салициловой кислоты подтверждает реакция декарбоксилирования:
а) карбоксильной; б) фенольного фрагмента; в) карбонильной; г) метильной; д) альдегидной.
6. Образование цикла при нагревании 4-гидроксипентановой кислоты это реакция:
а) дегидрирование; б) дегидратация; в) гидролиз; г) гидрирование; д) гидратация.
Приведите формулу соединения, образующегося при нагревании 4-гидроксипентановой кислоты.
ТЕМА 10. Биологически важные гетероциклические соединения
Гетероциклические соединения (гетероциклы) – соединения, включающие в цикл один или несколько атомов, отличных от углерода (гетероатомов). Гетероциклические системы лежат в основе структуры соединений различных классов биологически активных веществ, таких как ДНК, РНК, многих лекарственных препаратов, а также алкалоидов. Последние представляют собой азотсодержащие гетероциклы растительного происхождения, обладающие выраженным физиологическим действием. К ним относятся различные наркотические средства, никотин, кофеин, морфин, атропин и др.
Наибольшее значение для организма имеют ароматические азотсодержащие гетероциклы — сопряженные системы, содержащие атом (атомы) азота и удовлетворяющие критерию ароматичности. Ароматические гетероциклы можно подразделить на две группы.
1. p-Избыточные системы — молекулы с повышенной электронной плотностью внутри цикла. Это происходит, когда пара р-электронов атома азота вступает в сопряжение с p-электронами атомов углерода (р, p-сопряжение). В этом случае гетероатом является электронодонором, а повышение электронной плотности внутри цикла облегчает протекание реакций по механизму SЕ (в a-положение к гетероатому); соединения легко окисляются. Простейшим примером p-избыточной гетероциклической системы является пиррол:

Электронодонорный атом азота, называемый пиррольным, является NH-кислотным центром. Кислотные свойства выражены очень слабо; например, пиррол взаимодействует со щелочными металлами и их амидами. Восстанавливается пиррол с трудом в жестких условиях, образуя гетероцикл пирролидин, обладающим сильноосновными свойствами. Пиррольное ядро входит в состав порфина, порфирина (тетрапиррольные соединения), природной аминокислоты триптофана, в состав индола (бензопиррола):

2. p-Дефицитные системы — гетероциклы с пониженной электронной плотностью внутри цикла. В этом случае в сопряжении с p-электронами атомов углерода участвует только один p-элекгрон атома азота, а электронодефицитное состояние обусловлено большей по сравнению с атомом углерода электроотрицательностью атома азота. В этом случае гетероатом является акцептором протона за счет пары электронов, не участвующей в сопряжении, и проявляет основные свойства (пиридиновый атом азота). Электронодефицитное состояние ароматической системы приводит к затруднению реакции SЕ (в b-положении к гетероатому). Простейшим примером такой гетероциклической системы является пиридин:
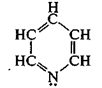 |
Соединения, содержащие пиридиновый цикл, с трудом окисляются, но легче восстанавливаются (гидрируются). Например, в хинолине (бензопиридине), представляющем конденсированную ароматическую систему, окислению легче подвергается бензольное кольцо, а восстановлению — пиридиновое.
 | |||
 | |||
Однако гомологи пиридина легко окисляются даже в мягких условиях. Так, при окислении b-пиколина (2-метилпиридина) образуется никотиновая кислота (витамин РР):

Ядро пиридина и пиперидина входит в состав витаминов (РР, группы В), анестетиков и т.д.
Кроме того, пиридиновый атом азота проявляет нуклеофильные свойства, реагируя с галогеналканами, образуя алкилпиридиниевые ионы, которые в свою очередь с такими сильными нуклеофилами, как гидрид-ион, дают четвертичные алкилпиридиниевые соли. Реакция лежит в основе действия кофермента НАД+, содержащего замещенный катион пиридиния:
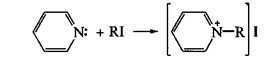 | |||
 | |||
Наконец, сочетание в одной молекуле пиррольного и пиридинового атомов азота обусловливает амфотерные свойства, которые выражены слабо вследствие «слабости» NH-кислотного и N-основного центров. Таким образом, не происходит полного переноса протона, как в случае аминокислот, однако возможно образование межмолекулярных водородных связей, как в случае имидазола:

а также взаимодействие соединений с кислотами и щелочами (в отличие от пиррола). Ядро имидазола входит, в частности, в состав аминокислоты гистидина и продукта ее декарбоксилирования – биогенного амина гистамина.
Сочетание в молекуле двух пиридиновых атомов азота приводит к увеличению дефицита электронов внутри цикла и еще большему по сравнению пиридином понижению активности (инертности) соединений в реакциях SЕ а также уменьшению их основности по сравнению с пиридином. Так, шестичленный гетероцикл с двумя пиридиновыми атомами азота – пиримидин – в реакции с серной кислотой образует соли только по одному атому азота:

Для многих замещенных гетероциклов с двумя атомами азота, а также для некоторых гетерофункциональных соединений характерно явление таутомерии.
Таутомерия – это равновесная динамическая изомерия, сопровождающаяся миграцией (переносом) подвижной группы между двумя или несколькими реакционными центрами в молекуле. Если осуществляется перенос протона Н+, то таутомерия называется прототропная. Пример прототропной таутомерии – таутомерия гомологов имидазола (перенос протона между двумя атомами азота):
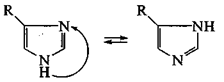
Таким образом, в основе явления таутомерии лежит кислотно-основное взаимодействие. К разновидностям прототропной таутомерии можно отнести лактим-лактамную (перенос протона между атомами азота и кислорода), енамин-иминную (перенос протона между атомами азота и углерода) и кето-енольную (перенос протона между атомами кислорода и углерода).
Первые два вида таутомерии удобно рассмотреть на примере гидрокси- и аминопроизводных пиримидина (соединений, входящих в состав нуклеиновых кислот), например цитозина (прямые стрелки указывают направление смещения таутомерного равновесия; изогнутые – направление миграции протона):

Кето-енольная таутомерия пировиноградной кислоты описывается равновесием:

В большинстве случаев кетонный таутомер оказывается гораздо более устойчивым. Присутствие енольного таутомера, однако, можно подтвердить образованием (при взаимодействии с фосфорной кислотой) фосфоенолпирувата – важнейшего метаболита в процессе гликолиза:

В некоторых случаях может происходить значительная стабилизация енольной формы либо за счет возникновения термодинамически выгодной сопряженной системы, либо за счет образования водородных связей. Так, молекула щавелевоуксусной кислоты преимущественно находится в форме енольного таутомера, поскольку в ней реализуется система сопряженных связей (включает шесть атомов) и образуется внутримолекулярная водородная связь (показана точками):

Производные пиримидина входят в состав ряда алкалоидов и сульфаниламидов.
Присутствие гидроксильных групп придает соответствующим производным пиримидина кислые свойства. Особенно сильные кислотные свойства проявляет 2,4,6- тригидроксипиримидин – барбитуровая кислота – более сильная, чем уксусная.
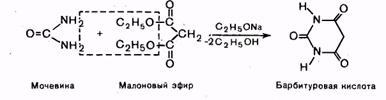
Барбитуровая кислота представляет собой циклический уреид малоновой кислоты. Она может быть получена при взаимодействии малонового эфира с мочевиной в присутствии этоксида натрия.
 |
Для барбитуровой кислоты характерны лактим-лактамная и кето-енольная таутомерии.
Большую роль в качестве снотворных и противосудорожных средств играют 5,5- дизамещенные производные барбитуровой кислоты, так называемые барбитураты. Их получают аналогично барбитуровой кислоте, используя дизамещенные эфиры малоновой кислоты. Для барбитуратов возможна только лактим-лактамная таутомерия. Они легко образуют водорастворимые соли с одним эквивалентом щелочи
 |
 Примерами барбитуратов служат 5,5-диэтилбарбитуровая кислота, барбитал (веронал) R = R’ = C2H5, ее натриевая соль, барбитал-натрий, 5-этил-5-фенилбарбитуровая кислота, фенобарбитал (люминал) R=C2H5, R’ = C6H5.
Примерами барбитуратов служат 5,5-диэтилбарбитуровая кислота, барбитал (веронал) R = R’ = C2H5, ее натриевая соль, барбитал-натрий, 5-этил-5-фенилбарбитуровая кислота, фенобарбитал (люминал) R=C2H5, R’ = C6H5.
Тиамин (витамин В1) – один из важнейших витаминов – содержит два гетероциклических кольца – пиримидиновое и тиазольное, связанные метиленовой группой.
Из бициклических гетероциклов наиболее распространены в природе соединения пуринового и перидинового рядов.
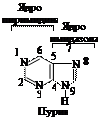 Пурин — бициклическое гетероциклическое соединение, обработанное конденсированными ядрами пиримидина и имидазола
Пурин — бициклическое гетероциклическое соединение, обработанное конденсированными ядрами пиримидина и имидазола
 |
Пуриновая система ароматична. Она включает 8 p-электронов двойных связей и неподеленную пару электронов атома азота в положении 9, что соответствует правилу Хюккеля (4п + 2, где п = 2). Пурин (т. пл. 216 °С) устойчив к действию окислителей, хорошо растворим в воде, амфотерен, образует соли не только с сильными кислотами, но (благодаря наличию NH-группы) и со щелочными металлами. Наиболее важны гидрокси- и аминопурины, принимающие активное участие в процессах жизнедеятельности.
6- Гидроксипурин (гипоксантин), 2,6- дигидроксипурин (ксантин) и 2,6,8- тригидроксипурин (мочевая кислота) – образуются в организме при метаболизме нуклеиновых кислот. У гидроксипуринов возможна как лактим-лактамная таутомерия, так и миграция атома водорода между атомами азота в положениях 7 и 9 имидазольного кольца, по аналогии с имида-золом.
Мочевая кислота – конечный продукт метаболизма пуриновых соединений в организме. Она выделяется с мочой в количестве 0,5-1 г в сутки. Мочевая кислота двухосновна, плохо растворима в воде, но легко растворяется в щелочах, образуя соли с одним или двумя эквивалентами щелочи.
Соли мочевой кислоты называют уратами. При некоторых нарушениях в организме они откладываются в суставах (подагра), а также в виде почечных камней. В результате нагревания мочевой кислоты с азотной кислотой с последующим добавлением аммиака к охлажденной реакционной смеси появляется интенсивное фиолетовое окрашивание. Оно используется для качественного обнаружения соединений, содержащих пуриновое ядро (мурексидная реакция).
По химическому поведению ксантин и гипоксантин в значительной степени аналогичны мочевой кислоте. Они амфотерны и образуют соли с кислотами и щелочами. N-метилзамещенные производные ксантина относятся к алкалоидам.
Аминопурины. Наиболее важные 6-аминопурин, или аденин и 1-амино-6-гидроксипурин, или гуанин, являющиеся обязательными компонентами нуклеиновых кислот. Аденин входит в состав некоторых коферментов. Для аденина возможна прототропная таутомерия за счет миграции атома водорода между N-7 и N-9.
В водных растворах HN-7-таутомер преобладает в 2,5 раза, возможно вследствие внутримолекулярной водородной связи между атомом водорода NH-группы и атомом азота аминогруппы и С-6. Для гуанина возможна также лактим-лактамная таутомерия.
При действии азотистой кислоты на аденин и гуанин происходит их дезаминирование с образованием гипоксантина и ксантина соответственно
 | |||
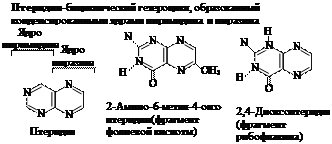 | |||
Птеридиновая система ароматична, устойчива к действию окислителей, проявляет основные свойства. В природе довольно широко распространены гидрокси- и аминоптеридины. В частности, остаток 2-амино-6-метил-4-оксо-птеридина входит в состав фолиевой кислоты, а фрагмент 2,4- диоксоптеридина присутствует в важнейшем витамине рибофлавине – факторе роста живых организмов (витамин В2).
Алкалоидами называют гетероциклические азотсодержащие основания растительного происхождения, обладающие выраженным физиологическим действием. Как правило, алкалоиды представляют собой третичные амины и содержатся в растениях в виде солей органических кислот – лимонной, яблочной, щавелевой, янтарной и др. Их выделение, очистка и установление строения – весьма трудоемкая задача, которая включает использование методов современной органической химии (хроматография, ИК-, УФ- и ЯМР-спектроскопия, масс- спектрометрия, рентгеноструктурный анализ). Алкалоиды – обычно бесцветные кристаллические вещества горького вкуса, практически не растворимые в воде, но растворимые в органических растворителях – эфире, хлороформе, бензоле. Их соли, напротив, хорошо растворимы в воде и не растворимы в органических растворителях. К настоящему времени известно более 5000 алкалоидов. Большинство из них оптически активны. В основе структуры алкалоидов лежит какой-либо гетероцикл. Это обстоятельство учитывается при химической классификации алкалоидов. Ранее применялась также классификация алкалоидов по ботаническому признаку, т. е. по группам растений, из которых они и выделены (алкалоиды пасленовых, алкалоиды опия и т. д.).
Антибиотиками называют вещества, синтезируемые микроорганизмами и способные препятствовать развитию других микроорганизмов.
По химической структуре антибиотики относятся к различным классам органических соединений. Синтез антибиотиков труден, поэтому в промышленных масштабах их получают микробиологическим или полусинтетическим путем.
В основе структуры пенициллинов лежит пенициллановая кислота, содержащая два конденсированных гетероциклических кольца
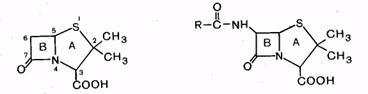
Природные и полусинтетические пенициллины представляют собой N-ацилированные различными ацильными радикалами производные 6-аминопенициллановой кислоты. Природа радикала в ацильной группе учитывается в названии пенициллина. Например, соединение с R = С6Н5СН2– называют бензилпенициллином, а с R = C6H5OCH3 – феноксиметилпенициллином.
6-Аминопенициллановая кислота может рассматриваться как дипептид. Основная особенность строения пенициллинов, долгое время препятствовавшая установлению их структуры, заключается в наличии четырехчленного b-лактамного кольца, не встречавшегося ранее в природных соединениях. b-Лактамное кольцо чрезвычайно лабильно. В мягких условиях оно гидролизуется с разрывом связи С7 – N4, что приводит к потере биологической активности.
Природные пенициллины обладают довольно избирательнымспектром, полусинтетические – гораздо более широким спектром антимикробного действия.
Цефалоспориновые антибиотики близки по строению к пенициллинам а также содержат b-лактамное кольцо. В основе их структуры лежит цефалоспорановая кислота, содержащая два конденсированных гетероциклических кольца – шестичленное частично гидрированное 1,3-тиазиновое (А) и четырехчленное b-лактамное (В).

Антибиотики цефалоспориновой группы являются производными 7- аминоцефалоспорановой кислоты. Они обладают широким спектром действия и тормозят рост некоторых штаммов бактерий, устойчивых к пенициллину.
Стрептомицин относится к аминогликозидам, грамицидин и инсулин – к пептидам, а левомицетин (хлоромицетин) – к производным аминодиола. Этот антибиотик имеет относительно простое строение и является пока единственным, производимым полностью синтетическим путем.

Тетрациклины представляют собой производные частично гидрированного нафтацена – соединения, состоящего из четырех линейно конденсированных шестичленных коциклов. Тетрациклины обладают широким спектром антимикробного действия и могут быть использованы даже при вирусных заболеваниях.
Контрольные задания
1. Воспалительные процессы при подагре вызываются осаждением в суставах мононатриевой соли мочевой кислоты. В какой таутомерной форме мочевая кислота участвует в образовании натриевой соли?
Дата добавления: 2014-04-05; просмотров: 3518; Нарушение авторских прав

Мы поможем в написании ваших работ!