
Главная страница Случайная лекция

Мы поможем в написании ваших работ!
Порталы:
БиологияВойнаГеографияИнформатикаИскусствоИсторияКультураЛингвистикаМатематикаМедицинаОхрана трудаПолитикаПравоПсихологияРелигияТехникаФизикаФилософияЭкономика

Мы поможем в написании ваших работ!
ДИЕНОВЫЕ УГЛЕВОДОРОДЫ
|
Читайте также: |
К диеновым углеводородам относятся органические соединения, содержащие в молекуле две двойные связи. Если в молекуле есть несколько двойных связей, то такие вещества относятся к полиеновым соединениям (например, природный пигмент β-каротин).
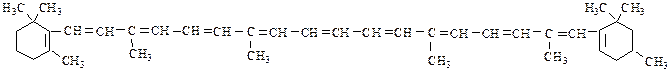
|
При составлении названий веществ перед суффиксом добавляется умножающая приставка ди- (-диен), если три двойных связи в молекуле – три- (-триен), N двойных связей – поли- (-полиен).
|
|
|
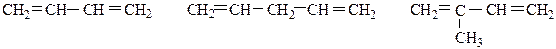
|
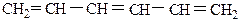
В зависимости от расположения двойных связей различают:
1) сопряженные диены, когда π-связи чередуются одной σ-связью
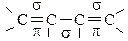
2) изолированные, если двойная связь разделена более чем одной σ-связью
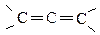
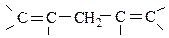
3) кумулированные, когда π-связи расположены рядом
СПОСОБЫ ПОЛУЧЕНИЯ
Способы получения диеновых углеводородов аналогичны способам получения алкенов.
1. Дегидрирование предельных углеводородов происходит при нагревании в присутствии катализаторов (Pt, Ni, Pd, Cr2O3).
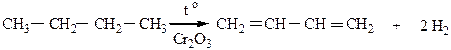
2. Дегидратация непредельных спиртов идет при нагревании в присутствии водоотнимающих средств (H2SO4, H3PO4, Al2O3).
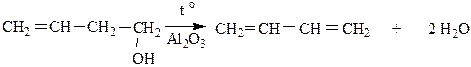
3. Дегидратация гликолей. Условия реакции аналогичны вышеприведенным в п.2.
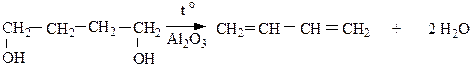
4. Метод Лебедева – промышленный способ получения дивинила из этанола.
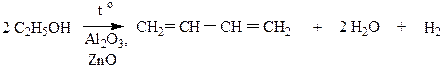
Физические свойства
Основные закономерности изменения физических свойств в гомологическом ряду алкадиенов аналогичны ряду алкенов.
ХИМИЧЕСКИЕ СВОЙСТВА
Для диеновых углеводородов характерны реакции присоединения, окисления и полимеризации, протекающие в условиях, аналогичных для алкенов. Ниже приведены реакции, характеризующие особые свойства сопряженных диенов.
Кумулированные и изолированные диены обладают такими же химическими свойствами, как и алкены; сопряженные – обладают повышенной реакционной способностью и могут вступать как в 1,2–, так и в 1,4– присоединение.
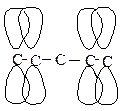 Поведение диеновых углеводородов обусловлено строением их молекул (рис. 4).
Поведение диеновых углеводородов обусловлено строением их молекул (рис. 4).
Изолированные диены
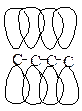 Сопряженные диены
Сопряженные диены
Рис. 4. Электронное строение диеновых углеводородов
В молекулах сопряженных диенов наблюдается π-сопряжение, электронная плотность равномерно распределяется по всем 4-м атомам углерода. Реакции, характерные для диеновых углеводородов, протекают с образованием более устойчивых радикалов или карбкатионов.
|
|
|
|
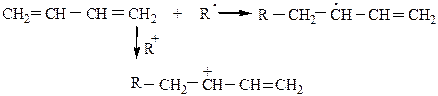
При низких температурах химические реакции для сопряженных диенов идут по типу 1,2– присоединения; при повышенной температуре происходит перегруппировка с образованием аллильного радикала или карбкатиона, вследствие чего протекает 1,4– присоединение.
1. Реакции присоединения.
1) Галогенирование
|
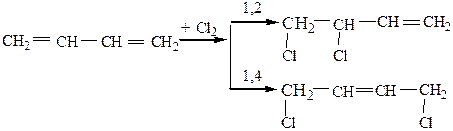
2) Гидрогалогенирование
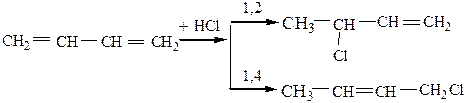
3) Гидрирование
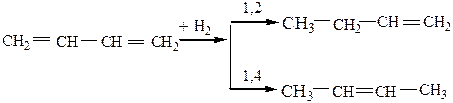
2. Реакции полимеризации.
|
|
|
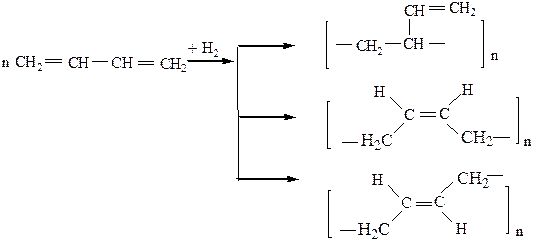
3. Димеризация.
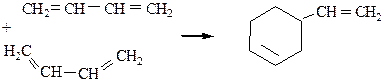
4. Диеновый синтез.
|
|
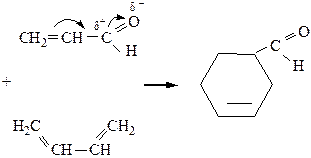
АЛКИНЫ
Алкинами называются непредельные углеводороды, содержащие в своем составе тройную связь 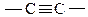 . Общая формула алкинов CnH2n-2. Тип гибридизации углеродных атомов, связанных тройной связью – sp, т.е. углерод находится в третьем валентном состоянии (гибридизованы только две орбитали: s и p). σ-связь лежит в одной плоскости, две π-связи – во взаимно перпендикулярных областях образуются негибридизованными р-орбиталями атомов углерода (рис. 5).
. Общая формула алкинов CnH2n-2. Тип гибридизации углеродных атомов, связанных тройной связью – sp, т.е. углерод находится в третьем валентном состоянии (гибридизованы только две орбитали: s и p). σ-связь лежит в одной плоскости, две π-связи – во взаимно перпендикулярных областях образуются негибридизованными р-орбиталями атомов углерода (рис. 5).
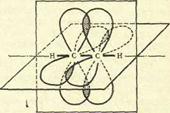
Рис. 5. Пространственное расположение орбиталей в молекуле ацетилена.
Угол σ-связей равен 180 оС. Длина связей С-С равна 0,120 нм, С-Н – 0,106 нм.
НОМЕНКЛАТУРА, ИЗОМЕРИЯ.
Первый представитель гомологического ряда алкинов – ацетилен НС≡СН.
При составлении названия гомологов ацетилена в названии соответствующего алкана суффикс «–ан» заменяется на «–ин».
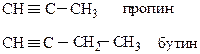
Структурная изомерия связана со строением углеродного скелета и положением тройной связи.
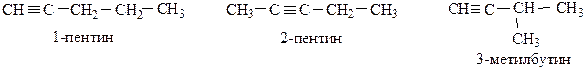
Геометрическая изомерия в ряду алкинов отсутствует.
СПОСОБЫ ПОЛУЧЕНИЯ
Наибольшее практическое применение из алкинов имеет ацетилен. В промышленности его получают следующими способами.
1. Получение из карбида кальция (способ Велера)

2. Термический крекинг (из алканов С1-С4 под действием высокой температуры)
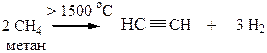
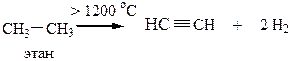
Способы получения гомологов ацетилена можно разделить на следующие.
1) Из вицинальных дигалогенопроизводных. Действием КОН спиртового раствора или твердой щелочи КОН последовательно получаются двойная, а затем тройная связь.
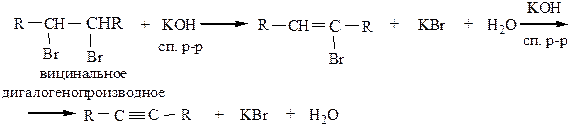
2) Из геминальных дигалогенопроизводных в условиях, аналогичных предыдущей реакции, можно получить какой-либо гомолог ацетилена.
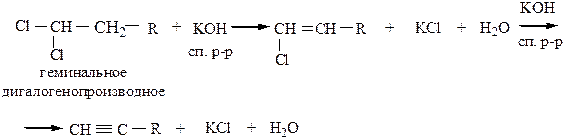
3) Алкилирование металлорганических производных ацетилена. При взаимодействии ацетиленидов натрия, серебра и др. с галогенопроизводными могуь быть получены алкины заданного строения.

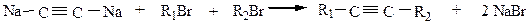
Физические свойства.
Гомологи С2–С4 (за исключением 1-бутина) – газы, С5–С15 – жидкости, С15 и более – твердые вещества. Закономерности в изменении tпл., tкип., и ρ – такие же, как у алкенов.
ХИМИЧЕСКИЕ СВОЙСТВА
Поведение алкинов связано с наличием в их молекулах тройной связи. Для углеводородов этого класса характерны реакции присоединения, полимеризации, окисления и замещения атома водорода у тройной связи.
Реакции присоединения протекают ступенчато с образованием алкенов или их производных, затем алканов (или их производных). Так как в молекулах алкинов атомы углерода, связанные тройной связью, находятся в состоянии sp-гибридизации, они расположены ближе друг к другу и более электроотрицательны, чем атомы углерода, связанные двойной связью в алкенах. π-электроны тройной связи втянуты внутрь молекулы, поэтому атомы углерода меньше экранированы с внешней стороны. Поляризуемость π-связи 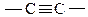 уменьшена, поэтому алкины легче присоединяют нуклеофильные реагенты, труднее – электрофильные. 1-алкины проявляют кислотные свойства и могут отдавать атом Н, стоящий у тройной связи, замещая его на атом металла и образуя при этом ацетилениды.
уменьшена, поэтому алкины легче присоединяют нуклеофильные реагенты, труднее – электрофильные. 1-алкины проявляют кислотные свойства и могут отдавать атом Н, стоящий у тройной связи, замещая его на атом металла и образуя при этом ацетилениды.
1) Гидрирование. Присоединение водорода в присутствии катализатора (Ni, Pt или Pd) происходит ступенчато, с образованием вначале алкена, затем алкана.
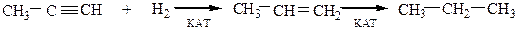
2) Галогенирование – присоединение Br2 или Cl2 по тройной связи идет с меньшей скоростью, чем у алкенов.
Присоединение Br2 в Cl4 является качественной реакцией и на тройную связь, так как при этом бромная вода обесцвечивается.
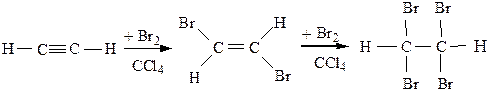
3) Гидрогалогенирование – присоединение галогеноводородов (HBr или HCl) идет по электрофильному механизму (аналогично алкенам) по правилу Марковникова)
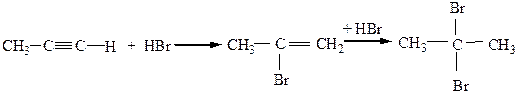
4) Гидратация (присоединение воды) происходит в присутствии солей двухвалентной ртути или кадмия (реакция Кучерова). Гидратация ацетилена приводит к образованию альдегида, остальных алкинов – к образованию соответствующего кетона
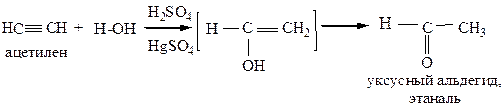
Виниловый спирт, образующийся на промежуточной стадии неустойчив согласно правилу Эльтекова: гидроксил у двойной связи неустойчив, в результате чего происходит внутримолекулярная перегруппировка с образованием соответствующего карбонильного соединения.
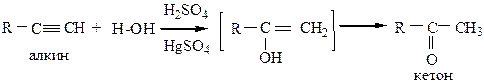
5) Присоединение спиртов (реакция Фаворского и Шостаковского) происходит в присутствии твердых щелочей при нагревании по правилу Марковникова
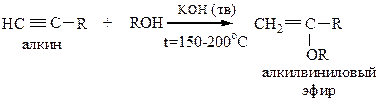
6) Присоединение карбоновых кислот протекает по правилу Марковникова в присутствии H3PO4 как катализатора
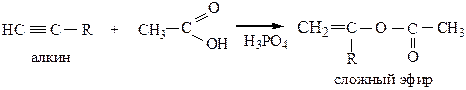
7) Присоединение синильной кислоты идет по правилу Марковникова при участии в качестве катализатора раствора, содержащего хлорид меди.
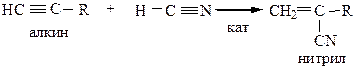
8) Реакция Ренке – присоединение оксида углерода и спиртов – происходит в присутствии катализатора Ni(Co)4.
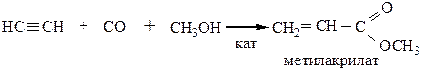
9) Реакции замещения ацетиленового атома водорода. 1-алкины обладают слабыми кислотными свойствами, т.к. могут под действием некоторых реагентов отщеплять Н+. Это связано с тем, что атомы углерода у тройной связи обладают повышенной электроотрицательностью:
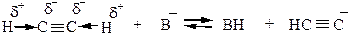
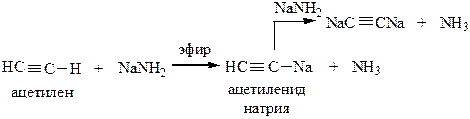
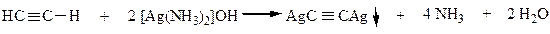
Реакция с аммиачным раствором гидроксида серебра является качественной реакцией на концевую тройную связь.
Ацетилениды в сухом виде являются взрывоопасными веществами.
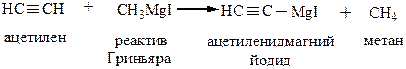
Металлорганические производные ацетилена: CH≡CMgI и CH≡CNa – используются для получения гомологов ацетилена.
10) Присоединение альдегидов и кетонов происходит по нуклеофильному механизму, также является реакцией проявления алкинами кислотных свойств.
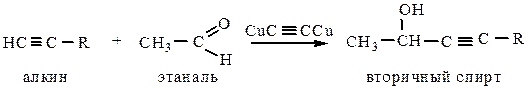
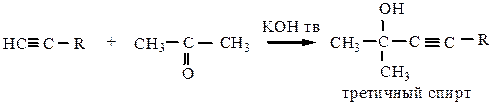
11) Окисление алкинов происходит по тройной связи с ее разрывом. При действии окислителей (KMnO4, концентрированных кислот, хромовой смеси) образуется смесь карбоновых кислот.
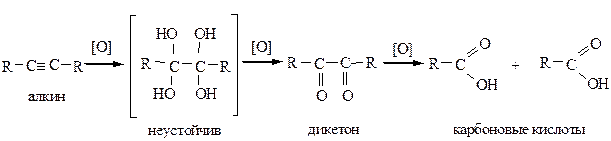
Алкины окисляются в условиях реакции Вагнера (разбавленным раствором KMnO4), т.е. она является качественной и на тройную связь.
При полном окислении (горении) образуется смесь СО2 и Н2О с выделением большого количества теплоты.
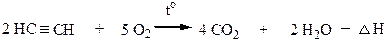
12) Изомеризация (реакция Фаворского) – реакция, в результате которой тройная связь перемещается из конца в середину молекулы под действием спиртовых растворов щелочей.
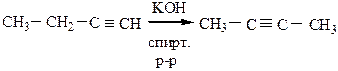
13) Полимеризация. В зависимости от условий реакции, при полимеризации могут образовываться различные продукты, применяющиеся в химической промышленности.
а) Реакция Зелинского – образование бензола при нагревании ацетилена над активированным углем при температуре до 450 оС.
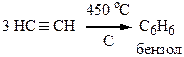
б) Образование винилацетилена.
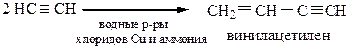
в) В общем виде реакция полимеризации может быть записана в следующем виде:
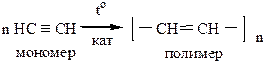
АРЕНЫ
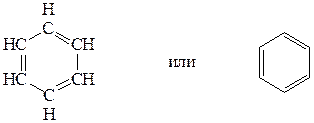 Ароматические соединения(арены) – это соединения, содержащие в своей структуре бензольное ядро – особую циклическую группировку из шести атомов углерода:
Ароматические соединения(арены) – это соединения, содержащие в своей структуре бензольное ядро – особую циклическую группировку из шести атомов углерода:
По количеству бензольных группировок арены делятся на одноядерные и многоядерные, в качестве боковых цепочек они могут содержать различные алифатические, циклические группировки, либо функциональные группы.
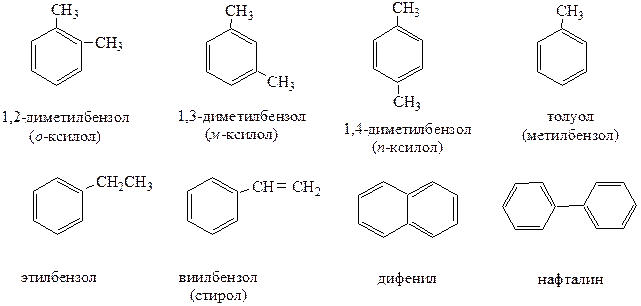
| <== предыдущая страница | | | следующая страница ==> |
| ХИМИЧЕСКИЕ СВОЙСТВА | | | ОДНОЯДЕРНЫЕ АРОМАТИЧЕСКИЕ УГЛЕВОДОРДЫ |
Дата добавления: 2014-04-15; просмотров: 2250; Нарушение авторских прав

Мы поможем в написании ваших работ!